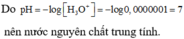a.Nếu dung dịch có pH=4 thì tích số ion [H* ||OH | trong dung dịch đó sẽ là? b.Khi dung dịch có pH = 0 thì [H+] trong dung dịch bằng mấy? c.Khi bạn để dư quần áo lâu ngày có mùi chua vậy khi đó khắp người bạn sẽ có môi trường gì? pH như thế nào?

Những câu hỏi liên quan
Độ pH của một dung dịch được tính theo công thức pH-log[H+] với [H+] là nồng độ ion H+ trong dung dịch đó. Cho dung dịch A có độ pH ban đầu bằng 6. Nếu nồng độ ion H+ trong dung dịch A tăng lên 4 lần thì độ pH trong dung dịch mới gần bằng giá trị nào dưới đây? A. 5,2 B. 6,6 C. 5,7 D. 5,4
Đọc tiếp
Độ pH của một dung dịch được tính theo công thức pH=-log[H+] với [H+] là nồng độ ion H+ trong dung dịch đó. Cho dung dịch A có độ pH ban đầu bằng 6. Nếu nồng độ ion H+ trong dung dịch A tăng lên 4 lần thì độ pH trong dung dịch mới gần bằng giá trị nào dưới đây?
A. 5,2
B. 6,6
C. 5,7
D. 5,4
Độ pH của một dung dịch được tính theo công thức
p
H
-
log
H
+
với
H
+
là nồng độ ion
H
+
trong dung dịch đó. Cho dung dịch A có độ pH ban đầu bằng 6. Nếu nồng độ ion
H
+
trong dung dịch A tăng lên 4 lần thì độ pH trong dung dịch mới gần bằng giá...
Đọc tiếp
Độ pH của một dung dịch được tính theo công thức p H = - log H + với H + là nồng độ ion H + trong dung dịch đó. Cho dung dịch A có độ pH ban đầu bằng 6. Nếu nồng độ ion H + trong dung dịch A tăng lên 4 lần thì độ pH trong dung dịch mới gần bằng giá trị nào dưới đây?
A. 5,2
B. 6,6
C. 5,7
D. 5,4
Dung dịch axit fomic 0,007M có pH = 3. Kết luận nào sau đây không đúng?
A.Khi pha loãng 10 lần dung dịch trên thì thu được dung dịch có pH = 4.
B.Khi pha loãng dung dịch trên thì độ điện li của axit fomic tăng.
C.Độ điện li của axit fomic trong dung dịch trên là 14,29%.
D.Độ điện li của axit fomic sẽ giảm khi thêm dung dịch HCl.
Trước khi pha loãng: pH = 3 → [H+] = 10-3 → nH+ = 10-3V1 (mol).
Sau khi pha loãng: nH+ = 10-pHV2 (mol) = 10-pH .10V1 (mol)
Do số mol sau pha loãng > trước pha loãng nên: pH < 4
Đúng 0
Bình luận (0)
Tính số mol, nồng độ mol ion H+ và OH- và pH của dung dịch axit b) HNO3 0,04M c) dung dịch HCl 0.001M d) dung dịch H2SO4 0,003M e) dung dịch HNO3 có pH=2 f) dung dịch H2SO4 có pH=4 g) 200ml dung dịch H2SO4 0,01M + 100ml dung dịch HCl 0,05M Giúp em với ạ
Để biết dung dịch có tính axit, tính bazo, hay trung tính, người ta dùng độ pH đế xác định, biết
pH
-
log
H
3
O
+
Trong đó, pH: là hai chữ đầu của nhóm từ “potential of hydrogen” nghĩa là tiềm lực của hiđrô, pH 7 Dung dịch có tính axít; pH 7 Dung dịch có tính bazơ; pH7 Dung dịch trung tính. Hỏi nếu dung dịch nước nguyên chất có n...
Đọc tiếp
Để biết dung dịch có tính axit, tính bazo, hay trung tính, người ta dùng độ pH đế xác định, biết pH = - log H 3 O + Trong đó, pH: là hai chữ đầu của nhóm từ “potential of hydrogen” nghĩa là tiềm lực của hiđrô, pH < 7 Dung dịch có tính axít; pH > 7 Dung dịch có tính bazơ; pH=7 Dung dịch trung tính. Hỏi nếu dung dịch nước nguyên chất có nồng độ ion hiđrô H 3 O + = 0 , 0000001 thì nước nguyên chất có tính chất gì?
A. Trung tính
B. Không xác định
C. Tính bazo
D. Tính axít
Trộn 100 ml dung dịch NaOH có pH 11 với 50 ml dung dịch KOH có pH 12 thu được dung dịch X. Nồng độ ion OH trong dung dịch X là A.
7
.
10
-
12
M
B.
4
,
3
.
10
-
11
M
C.
4
.
10
-
3...
Đọc tiếp
Trộn 100 ml dung dịch NaOH có pH = 11 với 50 ml dung dịch KOH có pH = 12 thu được dung dịch X. Nồng độ ion OH trong dung dịch X là
A. 7 . 10 - 12 M
B. 4 , 3 . 10 - 11 M
C. 4 . 10 - 3 M
D. 7 , 3 . 10 - 2 M
Chọn C
pH = 11 → [ OH - ] = 10 - 3 (M)
pH = 12 → [ OH - ] = 10 - 2 (M)
Tổng số mol OH - có trong dung dịch X là: n = 0 , 1 . 10 - 3 + 0 , 05 . 10 - 2 = 6 . 10 - 4 (mol)
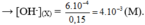
Đúng 0
Bình luận (0)
Cho dung dịch chứa các ion sau: K+, Ca2+, Ba2+, Mg2+, H+, Cl-. Muốn tách được nhiều cation ra khỏi dung dịch mà không đưa ion lạ vào đó thì ta có thể cho dung dịch trên tác dụng với dung dịch nào trong số các dung dịch sau A. Na2SO4 vừa đủ B. K2CO3 vừa đủ C. NaOH vừa đủ D. Na2CO3 vừa đủ
Đọc tiếp
Cho dung dịch chứa các ion sau: K+, Ca2+, Ba2+, Mg2+, H+, Cl-. Muốn tách được nhiều cation ra khỏi dung dịch mà không đưa ion lạ vào đó thì ta có thể cho dung dịch trên tác dụng với dung dịch nào trong số các dung dịch sau
A. Na2SO4 vừa đủ
B. K2CO3 vừa đủ
C. NaOH vừa đủ
D. Na2CO3 vừa đủ
Cho các nhận xét sau: (1) Khi cho anilin vào dung dịch HCl dư thì tạo thành dung dịch đồng nhất trong suốt. (2) Khi sục CO2 vào dung dịch natriphenolat thì thấy vẩn đục. (3) Khi cho Cu(OH)2 vào dung dịch glucozơ có chứa NaOH ở nhiệt độ thường thì xuất hiện kết tủa đỏ gạch. (4) Dung dịch HCl, dung dịch NaOH, đều có thể nhận biết anilin và phenol trong các lọ riêng biệt. (5) Để nhận biết glixerol và saccarozơ có thể dùng Cu(OH)2 trong môi trường kiềm. Số nhận xét đúng là: A. 2 B. 4 C. 1 D. 3
Đọc tiếp
Cho các nhận xét sau:
(1) Khi cho anilin vào dung dịch HCl dư thì tạo thành dung dịch đồng nhất trong suốt.
(2) Khi sục CO2 vào dung dịch natriphenolat thì thấy vẩn đục.
(3) Khi cho Cu(OH)2 vào dung dịch glucozơ có chứa NaOH ở nhiệt độ thường thì xuất hiện kết tủa đỏ gạch.
(4) Dung dịch HCl, dung dịch NaOH, đều có thể nhận biết anilin và phenol trong các lọ riêng biệt.
(5) Để nhận biết glixerol và saccarozơ có thể dùng Cu(OH)2 trong môi trường kiềm.
Số nhận xét đúng là:
A. 2
B. 4
C. 1
D. 3
Chọn D
(1) Khi cho anilin vào dung dịch HCl dư thì tạo thành dung dịch đồng nhất trong suốt.
(2) Khi sục CO2 vào dung dịch natriphenolat thì thấy vẩn đục
(4) Dung dịch HCl, dung dịch NaOH, đều có thể nhận biết anilin và phenol trong các lọ riêng biệt
Đúng 0
Bình luận (0)
một dung dịch có pH=9,0 . Tính nồng độ mol của các ion H+ và OH- trong dung dịch . hãy cho biết màu của phenolphtalein trong dung dịch này .
[OH-] = 10^-14 : [H+] = 10^-12
pH = -log[H+] = 2 <7 => mt axit
pH = 9 => [H+] = 10^-9 => [OH-] = 10^-5 => mt bazo, phenolphtalein chuyển hồng
Đúng 0
Bình luận (0)