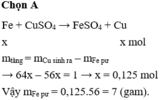cho 7g Al vào dung dịch muối CuCl2 ,sau 1 thời gian , lấy ra rửa sạch làm khô , cân thấy khối lượng nhôm tăng 13,8g , Khối lượng Al tham gia phản ứng là ?

Những câu hỏi liên quan
cho 7g Al vào dung dịch muối CuCl2 ,sau 1 thời gian , lấy ra rửa sạch làm khô , cân thấy khối lượng nhôm tăng 13,8g , Khối lượng Al tham gia phản ứng là ?
Đáp án : 5,4g . Giải thích tại sao ?
Hòa tan 11,2g Fe vào 200ml dung dịch CuSO4. Sau một thời gian lấy lá sắt ra, rửa nhẹ, lau khô và đem cân thấy khối lượng kim loại tăng 0,8g. Tính khối lượng Fe đã tham gia phản ứng và khối lượng Cu sinh ra sau phản ứng?
PTHH: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
Đặt \(n_{Fe\left(phản.ứng\right)}=x\left(mol\right)=n_{Cu\left(tạo.ra\right)}\)
\(\Rightarrow64x-56x=0,8\) \(\Rightarrow x=0,1\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe\left(phản.ứng\right)}=0,1\cdot56=5,6\left(g\right)\\m_{Cu\left(tạo.ra\right)}=0,1\cdot64=6,4\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Nhúng 1 thanh Al có khối lượng 50g vào 250ml dd AgNO3 0,4M. Sau một thời gian lấy thanh Al ra ,rửa sạch ,làm khô cân nặng 52,97g
A/ Tính khối lượng Al phản ứng và Ag sinh ra
B/tính nồng độ mol các chất yỏng dung dịch sau pứ .biết rằng Vdd thay đổi ko đáng kể
nAgNO3= 0,1 (mol)
Al + 3AgNO3 \(\rightarrow\) Al(NO3)3 + 3Ag
Cứ 1 mol Al pư thì khối lượng thanh Al tăng 297 g
0,01 mol <--------------------------------------- (52,97 - 50)
a) mAl pư = 0,01 . 27=,27 (g)
Theo pt nAg = 3nAl=3 . 0,01 = 0,03 (mol) = nAgNO3 pư
mAg=0,03 . 108 = 3,24 (g)
b)nAgNO3 dư = 0,1 - 0,03 = 0,07 (mol)
CM (AgNO3)= \(\frac{0,07}{0,25}\) = 0,28 (M)
CM (Al(NO3)3) = \(\frac{0,01}{0,25}\) = 0,04 (M)
Đúng 0
Bình luận (0)
Nhúng một lá nhôm vào dung dịch CuSO 4 . Sau một thời gian, lấy lá nhôm ra khỏi dung dịch thì thấy khối lượng dung dịch giảm 1,38 gám. Khối lượng của Al đã tham gia phản ứng là
A. 0,27 gam ; B. 0,81 gam ; C. 0,54 gam ; D. 1,08 gam.
Đáp án C.
Gọi khối lượng miếng Al là a gam, lượng nhôm đã phản ứng là x gam :
2Al + 3 CuSO 4 → Al 2 SO 4 3 + 3 Cu
Gọi x là khối lượng Al phản ứng.
![]()
So với khối lượng miếng Al ban đầu thì khối lượng miếng Al sau phản ứng tăng 1,38 gam.
Đúng 0
Bình luận (0)
Nhúng thanh Fe vào dung dịch CuSO4. Sau một thời gian phản ứng, lấy thanh Fe ra rửa nhẹ, làm khô, đem cân thấy khối lượng thanh Fe tăng thêm 1,6 gam. Khối lượng Cu bám trên thanh Fe là
A. 6,4gam
B. 12,8gam
C. 8,2gam
D. 9,6gam
Chọn đáp án B.
Áp dụng tăng giảm khối lượng có:
n C u = 1 , 6 64 - 56 = 0 , 2 m o l
⇒ m C u = 64 . 0 , 2 = 12 , 8 gam
Đúng 0
Bình luận (0)
Nhúng thanh Fe vào dung dịch CuSO4. Sau một thời gian phản ứng, lấy thanh Fe ra rửa nhẹ, làm khô, đem cân thấy khối lượng thanh Fe tăng thêm 1,6 gam. Khối lượng Cu bám trên thanh Fe là A. 6,4gam B. 12,8gam, C. 8,2gam. D. 9,6gam.
Đọc tiếp
Nhúng thanh Fe vào dung dịch CuSO4. Sau một thời gian phản ứng, lấy thanh Fe ra rửa nhẹ, làm khô, đem cân thấy khối lượng thanh Fe tăng thêm 1,6 gam. Khối lượng Cu bám trên thanh Fe là
A. 6,4gam
B. 12,8gam,
C. 8,2gam.
D. 9,6gam.
Đáp án B
Áp dụng tăng giảm khối lượng có:
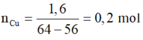
![]()
Đúng 0
Bình luận (0)
Cho 333g hh: \(MgSO_4;CuSO_4;BaSO_4\) vào nước thu được dung dịch D và 1 phần không tan C có khối lượng 233g. Nhúng thanh Al vào dung dịch D sau phản ứng nhấc thanh Al ra khỏi dung dịch, làm sạch, sấy khô, thấy khối lượng thanh Al tăng 11,5g
a) Viết pt
b) Tính khối lượng mỗi muối trong hỗn hợp ban đầu
\(MgSO_4;CuSO_4;BaSO_4+H_2O\)
\(\Rightarrow\) Dung dịch D gồm \(MgSO_4;CuSO_4\)
\(\Rightarrow\) Phần không tan là \(BaSO_4\)\(\Leftrightarrow m_{BaSO_4}=233\left(g\right)\)
Vậy \(m_{MgSO_4;CuSO_4}=m_{hh}-m_{BaSO_4}=333-233=100\left(g\right)\)
\(3CuSO_4+2Al\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
TĐB: 1,5x x 1,5x (mol)
Gọi x là số mol của Al
\(m\) khối lượng tăng= \(m_{Cu}-m_{Al}\)
\(\Leftrightarrow11,5=1,5x.64-27x\)
\(\Leftrightarrow11,5=96x-27x\)
\(\Leftrightarrow11,5=69x\)
\(\Leftrightarrow x=\dfrac{1}{6}\left(mol\right)\)
\(m_{CuSO_4}=n.M=1,5x.160=1,5.\dfrac{1}{6}.160=40\left(g\right)\)
\(m_{MgSO_4}=m_{MgSO_4;CuSO_4}-m_{CuSO_4}=100-40=60\left(g\right)\)
Đúng 2
Bình luận (0)
Ngâm một đinh sắt trong dung dịch C u S O 4 , sau một thời gian lấy đinh sắt ra, sấy khô, đem cân thấy khối lượng tăng 1g. Khối lượng Fe tham gia phản ứng là
A. 7g.
B. 8g.
C. 5,6g.
D. 8,4g.
Cho đinh sắt có khối lượng 2,3 gam vào dung dịch CuSO4. Sau một thời gian lấy đinh ra, rửa nhẹ, làm khô, cân thấy khối lượng là 3,5 gam. Tính Khối lượng muối sắt tạo ra là?
Tham khảo:
PTHH: Fe + CuSo4 ---->FeSo4 + Cu
Gọi a(mol) là số mol của Fe phản ứng
mCu - mFe = 3.5 - 2.3 = 1.2(g)
<--> 64a - 56a = 1.2
<--> 8a = 1.2
<--> a = 0.15
Dựa vào PTHH: nFe = nFeSo4 = 0.15(mol)
--> mFeSo4 = 0.15×152 = 22.8(g)
Đúng 1
Bình luận (0)