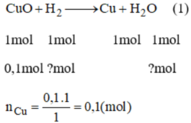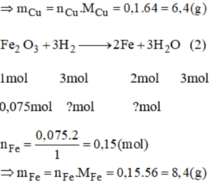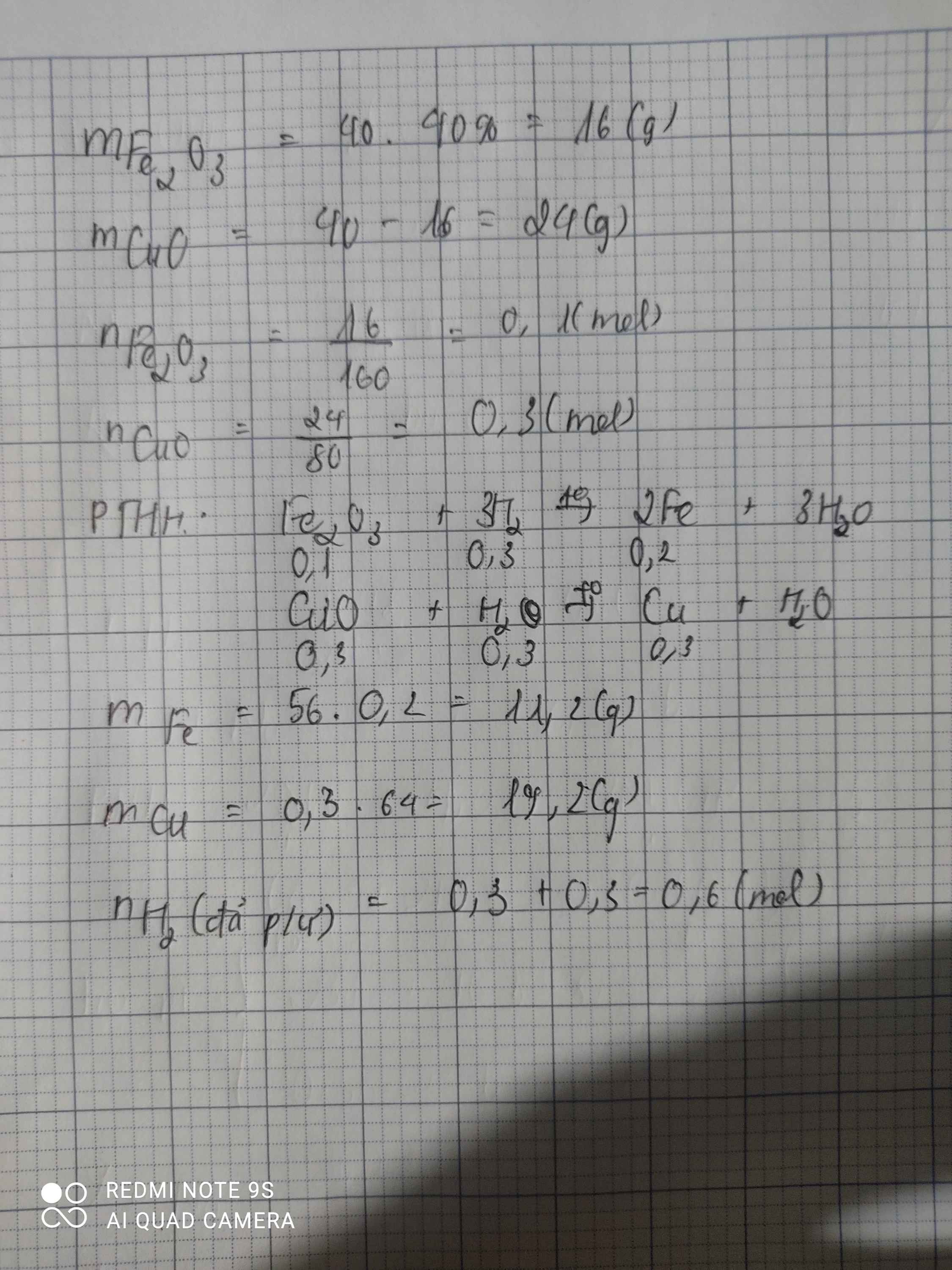Có một hỗn hợp 75% Fe\(_2\)O\(_3\) và 25% CuO, người ta cần dùng H\(_2\) để khử 16g hỗn hợp đó. Tính khối lượng Fe và Cu thu được và thuể tích khí Hydro đã tham gia phản ứng.

Những câu hỏi liên quan
có một hỗn hợp gồm 75%Fe2O3 và 25%CuO.N gười ta dùng H2 để khử 16g hỗn hợp đó.a) Tính khối lượng Fe và Cu thu đc sau phản ứngb)Tính thể tích H2 đã tham gia phản ứng (đktc) cần gắp nha
Xem chi tiết
\(a) n_{Fe_2O_3} = \dfrac{16.75\%}{160} = 0,075(mol)\\ n_{CuO} = \dfrac{16.25\%}{80} = 0,05(mol)\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{Fe} = 2n_{Fe_2O_3} = 0,15(mol) \Rightarrow m_{Fe} = 0,15.56 = 8,4(gam)\\ n_{Cu} = n_{CuO} = 0,05(mol) \Rightarrow m_{Cu} = 0,05.64 = 3,2(gam)\\ b) n_{H_2} = 3n_{Fe_2O_3} + n_{CuO} = 0,075.3 + 0,05 = 0,275(mol)\\ V_{H_2} = 0,275.22,4 = 6,16(lít)\)
Đúng 2
Bình luận (0)
Người ta dùng H2 (dư) để khử 16g hỗn hợp gồm 75% Fe2O3 và 25% CuO.
a. Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng
b. Tính số mol H2 đã tham gia phản ứng.
\(m_{Fe_2O_3}=16\cdot75\%=12\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{12}{160}=0.075\left(mol\right)\)
\(n_{CuO}=16\cdot25\%=4\left(g\right)\)
\(n_{CuO}=\dfrac{4}{80}=0.05\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(n_{H_2}=3\cdot0.075+0.05=0.275\left(mol\right)\)
Đúng 1
Bình luận (1)
a,\(m_{Fe_2O_3}=16.75\%=12\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
\(m_{CuO}=16-12=4\left(g\right)\Rightarrow n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,075 0,225 0,15
PTHH: CuO + H2 → Cu + H2O
Mol: 0,05 0,05 0,05
\(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right);m_{Cu}=0,05.64=3,2\left(g\right)\)
b,\(n_{H_2}=0,225+0,05=0,275\left(mol\right)\)
Đúng 0
Bình luận (1)
giúp em câu này với ạ,em đang cần gấp.em cảm ơn.
câu 4: có một hỗn hợp gồm 75% Fe2O3 và 25% CuO. Người ta dùng hiđro dư để khử 32g hỗn hợp đó
a) tính khối lượng Fe và Cu thu được sau phản ứng
b) tính thể tích khí H2 (đktc) đã tham gia phản ứng
c) tính khối lượng nhôm và axit clohiđric cần dùng để điều chế được thể tích khí hiđro nói trên
a, mFe2O3 = 32 . 75% = 24 (g)
nFe2O3 = 24/160 = 0,15 (mol)
mCuO = 32 - 24 = 8 (g)
nCuO = 8/80 = 0,1 (mol)
PTHH:
Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
0,15 ---> 0,45 ---> 0,3
CuO + H2 -> (t°) Cu + H2O
0,1 ---> 0,1 ---> 0,1
mFe = 0,3 . 56 = 16,8 (g)
mCu = 64 . 0,1 = 6,4 (g)
b, nH2 = 0,1 + 0,45 = 0,55 (mol)
VH2 = 0,55 . 22,4 = 12,32 (l)
c, PTHH:
2Al + 6HCl -> 2AlCl3 + 3H2
11/30 <--- 1,1 <--- 11/30 <--- 0,55
mAl = 11/30 . 27 = 9,9 (g)
mHCl = 1,1 . 36,5 = 40,15 (g)
Đúng 2
Bình luận (0)
Câu 1: Hòa tan 16,24 gam hỗn hợp bột kẽm và nhôm trong HCl dư, thu được 8,512 lít H_2 (đktc). Khối lượng của mỗi kim loại trong hỗn hợp ban đầu lần lượt là bao nhiêu?Câu 2: Hòa tan 7,2 gam một oxit sắt có dạng (Fe_xOy) vào HCl dư, thu được 14,625 gam muối sắt clorua khan. Xác định công thức của oxit sắt đem dùng.Câu 3: Nếu lấy cùng khối lượng các kim loại: Ba, Ca, Fe, Al cho phản ứng lần lượt với HCl dư thì thể tích khí H_2 (đktc) thu được lớn nhất thoát ra từ kim loại nào?Câu 4:Nếu dùng khí CO...
Đọc tiếp
Câu 1: Hòa tan 16,24 gam hỗn hợp bột kẽm và nhôm trong HCl dư, thu được 8,512 lít H\(_2\) (đktc). Khối lượng của mỗi kim loại trong hỗn hợp ban đầu lần lượt là bao nhiêu?
Câu 2: Hòa tan 7,2 gam một oxit sắt có dạng (Fe\(_x\)O\(y\)) vào HCl dư, thu được 14,625 gam muối sắt clorua khan. Xác định công thức của oxit sắt đem dùng.
Câu 3: Nếu lấy cùng khối lượng các kim loại: Ba, Ca, Fe, Al cho phản ứng lần lượt với HCl dư thì thể tích khí H\(_2\) (đktc) thu được lớn nhất thoát ra từ kim loại nào?
Câu 4:Nếu dùng khí CO để khử 80 gam hỗn hợp gồm CuO và Fe\(_2\)O\(_3\), trong đó Fe\(_2\)O\(_3\) chiếm 60% khối lượng hỗn hợp. Thể tích khí CO (đktc) cần dùng là bao nhiêu?
Câu 5: Để điều chế hợp chất khí hiđro clorua, người ta cần dẫn 25 lít H\(_2\) và 25 lít Cl\(_2\)vào tháp tổng hợp ở nhiệt độ cao. Thể tích khí hiđro clorua thu được sau phản ứng là bao nhiêu?
P/s: Giải kỹ với ạ, mơn.
Câu 5:
PTHH : H2+ Cl2 -to-> 2 HCl
Vì số mol , tỉ lệ thuận theo thể tích , nên ta có:
25/1 = 25/1 => P.ứ hết, không có chất dư, tính theo chất nào cũng được
=> V(HCl)= 2. V(H2)= 2. 25= 50(l)
Câu 4: mFe2O3= 0,6. 80= 48(g)
=> nFe2O3= 48/160=0,3(mol)
mCuO= 80-48=32(g) => nCuO=32/80=0,4(mol)
PTHH: CuO + CO -to-> Cu + CO2
0,4_______0,4_____0,4____0,4(mol)
Fe2O3 + 3 CO -to-> 2 Fe +3 CO2
0,3_____0,9____0,6______0,9(mol)
=>nCO= 0,4+ 0,9= 1,3(mol)
=> V(CO, đktc)= 1,3. 22,4=29,12(l)
Có một hỗn hợp gồm 60% F e 2 O 3 và 40% CuO. Người ta dùng H 2 ( dư) để khử 20g hỗn hợp đó. Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng.
có 40g hỗn hợp gồm 40% Fe2O3 và 60% CuO người ta dùng h2 ( dư) để khử hỗn hợp đó . a, Tính klg Fe và Cu thu đc sau phản ứng b, Tính số mol H2 đã tham gia phản ứng
dùng 9.10\(^{23}\) tất cả khí hidro để khử Fe\(_2\)O\(_3\)
a) tính khối lượng Fe\(_2\)O\(_3\) đã phản ứng
b) tính khối lượng kim loại thu đc
a. \(n_{H_2}=\dfrac{9.10^{23}}{6.10^{23}}=1,5\left(mol\right)\)
PTHH : Fe2O3 + 3H2 -> 2Fe + 3H2O
0,5 1,5 1
\(m_{Fe_2O_3}=0,5.160=80\left(g\right)\)
b. \(m_{Fe}=1.56=56\left(g\right)\)
Đúng 2
Bình luận (0)
nH2 = 9.10^23/6.10^23 = 1,5 (mol)
PTHH: Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
Mol: 0,5 <--- 1,5 ---> 1
mFe2O3 = 0,5 . 160 = 80 (g)
mFe = 1 . 56 = 56 (g)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Dùng H² để khử 50g hỗn hợp CuO và Fe²O³ , trong đó Fe²O³ chiếm 80% khối lượng hỗn hợp a) viết pthh b) tính khối lượng mỗi kim loại thu được c) tính thể tích khí H² cần dùng
a, PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, Ta có: \(m_{Fe_2O_3}=50.80\%=40\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{40}{160}=0,25\left(mol\right)\)
\(\Rightarrow m_{CuO}=10\left(g\right)\Rightarrow n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{Cu}=n_{CuO}=0,125\left(mol\right)\\n_{Fe}=2n_{Fe_2O_3}=0,5\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Cu}=0,125.64=8\left(g\right)\\m_{Fe}=0,5.56=28\left(g\right)\end{matrix}\right.\)
b, Theo PT: \(n_{H_2}=n_{CuO}+3n_{Fe_2O_3}=0,875\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,875.22,4=19,6\left(l\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Bài 6: Cho H2 khử 20 gam hỗn hợp Fe2O3 và CuO trong đó CuO chiếm 40% khối lượng.
a) Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng?
b) Tính thể tích khí Hiđro (đktc) cần dùng?
a) \(m_{CuO}=\dfrac{20.40}{100}=8\left(g\right)\) => \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(m_{Fe_2O_3}=20-8=12\left(g\right)\) => \(n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,1--->0,1------>0,1
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,075--->0,225----->0,15
=> mCu = 0,1.64 = 6,4 (g)
=> mFe = 0,15.56 = 8,4 (g)
b) \(V_{H_2}=\left(0,1+0,225\right).22,4=7,28\left(l\right)\)
Đúng 4
Bình luận (0)