Cho 8,3g hỗn hợp Fe và Al tác dụng HNO3 đặc dư đun nóg. Thu được 13,44 lít khí NO2 duy nhất. Tính % khối lượng kim loại trong hỗn hợp

Những câu hỏi liên quan
Khi cho 3,00 g hỗn hợp Cu và Al tác dụng với dung dịch HNO3 đặc dư, đun nóng, sinh ra 4,48 lít khí duy nhất NO2 (đktc). Xác định phần trăm khối lượng của mỗi kim loại trong hỗn hợp?
Gọi nAl = x (mol), nCu = y (mol); nNO2 = 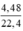 = 0,2 mol
= 0,2 mol
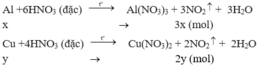
Theo pt: nNO2(1) = 3. nAl = 3.x mol
nNO2(2) = 2. nCu = 2y mol
⇒ Tổng nNO2 = 3x + 2y = 0,2 mol
Ta có hệ phương trình
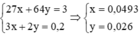
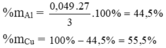
Đúng 1
Bình luận (0)
Khi cho 3 gam hỗn hợp Cu và Al tác dụng với dung dịch HNO3 đặc dư, đun nóng, sinh ra 4,48 lít khí duy nhất là NO2 (đktc). Xác định phần trăm khối lượng của mỗi kim loại trong hỗn hợp.
Gọi $n_{Cu} = a(mol) ; n_{Al} = b(mol) \Rightarrow 64a + 27b = 3(1)$
$Cu^0 \to Cu^{+2} + 2e$
$Al^0 \to Al^{+3} + 3e$
$N^{+5} + 1e \to N^{+4}$
Bảo toàn electron :
$2a + 3b = 0,2(2)$
Từ (1)(2) suy ra $a = \dfrac{3}{115} ; b = \dfrac{17}{345}$
\(\%m_{Cu}=\dfrac{\dfrac{3}{115}.64}{3}.100\%=55,65\%\\ \%m_{Al}=100\%-55,65\%=44,35\%\)
Đúng 1
Bình luận (0)
Gọi số mol của Cu và Al lần lượt là x,y (mol) (x,y>0)
\(Cu+4HNO_{3\left(đ\right)}\underrightarrow{to}Cu\left(NO_3\right)_2+2NO_2+2H_2O\\ x..................................2x\left(mol\right)\\ Al+6HNO_{3\left(đ\right)}\underrightarrow{to}Al\left(NO_3\right)_3+3NO_2+3H_2O\\ y...............................3y\left(mol\right)\)
\(\left\{{}\begin{matrix}64x+27y=3\\2x+3y=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=\dfrac{3}{115}\\y=\dfrac{17}{345}\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{\dfrac{3}{115}.64}{3}.100\approx55,652\%\\\%m_{Al}\approx44,348\%\end{matrix}\right.\\ \)
Đúng 0
Bình luận (0)
Hòa tan hết 6,95 gam hỗn hợp Al và Fe vào dung dịch HNO3 đặc, nóng (dư) thu được 10,08 lít khí NO2 duy nhất (điều kiện tiêu chuẩn). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu
\(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=6.95\left(g\right)\left(1\right)\)
\(n_{NO_2}=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
Bảo toàn e :
\(3a+3b=0.45\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.05,b=0.1\)
\(m_{Al}=0.05\cdot27=1.35\left(g\right)\)
\(m_{Fe}=0.1\cdot56=5.6\left(g\right)\)
Đúng 2
Bình luận (0)
Cho 8,3g hỗn hợp kim loại gồm Fe và Al tác dụng vừa đủ với dd H2SO4 đặc 98% nóng dư thu được 7,437 lít khí SO2(đkc) là sản phẩm khử duy nhất.Tính phần trăm theo khối lượng của từng kim loại trong hỗn hợp
Ta có: 56nFe + 27nAl = 8,3 (1)
\(n_{SO_2}=\dfrac{7,427}{24,79}=0,3\left(mol\right)\)
Theo ĐLBT e, có: 3nFe + 3nAl = 2nSO2 = 0,6 (2)
Từ (1) và (2) ⇒ nFe = nAl = 0,1 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1.56}{8,3}.100\%\approx67,47\%\\\%m_{Al}\approx32,53\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho 2,11 gam hỗn hợp Zn và Al tác dụng hết với dung dịch HNO3 đặc, nóng thu được 2,912 lít khí duy nhất NO2 (đktc). Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp đầu.
$n_{NO_2} = 0,13(mol)$
$n_{Zn} = a(mol) ; n_{Al} = b(mol)$
Ta có :
$m_{hh} = 65a + 27b = 2,11(gam)$
Bảo toàn electron : $2a + 3b = 0,13$
Suy ra a = 0,02 ; b = 0,03
$\%m_{Zn} = \dfrac{0,02.65}{2,11}.100\% = 61,61\%$
$\%m_{Al} = 100\% -61,61\% = 38,39\%$
Đúng 1
Bình luận (0)
Khi cho 14,5 gam hỗn hợp Cu và Al tác dụng với HNO3 đặc, dư, đun nóng sinh ra 24,64 lít khí NO2 ở đktc (sản phẩm khử duy nhất). Phần trăm khối lượng kim loại Cu trong hỗn hợp là (Cho H=1, N=14, O=16, Al=27, Cu=64)
Chia m gam hỗn hợp gồm 3 kim loại Mg, Al, Cu thành 2 phần bằng nhau: - Phần 1: Cho tác dụng với dung dịch HNO3 đặc, nóng dư thu được 10,528 lít khí NO2 (đktc, là sản phẩm khử duy nhất). - Phần 2: Tác dụng với Cl2 dư thu được 27,875g hỗn hợp muối clorua. Khối lượng m gam hỗn hợp kim loại là A. 22,38 gam B. 20,38 gam C. 11,19 gam D. 10,19 gam
Đọc tiếp
Chia m gam hỗn hợp gồm 3 kim loại Mg, Al, Cu thành 2 phần bằng nhau:
- Phần 1: Cho tác dụng với dung dịch HNO3 đặc, nóng dư thu được 10,528 lít khí NO2 (đktc, là sản phẩm khử duy nhất).
- Phần 2: Tác dụng với Cl2 dư thu được 27,875g hỗn hợp muối clorua.
Khối lượng m gam hỗn hợp kim loại là
A. 22,38 gam
B. 20,38 gam
C. 11,19 gam
D. 10,19 gam
Đáp án : A
P1 : ne trao đổi = nNO2 = 0,47 mol
P2 : ne trao đổi = nCl2 .2 => nCl2 pứ = 0,235 mol
=> mKL = mmuối – mCl2 pứ = 11,19g
=> m = 2.11,19 = 22,38g
Đúng 0
Bình luận (0)
Chia m gam hỗn hợp gồm 3 kim loại Mg, Al, Cu thành 2 phần bằng nhau: -Phần 1: Cho tác dụng với dung dịch HNO3 đặc nóng dư thu được 10,528 lít khí NO2 (sản phẩm khử duy nhất). -Phần 2: Tác dụng vừa đủ với Cl2 thu được 27,875 gam hỗn hợp muối clorua. Khối lượng m gam hỗn hợp kim loại là: A. 22,38 gam B. 11,19 gam C. 44,56 gam D. 5,628 gam
Đọc tiếp
Chia m gam hỗn hợp gồm 3 kim loại Mg, Al, Cu thành 2 phần bằng nhau:
-Phần 1: Cho tác dụng với dung dịch HNO3 đặc nóng dư thu được 10,528 lít khí NO2 (sản phẩm khử duy nhất).
-Phần 2: Tác dụng vừa đủ với Cl2 thu được 27,875 gam hỗn hợp muối clorua.
Khối lượng m gam hỗn hợp kim loại là:
A. 22,38 gam
B. 11,19 gam
C. 44,56 gam
D. 5,628 gam
QT cho e: Xét với ½ khối lượng hỗn hợp
Mg→ Mg2++ 2e (1)
x 2x mol
Al→ Al3++ 3e (2)
y 3y mol
Cu→ Cu2++ 2e (3)
z 2z mol
→ne cho= 2x+ 3y+2z mol
QT nhận e:
-Phần 1: nNO2=0,47 mol
N+5+ 1e→ NO2
0,47 0,47 mol
Theo ĐL bảo toàn e: ne cho= 2x+ 3y+2z = ne nhận= 0,47
-Phần 2:
Cl2+ 2e→ 2Cl-
0,47 0,47
Theo ĐL bảo toàn e: ne cho= 2x+ 3y+2z = ne nhận= 0,47
mmuối clorua= mkim loại+ mCl-= mkim loại+ 0,47.35,5=27,875 → mkim loại=11,19 gam → m= 11,19.2=22,38 gam
Đúng 0
Bình luận (0)
Hòa tan hết 12,55 gam hỗn hợp Al và Fe vào dung dịch HNO3 đặc, nóng (dư) thu được 16,8 lít khí NO2 duy nhất (điều kiện tiêu chuẩn). a/ Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu b/ Tính mol HNO3 Phản ứng
mọi người giúp em với ạ làm ra giấy rồi chụp nhé
a)
Gọi $n_{Al} = a ; n_{Fe} = b$
$\Rightarrow 27a + 56b = 12,55(1)$
$n_{NO_2} = 0,75(mol)$
Bảo toàn electron :
$3n_{Al} + 3n_{Fe} = n_{NO_2} \Rightarrow 3a + 3b = 0,75(2)$
Từ (1)(2) suy ra a = 0,05 ; b = 0,2
$m_{Al} = 0,05.27 = 1,35(gam)$
$m_{Fe} = 0,2.56 = 11,2(gam)$
b)
$n_{HNO_3} = 2n_{NO_2} = 0,75.2 = 1,5(mol)$
Đúng 3
Bình luận (0)















