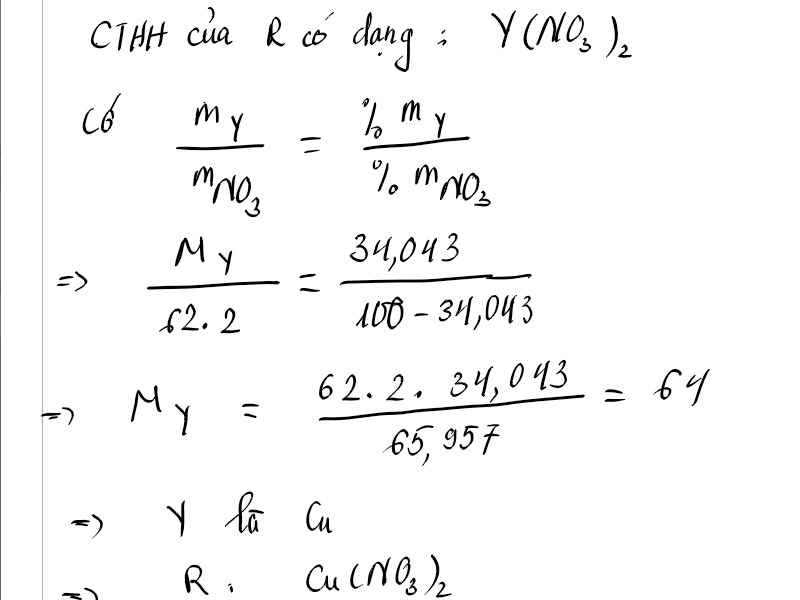Một kim loại M có hóa trị không đổi. Phần trăm khối lượng của M trong hợp chất với oxi gấp 3 lần phần trăm khối lượng của M trong muối sunfat của nó (hợp chất tạo bởi M và nhóm = SO4). Xác định kim loại M.

Những câu hỏi liên quan
1. Một hợp chất của nguyên tố R (hóa trị IV) với oxi có phần trăm khối lượng của nguyên tố R là 50%. Xác định nguyên tố R và công thức hóa học của hợp chất?2. Xác định công thức hóa học của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4? Biết rằng M chiếm 20% khối lượng của phân tử?3. Hợp chất A ở thể khí có %mC 75% và còn lại là H. Xác định CTHH của A? Biết tỉ khối của khí A với khí oxi là 0,54. Hợp chất B tạo bởi hidro và nhóm nguyên tử ( XOy) hóa trị III. Biết rằng phân tử B nặng bằng p...
Đọc tiếp
1. Một hợp chất của nguyên tố R (hóa trị IV) với oxi có phần trăm khối lượng của nguyên tố R là 50%. Xác định nguyên tố R và công thức hóa học của hợp chất?
2. Xác định công thức hóa học của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4? Biết rằng M chiếm 20% khối lượng của phân tử?
3. Hợp chất A ở thể khí có %mC = 75% và còn lại là H. Xác định CTHH của A? Biết tỉ khối của khí A với khí oxi là 0,5
4. Hợp chất B tạo bởi hidro và nhóm nguyên tử ( XOy) hóa trị III. Biết rằng phân tử B nặng bằng phân tử H2SO4 và nguyên tố oxi chiếm 65,31% về khối lượng của B.
a. Xác định chỉ số y và nguyên tử khối của nguyên tố X?
b. Cho biết tên, kí hiệu hóa học của X và công thức hóa học của B?
1. CT của hợp chất : RO2 (do R hóa trị IV)
Ta có : \(\%R=\dfrac{R}{R+16.2}.100=50\)
=> R=32
Vậy R là lưu huỳnh (S), CTHH của hợp chất : SO2
Đúng 2
Bình luận (1)
2. CTHH của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4 là MSO4 (do M hóa trị II)
Ta có : \(\%M=\dfrac{M}{M+96}.100=20\)
=>M=24
Vây M là Magie (Mg), CTHH của hợp chất MgSO4
Đúng 2
Bình luận (0)
3. Đặt CTHH của A là CxHy
\(M_A=0,5M_{O_2}=16\left(đvC\right)\)
Ta có : \(\%C=\dfrac{12x}{16}.100=75\Rightarrow x=1\)
Mặc khác : 12x + y = 16
=> y=4
Vậy CTHH của A là CH4
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
Kim loại (có hóa trị không đổi) trong muối sunfat chứa 40% về khối lượng.Không cần xác định tên kim loại, hãy tính phần trăm theo khối lượng của kim loại đó trong hợp chất với oxi.
giúp vs ạ, mk cần gấp
R là nguyên tố kim loại có hóa trị không đổi 1 hợp chất của R với nhóm cacbonat trong đó nguyên tố R chiếm 40% theo khối lượng không cần xác định nguyên tố R em Hãy tính phần trăm khối lượng của nguyên tố R trong hợp chất muối photphat
CTHH muối cacbonat: R2(CO3)n
CTHH muối photphat: R3(PO4)n
Xét R2(CO3)n
\(\%R=\dfrac{2.M_R}{2.M_R+60n}.100\%=40\%\)
=> 2.MR = 0,8.MR + 24n
=> 1,2.MR = 24n
=> \(M_R=20n\) (g/mol)
Xét R3(PO4)n
\(\%R=\dfrac{3.M_R}{3.M_R+95n}.100\%=\dfrac{3.20n}{3.20n+95n}.100\%=38,71\%\)
Đúng 2
Bình luận (0)
Cho một hợp chất được tỏa bởi kim loại A và nhóm SO4. Trong đó, phần trăm khối lượng S là 24%. Xác định kim loại A và CTHH của hợp chất đã cho.
Gọi CTHH là \(A_2\left(SO_4\right)_n\)
Ta có:
\(\%S=\dfrac{32n}{2A+96n}\cdot100\%=24\%\)
\(\Rightarrow A=\dfrac{56}{3}n\)
Nhận thấy n=3 thỏa mãn\(\Rightarrow A=56\)
Vậy A là sắt Fe.
CTHH hợp chất là \(Fe_2\left(SO_4\right)_3\)
Đúng 4
Bình luận (0)
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau: – Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn. – Phần 2: cho tác dụng với 200 ml dung...
Đọc tiếp
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau:
– Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn.
– Phần 2: cho tác dụng với 200 ml dung dịch CuSO4 1,5M. Sau khi kết thúc phản ứng tách bỏ chất rắn, cô cạn phần dung dịch thì thu được 46 gam muối khan.
a) Viết phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính phần trăm khối lượng các chất trong X.

Bảo toàn nguyên tố M: nMSO4 = 0,25mol
Bảo toàn nguyên tố Cu: nCuSO4 dư = 0,1 mol
=> M = 24 (Mg)
b.

Đúng 1
Bình luận (0)
Hợp chất A có khối lượng phân tử nặng gấp 31,5 lần khí Hidro được tạo bởi Hidro và nhóm nguyên tử XOy(hóa trị I) . Biết % khối lượng O trong A bằng 76,19. Hợp chất B tạo bởi 1 kim loại M và nhóm OH . Hợp chất C tạo bởi kim loại M và nhóm XOy có PTK là 213 . Xác định CT A , B , C
a) Hợp chất tạo bởi nguyên tố Y ( hóa trị a) và nhóm NO3 có thành phần khối lượng là 34,043% Y. Xác định khối lượng mol của Y theo a?
b) R kết hợp với nguyên tố Oxi tao hợp chất X. Tính phần trăm khối lượng nguyên tố R trong X ?
Đ
ặ
t
:
Y
(
N
O
3
)
2
V
ì
:
%
m
Y
=
34
,
043
%
⇔
M
Y
M
Y
+
124
=
34
,
043
%
⇔
M
Y
=
64
(
g
m
o
l
)
⇒
Y
:
Đ
ồ
n
g
(
C
u
=
64
)
⇒
C
T
H
H
:
C
u
(
N
O
3
)
2
Thu gọn
Đúng 0
Bình luận (0)
Nguyên tố kim loại A liên kết với nhóm hiđroxit tạo thành hai hợp chất. Phần trăm khối lượng của A trong các hợp chất trên là 50,485% và 60,465%. Xác định công thức hóa học của 2 hợp chất đó.
Gọi công thức hóa học của hai hợp chất lần lượt là Ax(OH)y và Ax(OH)z.
Theo thông tin cho, phần trăm khối lượng của A trong hợp chất Ax(OH)y là 50,485%. Điều này có nghĩa là 50,485g trong 100g của hợp chất đó là nguyên tố A.
Tương tự, phần trăm khối lượng của A trong hợp chất Ax(OH)z là 60,465%. Điều này có nghĩa là 60,465g trong 100g của hợp chất đó là nguyên tố A.
Với các thông tin này, ta có thể sử dụng phương pháp tính toán hóa học để xác định giá trị của x, y và z.
Đầu tiên, ta tính tỉ lệ giữa A và OH trong từng hợp chất:
Trong hợp chất Ax(OH)y, tỉ lệ A:OH là 50,485 : (100 - 50,485) = 50,485 : 49,515 (gọi là tỷ số 1)Trong hợp chất Ax(OH)z, tỉ lệ A:OH là 60,465 : (100 - 60,465) = 60,465 : 39,535 (gọi là tỷ số 2)Tiếp theo, ta xác định tỉ lệ giữa x, y và z bằng cách so sánh tỷ số 1 và tỷ số 2:
Tỷ số A:OH trong Ax(OH)y là 50,485 : 49,515 = 1,02Tỷ số A:OH trong Ax(OH)z là 60,465 : 39,535 = 1,53Do đó, ta có thể suy ra rằng tỷ số x:y trong công thức hóa học của hai hợp chất là 1,02:1,53, hoặc tương đương với 2:3.
Vậy, công thức hóa học của hai hợp chất là A2(OH)3 và A3(OH)2.
Đúng 0
Bình luận (0)
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nướ...
Đọc tiếp
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nước ở điều kiện thường ,muối clorua của M tan hoàn toàn trong nước,kim loại M hoạt động hóa học hơn Cu.
a)Viết các pthh và xác định kim loại M
b)Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp Q