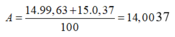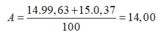nitơ trong tự nhiên có hai đồng vị \(^{_{7^{ }}14}N\left(99,63\%\right)\) và \(^{_715}N\)(0,37%) . tính số nguyên tử của \(^{14}N\) trong 1,700074 g NaNO\(_3\)

Những câu hỏi liên quan
Nito trong thiên nhiên là hỗn hợp của hai đồng vị gồm:14/7 N (99,63%) và 15/7N(0,37%). Nguyên tử khối trung bình của nitơ là?
\(\overline{NTK}_N=\dfrac{99,63\%.14+0,37\%.15}{100\%}=14,0037\left(đ.v.C\right)\)
Đúng 1
Bình luận (0)
Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị có % về số nguyên tử tương ứng là 147N (99,63%) và 157N(0,37%). Nguyên tử khối trung bình của Nitơ là:
A. 14,7
B. 14,0
C. 14,4
D. 13,7
Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị có % về số nguyên tử tương ứng là N 7 14 (99,63%) và N 7 15 (0,37%). Nguyên tử khối trung bình của nitơ là
A. 14,7.
B. 14,0.
C. 14,4.
D. 13,7.
Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị có % về số nguyên tử tương ứng là N 7 14 (99,63%) và N 7 15 (0,37%). Nguyên tử khối trung bình của nitơ là
A. 14,7.
B. 14,0.
C. 14,4.
D. 13,7.
Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị là 147N (99,63%) và A7N (0,37%). Trong HNO3 14N chiếm 22,1387% khối lượng. Nguyên tử khối của đồng vị thứ hai của Nitơ là: A. 14. B. 15. C. 16. D. 13.
Đọc tiếp
Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị là 147N (99,63%) và A7N (0,37%). Trong HNO3 14N chiếm 22,1387% khối lượng. Nguyên tử khối của đồng vị thứ hai của Nitơ là:
A. 14.
B. 15.
C. 16.
D. 13.
Đáp án B
MN = 14 x 0,9963 + A x 0,0037
= 13,9482 + 0,0037A.
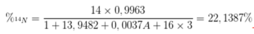
→ A = 15
Đúng 0
Bình luận (0)
Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị là
N
7
14
(99,63%) và
N
7
15
(0,37%). Nguyên tử khối trung bình của nitơ là A. 14,7. B. 14,0. C. 14.4 D. 13,7.
Đọc tiếp
Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị là N 7 14 (99,63%) và N 7 15 (0,37%). Nguyên tử khối trung bình của nitơ là
A. 14,7.
B. 14,0.
C. 14.4
D. 13,7.
Đáp án B
Nguyên tử khối trung bình của nguyên tố Nito là
M N = ( 12 . 98 , 89 + 13 . 1 , 11 ) / 100 = 14 , 0037
Đúng 0
Bình luận (0)
Câu 1: (3,0 điểm). Cho nguyên tử Nitơ (Z = 7).
a) Xác định số proton và số electron của nguyên tử.
b) Xác định sự phân bố electron trên các lớp electron.
c) Nguyên tố Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị là 14N7 (99,63%) và 15N7 (0,37%). Tính nguyên tử khối trung bình của Nitơ.
Nguyên tố nitrogen có hai đồng vị tự nhiên là \(\dfrac{14}{7}\)N và \(\dfrac{15}{7}\)N ,số loại phân tử N2 tồn tại bên trong khí quyển trái đất là? Giải thích?
Số loại phân tử N2: 3
CTHH của các phân tử N2: \(^{14}_7N^{14}_7N\), \(^{15}_7N^{15}_7N\) và \(^{14}_7N^{15}_7N\)
Đúng 2
Bình luận (0)
Nguyên tố đồng có hai đồng vị bền và . Biết nguyên tử khối trung bình của đồng là 63,54. Tính phần trăm hàm lượng của đồng vị 63Cu trong Cu(NO3)2 (cho O=16, N=14).
Xem chi tiết
Gọi :
Phần trăm số nguyên tử của đồng vị 63Cu là a
Phần trăm số nguyên tử của đồng vị 65Cu là b
Ta có :
\(a + b = 100\%\\ 63.a\% + 65.b\% = 63,54\)
Suy ra : a = 73% ; b = 27%
\(\)Phần trăm khối lượng của 63Cu trong Cu(NO3)2 là :
\(\dfrac{63.73\%}{63,54+ 14.2 + 16.6}.100\% = 24,52\%\)
Đúng 2
Bình luận (0)