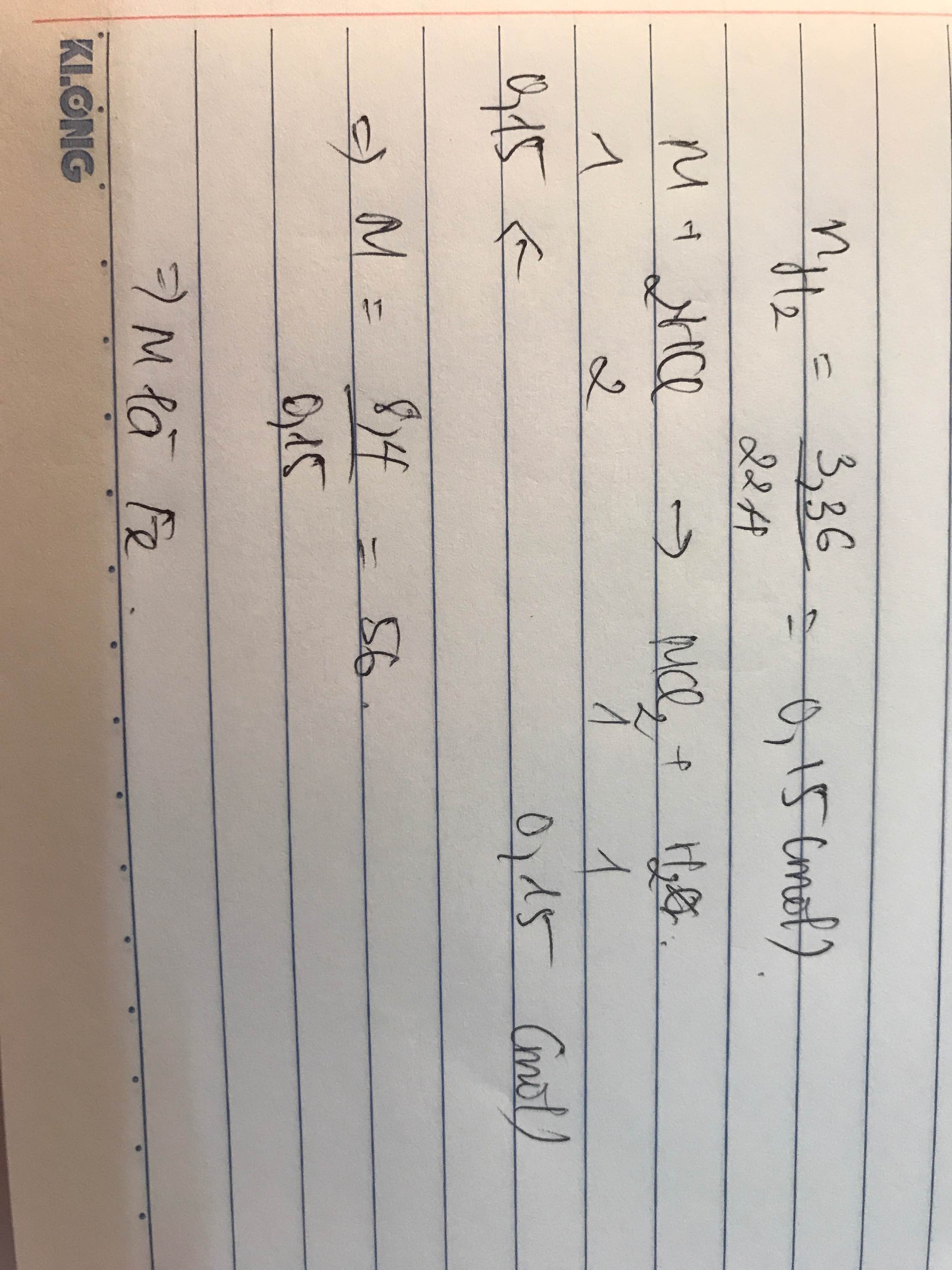hòa tan hết 5,52 g kim loại M nhóm 1A trong 109,5g dd HCl 10%.Sau phản ứng thu được 114,78g dung dịch X và khí H2.Xác định M và nồng độ % dung dịch X

Những câu hỏi liên quan
Hòa tan hoàn toàn 2,3 g một kim loại nhóm 1A vào 57,8 g nước thu được 1,12 lít khí h2 và dung dịch a
a. xác định tên kim loại
b .tính nồng độ phần trăm chất tan trong dung dịch a
a)Gọi A là kim loại cần tìm.
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05mol\)
Ta có PTHH:
\(2A+2H_2O\rightarrow2AOH+H_2\uparrow\)
0,1-----------------0,1--------0,05-----(mol);
Vậy \(M_A=\dfrac{2,3}{0,1}=23\)(g/mol) => A là Na
b) Ta có: \(m_{dd}=2,3+57,8-0,05\cdot2=60g\)
Từ đó suy ra:\(\%C_{NaOH}=\dfrac{0,1\cdot40}{60}\cdot100\%=6,67\%\)
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 7,8 gam kim loại kiềm trong dung dịch hcl 10% sau phản ứng thu được dung dịch x và 2,24 lít khí
a .xác định tên của kim loại trên
b. tìm nồng độ phần trăm của các chất trong dung dịch sau phản ứng biết HCl dùng dư 20% so với lượng phản ứng
Xem chi tiết
Gọi kim loại cần tìm là A
a) PTHH: \(A+H_2O\rightarrow AOH+\dfrac{1}{2}H_2\uparrow\)
\(AOH+HCl\rightarrow ACl+H_2O\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) \(\Rightarrow n_A=0,2mol\)
\(\Rightarrow M_A=\dfrac{7,8}{0,2}=39\) \(\Rightarrow\) Kim loại cần tìm là Kali
b) Ta có: \(\left\{{}\begin{matrix}n_{KCl}=0,2mol\\n_{HCl\left(pư\right)}=0,2mol\Rightarrow n_{HCl\left(dư\right)}=0,2\cdot20\%=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{KCl}=0,2\cdot74,5=14,9\left(g\right)\\m_{HCl\left(dư\right)}=0,04\cdot36,5=1,46\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{H_2}=2\cdot0,1=0,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_K+m_{ddHCl}-m_{H_2}=7,8+\dfrac{0,24\cdot36,5}{10\%}-0,2=95,2\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{KCl}=\dfrac{14,9}{95,2}\cdot100\%\approx15,65\%\\C\%_{HCl\left(dư\right)}=\dfrac{1,46}{95,2}\cdot100\%\approx1,53\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Hòa tan hết 8,4gam kim loại M vào 80gam dung dịch H2SO4 19,6% sau phản ứng thu được dung dịch X và 3,36 lít khí H2 (đktc)
a) Xác định kim loại M
b) Tính C% của chất tan có trong dung dịch X
a)
\(n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ n_{H_2SO_4} = \dfrac{80.19,6\%}{98} = 0,16(mol)\)
Gọi n là hóa trị của kim loại M
\(2M + nH_2SO_4 \to M_2(SO_4)_n + nH_2\)
Theo PTHH :
\(n_M = \dfrac{2}{n}n_{H_2} = \dfrac{0,3}{n}(mol)\\ n_{H_2SO_4\ phản\ ứng} = n_{H_2} = 0,15(mol)\\ \Rightarrow n_{H_2SO_4\ dư} = 0,16-0,15 = 0,01(mol)\)
Ta có : \(M = \dfrac{8,4}{\dfrac{0,3}{n}} = 28n\)
Với n = 2 thì M = 56(Fe)
b)
Sau phản ứng, mdung dịch = 8,4 + 80 - 0,15.2 = 88,1(gam)
\(n_{FeSO_4} = n_{H_2} = 0,15(mol)\)
Vậy :
\(C\%_{FeSO_4} = \dfrac{0,15.152}{88,1}.100\% = 25,88\%\\ C\%_{H_2SO_4} = \dfrac{0,01.98}{88,1}.100\% = 1,11\%\)
Đúng 0
Bình luận (0)
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
Cho 4,8 gam kim loại M vào 50 gam dung dịch HCl nồng độ 36,5 % , phản ứng xong thu được 4,48 lít khí H2 , ( ở đktc ) và dung dịch X. Xác định kim loại M và tính nồng độ phần trăm các chất trong X.
PTHH: \(2M+2xHCl\rightarrow2MCl_x+xH_2\uparrow\) (x là hóa trị của M)
Tính theo sản phẩm
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow n_M=\dfrac{0,4}{x}\left(mol\right)\) \(\Rightarrow M=\dfrac{4,8}{\dfrac{0,4}{x}}=12x\)
Ta thấy với \(x=2\) thì \(M=24\) (Magie)
Mặt khác: \(n_{HCl}=\dfrac{50\cdot36,5\%}{36,5}=0,5\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\\n_{HCl\left(dư\right)}=0,1\left(mol\right)\end{matrix}\right.\)
Ta lại có: \(m_{dd\left(sau.p/ứ\right)}=m_{Mg}+m_{ddHCl}-m_{H_2}=4,8+50-0,2\cdot2=54,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,2\cdot95}{54,4}\cdot100\%\approx34,93\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,1\cdot36,5}{54,4}\cdot100\%\approx6,71\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hòa tan hết 2,8 gam kim loại Fe vào cốc đựng 60 gam dung dịch HCl 7,3% thu được khí
H
2
và dung dịch X. Nồng độ phần trăm của muối sắt (II) clorua trong dung dịch sau phản ứng là A. 9,11%. B. 10,03%. C. 10,13%. D. 12,13%.
Đọc tiếp
Hòa tan hết 2,8 gam kim loại Fe vào cốc đựng 60 gam dung dịch HCl 7,3% thu được khí H 2 và dung dịch X. Nồng độ phần trăm của muối sắt (II) clorua trong dung dịch sau phản ứng là
A. 9,11%.
B. 10,03%.
C. 10,13%.
D. 12,13%.
hòa tan vừa hết 4 8 gam kim loại r(hoad trị 2) cần phải dùng m gam dung dịch hcl 7,3%.sau phản ứng thử được 4,48 lít khí h2(ở dktc).tìm tên kim loại r và nồng độ phần trăm muối trong dd thu được.
Hòa tan hết 3,6 gam một kim loại M (có hóa trị II) trong dung dịch HCl dư, sau phản ứng thu được dung dịch X và V lít khí H2 (đktc). Cô cạn dung dịch X thu được 14,25 gam muối khan.
a. Tìm V và kim loại M.
b. Dẫn toàn bộ khí H2 thu được qua ống thủy tinh chứa 16 gam CuO nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được a gam chất rắn. Tính a.
Xem chi tiết
a) Ta có \(m_{muôi}=m_{KL}+m_{Cl^-}\\ \Leftrightarrow m_{Cl^-}=m_{muôi}-m_{KL}=14,25-3,6=10,65g\\ \Rightarrow n_{Cl^-}=\dfrac{10,65}{35,5}=0,3mol\)
Theo bảo toàn nguyên tố Cl: \(n_{HCl}=n_{Cl^-}=0,3mol\)
Theo bảo toàn nguyên tố H: \(n_{H_2}=\dfrac{1}{2}\cdot n_{HCl}=\dfrac{1}{2}\cdot0,3=0,15mol\\ \Rightarrow V=0,15\cdot22,4=3,36l\)
Ta có PTHH: \(M+2HCl\rightarrow MCl_2+H_2\uparrow\)
----------------0,15-------------------------0,15---(mol)
\(\Rightarrow M=\dfrac{3,6}{0,15}=24\)(g/mol) => M là Magie (Mg)
b) \(n_{CuO}=\dfrac{16}{80}=0,2mol\)
Ta có quá trình phản ứng:
\(CuO+H_2\rightarrow Cu+H_2O\)
-0,15---0,15-----0,15----------(mol)
\(\Rightarrow a=m_{CuO\left(dư\right)}+m_{Cu}=\left(16-0,15\cdot80\right)+64\cdot0,15=13,6g\)
Đúng 1
Bình luận (0)
Hòa tan hết 11,2 gam kim loại M hóa trị II trong 500 ml dung dịch H2SO4 1M thu được dung dịch A và 4,48 lít H2 (đktc). a/ Xác định M. Fe b/ Tính nồng độ mol của các chất tan trong dung dịch A. 0,6 + 0,4 c/ Làm lạnh dung dịch sau phản ứng A thu được bao nhiêu gam MSO4.7H2O?
a, Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(M+H_2SO_4\rightarrow MSO_4+H_2\)
Theo PT: \(n_M=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{11,2}{0,2}=56\left(g/mol\right)\)
→ M là Fe.
b, Theo PT: \(n_{FeSO_4}=n_{H_2SO_4\left(pư\right)}=n_{H_2}=0,2\left(mol\right)\)
⇒ nH2SO4 dư = 0,5.1 - 0,2 = 0,3 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,3}{0,5}=0,6\left(M\right)\\C_{M_{FeSO_4}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\end{matrix}\right.\)
c, Ta có: \(n_{FeSO_4.7H_2O}=n_{FeSO_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{FeSO_4.7H_2O}=0,2.278=55,6\left(g\right)\)
Đúng 1
Bình luận (0)