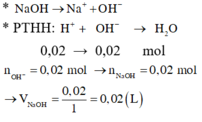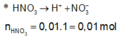Cho 10ml dung dịch hỗn hợp 2 axit HCl 2M và H2SO4 1M Để trung hòa hoàn toàn 10ml dung dịch 2 axit đó cần dùng vừa đủ bao nhiêu ml dung dịch NaOH 0,5M

Những câu hỏi liên quan
1/ Cho 10ml dung dịch hỗn hợp 2 axit HCl 2M và H2SO4 1M. Để trung hòa hoàn toàn 10ml dung dịch 2 axit đó cần dùng vừa đủ bao nhiêu ml dd NaOH 0,5M?2/ Cho 23,676 gam hh 3 kim loại Mg,Al,Cu tác dụng hết với O2, thu được 34,14g hh gồm 3 oxit. Hỏi để hòa tan hết lượng hỗn hợp oxit đó cần ít nhất bao nhiêu ml dd hh 2 axit HCl 3M và H2SO4 1,5MCác bạn giải hộ mình bài này theo cách lớp 9 với ạ!!! Mình cảm ơn trc nha!!!
Đọc tiếp
1/ Cho 10ml dung dịch hỗn hợp 2 axit HCl 2M và H2SO4 1M. Để trung hòa hoàn toàn 10ml dung dịch 2 axit đó cần dùng vừa đủ bao nhiêu ml dd NaOH 0,5M?
2/ Cho 23,676 gam hh 3 kim loại Mg,Al,Cu tác dụng hết với O2, thu được 34,14g hh gồm 3 oxit. Hỏi để hòa tan hết lượng hỗn hợp oxit đó cần ít nhất bao nhiêu ml dd hh 2 axit HCl 3M và H2SO4 1,5M
Các bạn giải hộ mình bài này theo cách lớp 9 với ạ!!! Mình cảm ơn trc nha!!!![]()
Bài 1 nHCl=10/1000.2=0,02 mol
nH2SO4=10/1000=0,01 mol
HCl + NaOH =>NaCl + H2O
0,02 mol=>0,02 mol
H2SO4 +2NaOH =>Na2SO4 +2H2O
0,01 mol=>0,02 mol
Tổng nNaOH=0,04 mol
=>V dd NaOH=0,04/0,5=0,08 lit=80ml
Đúng 0
Bình luận (0)
Bảo toàn khối lượng mO2=34,14-23,676=10,464g
=>nO2=0,327 mol
2Al +3/2 O2 =>Al2O3
Nếu viết pt oxit cộng dd axit pt rút gọn là
Al2O3 + 6H+ =>2Al3+ +3 H2O
Tương tự với các kim loại Cu,Mg em viết pthh ra sẽ đều thấy nH+=4nO2 pứ
=>nH+=4.0,327=1,308 mol
GS có V lit dd axit
=>nHCl=3V mol và nH2SO4=1,5V mol
1 mol H2SO4 thủy phân ra 2 mol H+
Tổng nH+ trong H2SO4 và HCl bằng 3V+1,5V.2=6V
=>V=1,308/6=0,218 lit=218ml
Đúng 0
Bình luận (2)
Cho 10ml dung dịch hỗn hợp 2 axit HCl 2M và H2SO4 1M Để trung hòa hoàn toàn 10ml dung dịch 2 axit đó cần dùng vừa đủ bao nhiêu ml dung dịch NaOH 0,5M
Help meeeeee!!!!
\(PTHH:NaOH+HCl\rightarrow NaCl+H2O\)
\(2NaOH+H2SO4\rightarrow Na2SO4+H2O\)
Ta có : \(n_{HCL}=0,02\left(mol\right)\)
\(\Rightarrow n_{NaOH}=0,04\left(mol\right)\)
\(\Rightarrow V_{dd_{NaOH}}=\frac{0,04}{0,5}=0,08l=80ml\)
Đúng 0
Bình luận (0)
NaOH +HCl---.NaCl +H2O(1)
2NaOH +H2SO4----,Na2SO4+H2O(2)
n\(_{HCl}=0,01.2=0,02\left(mol\right)\)
n\(_{H2SO4}=0,01.1=0,01\left(mol\right)\)
Theo pthh1
n\(_{NaOH}=n_{HCl}=0,02\left(mol\right)\)
Theo pthh2
n\(_{NaOH}=2n_{H2SO4}=0,02\left(mol\right)\)
\(\Sigma n_{NaOH}=0,02+0,02=0,04\left(mol\right)\)
V\(_{NaOH}=\frac{0,04}{0,5}=0,08\left(l\right)=80ml\)
Đúng 0
Bình luận (0)
Để trung hòa 10ml dung dịch hỗn hợp axit gồm H2SO4 và HCl cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100ml dung dịch hỗn hợp axit trên đem trung hòa với một lượng dung dịch NaOH vừa đủ rồi cô cạn thì thu được 24,65g muối khan. Tính nồng độ mol/L của mỗi axit
Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và
H
2
S
O
4
cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là A. 0,8M và 0,6M B. 1M và 0,5M C. 0,6M và 0,7M D. 0,2M và 0,9M
Đọc tiếp
Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và H 2 S O 4 cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là
A. 0,8M và 0,6M
B. 1M và 0,5M
C. 0,6M và 0,7M
D. 0,2M và 0,9M
Chọn A
Gọi nồng độ mol ban đầu của HCl và H 2 S O 4 lần lượt là x và y (M)


Đúng 0
Bình luận (0)
Cần bao nhiêu lít dung dịch NaOH 0,5M để trung hoà 400 ml hỗn hợp dung dịch axit gồm
H
2
S
O
4
0,5M và HCl 1M? A. 1,5 lít B. 0,5 lít C. 1,6 lít D. 1,0 lít
Đọc tiếp
Cần bao nhiêu lít dung dịch NaOH 0,5M để trung hoà 400 ml hỗn hợp dung dịch axit gồm H 2 S O 4 0,5M và HCl 1M?
A. 1,5 lít
B. 0,5 lít
C. 1,6 lít
D. 1,0 lít
trung hòa 10ml hỗn hợp dung dịch x gồm hcl và chcooh cần 3ml dung dịch koh 1M. cô sản phẩm thu được 0,235g muối khan. mặt khác, để trung hòa lượng axi trên cần v ml hỗn hợp dung dịch ba(oh)2 0,02M và naoh 0,01M: a) tính nồng độ mol của các axit trong hỗn hợp b) tinh v
nhớ ghi đầy đủ cách giả ra giấy , chụp và gửi
a, PT: \(HCl+KOH\rightarrow KCl+H_2O\)
\(CH_3COOH+KOH\rightarrow CH_3COOK+H_2O\)
Gọi: \(\left\{{}\begin{matrix}n_{HCl}=x\left(mol\right)\\n_{CH_3COOH}=y\left(mol\right)\end{matrix}\right.\)
Theo PT: \(n_{KOH}=n_{HCl}+n_{CH_3COOH}=x+y=0,003.1=0,003\left(mol\right)\left(1\right)\)
\(\left\{{}\begin{matrix}n_{KCl}=n_{HCl}=x\left(mol\right)\\n_{CH_3COOK}=n_{CH_3COOH}=y\left(mol\right)\end{matrix}\right.\) ⇒ 74,5x + 98y = 0,235 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x\approx0,0025\left(mol\right)\\y\approx0,0005\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{0,0025}{0,01}=0,25\left(M\right)\\C_{M_{CH_3COOH}}=\dfrac{0,0005}{0,01}=0,05\left(M\right)\end{matrix}\right.\)
b, Ta có: \(n_{H^+}=n_{HCl}+n_{CH_3COOH}=0,003\left(mol\right)\)
\(n_{OH^-}=2n_{Ba\left(OH\right)_2}+n_{NaOH}=2.\dfrac{V}{1000}.0,02+\dfrac{V}{1000}.0,01\left(mol\right)\)
PT: \(H^++OH^-\rightarrow H_2O\)
Theo PT: \(n_{H^+}=n_{OH^-}\)
\(\Rightarrow0,003=2.\dfrac{V}{1000}.0,02+\dfrac{V}{1000}.0,01\) \(\Rightarrow V=60\left(ml\right)\)
Đúng 2
Bình luận (0)
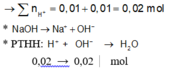
Cho 10 mL dung dịch hỗn hợp HNO3 1M và H2SO4 0,5M. Thể tích dung dịch NaOH 1M cần để trung hòa dung dịch axit trên là
A. 0,02 lít.
B. 0,01 lít.
C. 0,05 lít.
D. 0,04 lít.
Cho 10 mL dung dịch hỗn hợp HNO3 1M và H2SO4 0,5M. Thể tích dung dịch NaOH 1M cần để trung hòa dung dịch axit trên là
A. 0,02 lít.
B. 0,01 lít.
C. 0,05 lít.
D. 0,04 lít.
Trung hòa V ml dung dịch NaOH 2M cần dùng 50 ml dung dịch H2SO4 1M. Viết phương trình phản
ứng và tính V ? (trung hòa là phản ứng vừa đủ giữa axit và bazo)
\(n_{H_2SO_4}=1.0,05=0,05(mol)\\ PTHH:2NaOH+H_2SO_4\to Na_2SO_4+2H_2O\\ \Rightarrow n_{NaOH}=2n_{H_2SO_4}=0,1(mol)\\ \Rightarrow V_{dd_{NaOH}}=\dfrac{0,1}{2}=0,05(l)\)
Đúng 0
Bình luận (0)