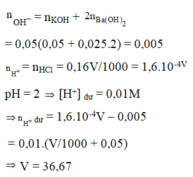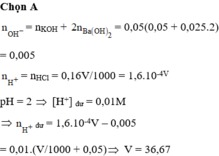cần thêm bao nhiêu ml dung dịch Ba(OH)2 có pH =12 vào 400ml dung dịch KOH 1,5.10-5 M để thu được dung dịch có pH =11

Những câu hỏi liên quan
Cho e hỏi: Cần thêm bai nhiêu ml Ba(OH)2 có pH=12 vào 400ml dung dịch KOH 1,5×10^5 M để thu được dung dịch có pH=11
Cần thêm bao nhiêu ml dung dịch NaOH có pH 13 vào 300ml dung dịch Ca(OH)2 0,0015M để thu được dung dịch có pH 12? A. 7/500 lít B. 7/300 lít C. 7/100 lít D. 7/200 lít
Đọc tiếp
Cần thêm bao nhiêu ml dung dịch NaOH có pH =13 vào 300ml dung dịch Ca(OH)2 0,0015M để thu được dung dịch có pH =12?
A. 7/500 lít
B. 7/300 lít
C. 7/100 lít
D. 7/200 lít
Đáp án B
Gọi thể tích dung dịch NaOH cần thêm là V lít
nOH- = V.10-1+ 0,3.0,0015.2 (mol)
[OH-] = nOH-/ Vdd = ( V.10-1+ 0,3.0,0015.2)/ (V+ 0,3) = 10-2
Giải ra V = 7/300 lít
Đúng 0
Bình luận (0)
Cho m(g) Ba vào H2O thu được 200ml dung dịch X có pH=12.Cần thêm vào 100ml dung dịch X bao nhiêu ml dung dịch H2SO4 0,6M để thu được dung dịch sau phản ứng có pH=1
pH=12=>pOH=2 =>nOH- = 10-2*0,2=2*10-3 mol
OH- + H+ => H2O
0,002 0,002
sau pư, pH=1 => số mol H+ dư = 10-1*(0,2+0,1)=0,03mol
vậy tổng số mol H+ thêm vào= 0,03+0,002=0,032mol => nH2SO4=0,032/2=0,016mol
=>Vdd=0,016/0,6=0,0267l =26,7ml
Đúng 0
Bình luận (0)
Cần thêm bao nhiêu ml dung dịch HCl 0,15M vào 100ml dung dịch hỗn hợp gồm hai bazo NaOH 0,1M + Ba(OH)2 0,075M để thu được dung dịch có pH2? A. 13/70 lít B. 15/70 lít C. 0,65 lít D. 1 lít
Đọc tiếp
Cần thêm bao nhiêu ml dung dịch HCl 0,15M vào 100ml dung dịch hỗn hợp gồm hai bazo NaOH 0,1M + Ba(OH)2 0,075M để thu được dung dịch có pH=2?
A. 13/70 lít
B. 15/70 lít
C. 0,65 lít
D. 1 lít
Đáp án A
nHCl = 0,15V mol = nH+
nOH-= 0,1.0,1+ 0,075.2.0,1 = 0,025 mol
Dung dịch thu được sau phản ứng có pH = 2 nên axit dư
H+ + OH- → H2O
0,025 0,025mol
nH+ dư = 0,15V- 0,025 mol
[H+] dư = nH+ dư/ Vdd = (0,15V- 0,025)/(V+0,1) = 10-2 suy ra V = 13/70 lít
Đúng 0
Bình luận (0)
Phải thêm bao nhiêu ml dung dịch Ba(OH)2.0,05M vào 9ml nước để được dung dịch có pH =12?
\(pH=12\)
\(\Rightarrow\left[H^+\right]=10^{-12}\)
\(\Rightarrow\left[OH^-\right]=10^{-2}\)
Ta có: \(n_{OH^-}=2.0,05.V=\left(V+0,009\right).0,01\)
\(\Rightarrow V=0,001\left(ml\right)=1\left(l\right)\)
Đúng 0
Bình luận (0)
Câu1 Trộn 100 ml dung dịch chứa HCl 0,1M và H2SO4 0,05M với 150 ml dung dịch Ba(OH)2 có nồng độ 0,15 M thu được 250 ml dung dịch có pH= x và m gam kết tủa. Giá trị của x và m là Câu2 Cho 10ml dung dịch HNO3 có pH=4. Cần thêm bao nhiêu ml nước cất để thu được dung dịch có pH=6?A. 990 ml. Câu3 Một dung dịch chứa 0,01 mol Na+; 0,02 mol SO42-; 0,01 mol Cl- và x mol Cu2+. Giá trị của x là
Có 50 ml dung dịch chứa hỗn hợp KOH 0,05M và Ba(OH)2 0,025M. Người ta thêm V ml dung dịch HCl 0,16M vào 50 ml dung dịch trên thu được dung dịch có pH 2. Giá trị của V là: A. 36,67. B. 30,33. C. 40,45. D. 45,67.
Đọc tiếp
Có 50 ml dung dịch chứa hỗn hợp KOH 0,05M và Ba(OH)2 0,025M. Người ta thêm V ml dung dịch HCl 0,16M vào 50 ml dung dịch trên thu được dung dịch có pH = 2. Giá trị của V là:
A. 36,67.
B. 30,33.
C. 40,45.
D. 45,67.
Có 50 ml dung dịch chứa hỗn hợp KOH 0,05M và Ba(OH)2 0,025M. Người ta thêm V ml dung dịch HCl 0,16M vào 50 ml dung dịch trên thu được dung dịch có pH 2. Giá trị của V là A. 36,67 B. 30,33. C. 40,45 D. 45,67.
Đọc tiếp
Có 50 ml dung dịch chứa hỗn hợp KOH 0,05M và Ba(OH)2 0,025M. Người ta thêm V ml dung dịch HCl 0,16M vào 50 ml dung dịch trên thu được dung dịch có pH = 2. Giá trị của V là
A. 36,67
B. 30,33.
C. 40,45
D. 45,67.
Có 50 ml dung dịch chứa hỗn hợp KOH 0,05M và Ba(OH)2 0,025M người ta thêm V ml dung dịch HCl 0,16M vào 50 ml dung dịch trên thu được dung dịch mới có pH = 2. Vậy giá trị của V là
A. 40,45 ml.
B. 45,67 ml.
C. 30,33 ml.
D. 36,67 ml.
Đáp án : D
nOH = nKOH + 2nBa(OH)2 = 0,005 mol
nH+ = nHCl = 0,16V.10-3 mol
=> [H+] = 10-pH
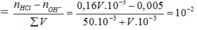
=> V = 36,67 ml
Đúng 0
Bình luận (0)