cần bao nhiêu gam HCL để pha chế 400ml dung dịch có pH=2

Những câu hỏi liên quan
Cần bao nhiêu gam HCl để pha chế 400 ml dung dịch có pH=2?
A. 0,146 gam
B. 0,292 gam
C. 0,438 gam
D. 0,219 gam
Đáp án A
nHCl= nH+= 0,4.10-2 (mol), mHCl= 0,146 gam
Đúng 0
Bình luận (0)
Câu 1. Có 2 dung dịch HCl có nồng độ 2M và 12M tính thể tích dung dịch cần lấy để pha chế được 400ml dung dịch HCl có nồng độ 10M
Câu 2. Trộn 600ml dung dịch KOH 2M và 400ml dung dịch KOH 3M. Hãy tính nồng độ mol của dung dịch này
Cần bao nhiêu gam NaOH để pha chế 250 ml dung dịch có pH = 10 ?
Khi pH = 10 thì [H+] = 1.10-10M và
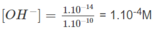
nghĩa là cần có 1. 10 - 4 mol NaOH trong 1 lít dung dịch.
Vậy trong 250 ml (0,25 lít) dung dịch cần có 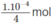 NaOH hoà tan, nghĩa là cần có
NaOH hoà tan, nghĩa là cần có
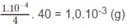 NaOH
NaOH
Đúng 0
Bình luận (0)
Cần bao nhiêu gam NaOH để pha chế 300,0 ml dung dịch có pH = 10,0?
\(pH=14+log\left[OH^-\right]=10\)
\(\Rightarrow\left[OH^-\right]=10^{-4}\)
\(n_{NaOH}=10^{-4}\cdot0.3=3\cdot10^{-5}\left(mol\right)\)
\(m_{NaOH}=3\cdot10^{-5}\cdot40=1.2\cdot10^{-3}\left(g\right)\)
Đúng 2
Bình luận (0)
\([H^+] = 10^{-pH} = 10^{-10} M\\ \Rightarrow C_{M_{NaOH}} = [OH^-] = \dfrac{10^{-14}}{10^{-10}}= 10^{-4}M\\ \Rightarrow n_{NaOH} = 10^{-4}.0,3 = 3.10^{-5}(mol)\\ m_{NaOH} = 3.10^{-5}.40 = 1,2.10^{-3}(gam)\)
Đúng 2
Bình luận (0)
1 Pha loãng dung dịch HCl có pH = 3 bao nhiêu lần để được dung dịch mới có pH = 4 ?
2 Pha loãng dung dịch 1 lít NaOH có pH = 9 bằng nước để được dung dịch mới có pH = 8. Thể tích nước cần dùng là?
Câu 1 :
Gọi thể tích dung dịch ban đầu là V(lít)
$[H^+] = 10^{-3}V(mol)$
Thể tích dung dịch lúc sau là :
$V' = \dfrac{10^{-3}.V}{10^{-4}} = 10V$
Do đó cần pha loãng dung dịch ban đầu 10 lần thì thu được dung dịch trên
Đúng 4
Bình luận (0)
Câu 2 :
$[OH^-] = 10^{-14} : 10^{-9} = 10^{-5}M$
$n_{OH^-} = 10^{-5}.1 = 10^{-5}(mol)$
Sau khi pha :
$[OH^-] = 10^{-14} : 10^{-8} = 10^{-6}M$
$V_{dd} = \dfrac{10^{-5}}{10^{-6}} = 0,1(lít) = 100(ml)$
$V_{nước\ cần\ dùng} = 1000 - 100 = 900(ml)$
Đúng 4
Bình luận (0)
Dung dịch HCl có pH = 3. Cần pha loãng dung dịch axit này (bằng nước) bao nhiêu lần để thu được dung dịch HCl có pH = 4?
A. 9
B. 10
C. 99
D. 100
Dung dịch HCl có pH = 3. Cần pha loãng dung dịch axit này (bằng nước) bao nhiêu lần để thu được dung dịch HCl có pH = 4?
A. 9.
B. 10.
C. 99.
D. 100.
Gọi V, V’ lần lượt là thể tích dung dịch HCl có pH = 3, pH = 4
Do pH = 3 → [H+] = 10-3M → nH+trước khi pha loãng = 10-3V
pH = 4 → [H+] = 10-4M → nH+sau khi pha loãng = 10-4V’
Ta có nH+trước khi pha loãng = nH+sau khi pha loãng → 10-3V = 10-4V’
V ' V = 10 - 3 10 - 4 = 10
Vậy cần pha loãng axit 10 lần
Đáp án B
Đúng 0
Bình luận (0)
Dung dịch HCl có pH 3. Cần pha loãng dung dịch axit này (bằng H2O) bao nhiêu lần để thu được dung dịch HCl có pH 4? A. 5 lần. B. 8 lần. C. 9 lần. D. 10 lần.
Đọc tiếp
Dung dịch HCl có pH = 3. Cần pha loãng dung dịch axit này (bằng H2O) bao nhiêu lần để thu được dung dịch HCl có pH = 4?
A. 5 lần.
B. 8 lần.
C. 9 lần.
D. 10 lần.
Chọn C.
Pha loãng hay cô cạn dung dịch thì số mol chất tan không đổi, thể tích thay đổi nên nồng độ mol thay đổi, pH thay đổi.
Gọi Vl, V2 là thể tích dung dịch axit có pH = 3 và thể tích H2O cần dùng để pha loãng.
- p H = 3 ⇒ H + = 10 - 3 M ⇒ s ố m o l H + = 10 - 3 V 1
- p H = 4 ⇒ H + = 10 - 4 M ⇒ s ố m o l H + = 10 - 4 V 1 + V 2
- Số mol H+ trước = số mol H+ sau ⇒ 10 - 3 V 1 = 10 - 4 V 1 + V 2 ⇒ 9 V 1 = V 2
Vậy phải hòa 1 thể tích axit với 9 phần thể tích H2O.
Đúng 0
Bình luận (0)
Dung dịch HCl có pH = 3. Cần pha loãng dung dịch axit này (bằng nước) bao nhiêu lần để thu được dung dịch HCl có pH = 4?
A. 9.
B. 10.
C. 99.
D. 100.
Đáp án B
Gọi V, V’ lần lượt là thể tích dung dịch HCl có pH = 3, pH = 4
Do pH = 3 => [H+] = 10-3M => nH+trước khi pha loãng = 10-3V
pH = 4 => [H+] = 10-4M => nH+sau khi pha loãng = 10-4V’
Ta có nH+trước khi pha loãng = nH+sau khi pha loãng=> 10-3V = 10-4V’
=> V ' V = 10 - 3 10 - 4 = 10
Vậy cần pha loãng axit 10 lần
Đúng 0
Bình luận (0)

















