Một quặng sắt chứa 90% Fe3O4, còn lại là tạm chất. Nếu dùng khí H2 để khử 0,5 tấn quặng thì khối lượng sắt thu được là bao nhiêu ?

Những câu hỏi liên quan
Khử hoàn toàn 0,58 tấn quặng sắt chứa 90 % là
F
e
3
O
4
bằng khí hiđro. Khối lượng sắt thu được là: A. 0,378 tấn B. 0,156 tấn C. 0,126 tấn D. 0,467 tấn
Đọc tiếp
Khử hoàn toàn 0,58 tấn quặng sắt chứa 90 % là F e 3 O 4 bằng khí hiđro. Khối lượng sắt thu được là:
A. 0,378 tấn
B. 0,156 tấn
C. 0,126 tấn
D. 0,467 tấn
Chọn A

=> khối lượng F e 3 O 4 có trong quặng là 0,552 (tấn)
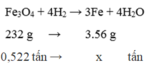
Vậy m F e = ( 0 , 522 . 3 . 56 ) : 232 = 0 , 378 t ấ n .
Đúng 0
Bình luận (0)
Một loại quặng sắt chứa 90% Fe3O4 còn lại là tạp chất ko chứa sắt tính khối lượng quặng còn lại để thu được 25,2(g) sắt
helpppp me ạ
Một quặng chứa 90% Fe3O4 còn lại là tạp chất.Nếu dùng khí H2 để khử 0.5 tấn quặng thì khối lượng sắt thu đc là bao nhiêu.
Khối lượng của Fe3O4 trong quặng là: 0,5 * 90% = 0,45 tấn
PTHH: 4H2 + Fe3O4 →3 Fe + 4H2O
...................+ 232 g........3*56 g.................
Vậy khử 450 g Fe3O4 thì đc x g Fe
⇒ x = \(\dfrac{450\cdot3\cdot56}{232}\) = 325,9 g = 0,326 tấn
Vậy....
Đúng 0
Bình luận (2)
Một quặng sắt chứa 90% Fe3O4 còn lại là tạp chất . Nếu dùng khí H2 để khử 0,5 tấn quặng thì khối lượng sắt thu được là bao nhiêu ?
- Khối lượng Fe3O4 trong 0,5 tấn quặng sắt là :
\(90\%.0,5=0,45\left(tons\right)=450000\left(g\right)\)
=> \(n_{Fe_3O_4}=\frac{m}{M}=\frac{56250}{29}\left(mol\right)\)
PTHH : \(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
Theo PTHH : \(n_{Fe}=\frac{168750}{29}\left(mol\right)\)
=> \(m_{Fe}=325862,069\left(g\right)\approx0,326\left(tons\right)\)
Đúng 0
Bình luận (0)
khử hoàn toàn 0,58 tấn quặng sắt chứa 80 % là Fe3O4 bằng khí hidro . Tính khối lượng sắt thu được ?
\(0,58\left(tấn\right)=580000\left(g\right)\\ \Rightarrow m_{Fe_3O_4}=580000\cdot80\%=464000\left(g\right)\\ \Rightarrow n_{Fe_3O_4}=\dfrac{464000}{232}=2000\left(mol\right)\\ PTHH:Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\\ \Rightarrow n_{Fe}=3n_{Fe_3O_4}=8000\left(mol\right)\\ \Rightarrow m_{Fe}=8000\cdot56=336000\left(g\right)=0,336\left(tấn\right)\)
Đúng 2
Bình luận (0)
Cho một luồng khí H2 (lấy dư) qua ống sứ đựng 10 gam quặng hemantit được đốt nóng ở nhiệt độ cao, sau khi phản ứng kết thúc, lấy chất rắn còn lại trong ống sứ đem hòa tan trong dung dịch HCl (lấy dư) thì thu được 2,24 lít khí H2 (đktc). Cho rằng quặng hemantit chứa Fe2O3 và các tạp chất coi như trơ. a) Tính phần trăm khối lượng Fe2O3 có trong quặng b) Cần bao nhiêu tấn quặng hemantit nói trên để sản xuất được 1 tấn gang chứa 96% sắt? Biết hiệu suất của quá trình là 80%.
Đọc tiếp
Cho một luồng khí H2 (lấy dư) qua ống sứ đựng 10 gam quặng hemantit được đốt nóng ở nhiệt độ cao, sau khi phản ứng kết thúc, lấy chất rắn còn lại trong ống sứ đem hòa tan trong dung dịch HCl (lấy dư) thì thu được 2,24 lít khí H2 (đktc). Cho rằng quặng hemantit chứa Fe2O3 và các tạp chất coi như trơ.
a) Tính phần trăm khối lượng Fe2O3 có trong quặng
b) Cần bao nhiêu tấn quặng hemantit nói trên để sản xuất được 1 tấn gang chứa 96% sắt? Biết hiệu suất của quá trình là 80%.
a. nH2 = nFe = 0,1mol
Bảo toàn nguyên tố Fe => nFe2O3 = 0,05mol
=> mFe2O3 = 8g
=> %Fe2O3 = (8:10) . 100% = 80%
Đúng 0
Bình luận (0)
M là một quặng sắt chứa 60% Fe2O3, N là một quặng sắt khác chứa 69,6% Fe3O4 trộn quặng M với N theo tỉ lệ khối lượng mM : mN = 2 : 5 ta được quặng C. Hỏi 1 tấn quặng C chứa bao nhiêu kg sắt
Ta có: \(\dfrac{m_M}{m_N}=\dfrac{2}{5}\Rightarrow5m_M-2m_N=0\left(1\right)\)
Mà: mM + mN = 1 (tấn) = 1000 (kg) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}m_M=\dfrac{2000}{7}\left(kg\right)\\m_N=\dfrac{5000}{7}\left(kg\right)\end{matrix}\right.\)
\(\Rightarrow m_{Fe_2O_3}=m_M.60\%=\dfrac{1200}{7}\left(kg\right)\Rightarrow n_{Fe_2O_3}=\dfrac{\dfrac{1200}{7}}{160}=\dfrac{15}{14}\left(kmol\right)\)
\(\Rightarrow n_{Fe}=2n_{Fe_2O_3}=\dfrac{15}{7}\left(kmol\right)\)
\(m_{Fe_3O_4}=m_N.69,6\%=\dfrac{3480}{7}\left(kg\right)\Rightarrow n_{Fe_3O_4}=\dfrac{\dfrac{3480}{7}}{232}=\dfrac{15}{7}\left(kmol\right)\)
\(\Rightarrow n_{Fe}=3n_{Fe_3O_4}=\dfrac{45}{7}\left(kmol\right)\)
\(\Rightarrow m_{Fe}=\left(\dfrac{15}{7}+\dfrac{45}{7}\right).56=480\left(kg\right)\)
Đúng 1
Bình luận (0)
M là một quặng sắt chứa 60% Fe2O3, N là một quặng sắt khác chứa 69,6% Fe3O4 trộn quặng M với N theo tỉ lệ khối lượng mM : mN = 2 : 5 ta được quặng C. Hỏi 1 tấn quặng C chứa bao nhiêu kg sắt
Bạn xem lời giải ở đây nhé.
https://olm.vn/hoi-dap/detail/7712766586263.html
Đúng 0
Bình luận (0)
A là một loại quặng sắt chứa 60% Fe2O3; B là loại quặng sắt khác chứa 69,6% Fe3O4. Hỏi trong một tấn quặng A hoặc B có chứa bao nhiêu kg sắt? 2. Trộn quặng A với quặng B theo tỉ lệ khối lượng mA:mB = 2:5 ta được quặng C có bao nhiêu kg sắt

















