Tỉ khối hơi của một hỗn hợp A gồm ozon và oxi đối với hidro là 18 . Xác định % theo thể tích của mỗi khí trong hỗn hợp

Những câu hỏi liên quan
1) Có một hỗn hợp khí gồm oxi và ozon. Hỗn hợp khí này có tỉ khối đối vs hidro là 18. Hãy xác đimhj thành phần phần trăm theo thể tích của hỗn hợp khí2) Hỗn hợp khí A gồm O2 và O3, tỉ khối hơi của hỗn hợp khí A và khí H2 là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hh khí B đối vs H2 là 3,6.@a) Tính thành phần % theo thể tích của mỗi khí có trong hh khí A và Bb) Một mol khí A có thể đốt cháy hoàn toàn bao nhiêu mol khí COGiải theo pp tăng giảm khối lượng hoặc phương pháp trung bình
Đọc tiếp
1) Có một hỗn hợp khí gồm oxi và ozon. Hỗn hợp khí này có tỉ khối đối vs hidro là 18. Hãy xác đimhj thành phần phần trăm theo thể tích của hỗn hợp khí
2) Hỗn hợp khí A gồm O2 và O3, tỉ khối hơi của hỗn hợp khí A và khí H2 là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hh khí B đối vs H2 là 3,6.
@
a) Tính thành phần % theo thể tích của mỗi khí có trong hh khí A và B
b) Một mol khí A có thể đốt cháy hoàn toàn bao nhiêu mol khí CO
Giải theo pp tăng giảm khối lượng hoặc phương pháp trung bình
Tỉ khối hơi của một hỗn hợp A gồm ozon và oxi đối với hidro là 18.
a) Xác định % theo thể tích của mỗi khí trong hỗn hợp đầu.
b) Tính dA/oxi
Tỉ khối của một hỗn hợp gồm oxi và ozon đối với hiđro là 18.
a. Tính thành phần phần trăm theo thể tích của hỗn hợp A ban đầu.
b. Tính tỉ khối hơi của A so với oxi.
Coi số mol hỗn hợp X = 1 mol.
nO2 = x (mol) ; nO3 = y (mol)
x + y = 1
32x + 48y = 1.18.2
⇒ x = 0,75, y = 0,25 (mol)
⇒ %VO2 = 75% ; %VO3 = 25%
Đúng 0
Bình luận (0)
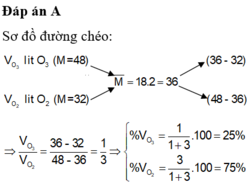
Có một hỗn hợp khí gồm oxi và ozon. Hỗn hợp khí này có ti khối đối với hiđro bằng 18. Hãy xác định thành phần phần trăm theo thể tích của hỗn hợp khí.
Khối lượng mol trung bình của hỗn hợp khí:
M = 18 x 2 = 36(g/mol)
Đặt x và y là số mol O 3 và O 2 có trong 1 mol hỗn hợp khí, ta có phương trình đại số :
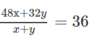
Giải phương trình, ta có y = 3x. Biết rằng tỉ lệ phần trăm về số mol khí cũng là tỉ lệ về thể tích : Thể tích khí oxi gấp 3 lần thể tích khí ozon. Thành phần của hỗn hợp khí là 25% ozon và 75% oxi.
Đúng 0
Bình luận (0)
Hỗn hợp khí X gồm oxi và ozon có tỉ khối so với hidro là 16,2. % của ozon theo thể tích
trong hỗn hợp là
Gọi số mol O2, O3 là a, b (mol)
Có: \(\dfrac{32a+48b}{a+b}=16,2.2=32,4\left(g/mol\right)\)
=> 0,4a = 15,6b
=> a = 39b
\(\%V_{O_3}=\dfrac{b}{a+b}.100\%=\dfrac{b}{39b+b}.100\%=2,5\%\)
Đúng 1
Bình luận (0)
Hỗn hợp khí ozon và oxi có tỉ khối so với khí H 2 là 18. Xác định % thể tích của ozon trong hỗn hợp.
Gọi x là số mol O 3 có trong 1 mol hỗn hợp khí, số mol O 2 sẽ là (1 - x) mol.
Ta có phương trình : 48x + (1 - x).32 = 18.2
Giải ra x = 0,25.
Do %n = %V nên ozon chiếm 25% thể tích hỗn hợp.
Đúng 1
Bình luận (0)
Hỗn hợp khí X gồm ozon và oxi có tỉ khối đối với hiđro bằng 18. Phần trăm theo thể tích mỗi khí trong hỗn hợp X lần lượt là:
A. 25% và 75%
B. 30% và 70%
C. 35% và 65%
D. 40% và 60%
4) hỗn hợp X gồm ozon và oxi có tỉ khối hơi so vs hiđro=18 a) xác định % khối lượng các khí trong X b) tính thể tích mỗi khí có trong 2,88 gam hh khí trên
\(a)n_{O_3} = a ; n_{O_2} = b\\ M_X = 18.2 = 36(g/mol)\\ \text{Ta có : } 48a + 32b = 36(a + b)\\ \Leftrightarrow 12a = 4b \Leftrightarrow \dfrac{a}{b} = \dfrac{4}{12} = \dfrac{1}{3}(1)\\ \%V_{O_3} = \dfrac{1}{1+3}.100\% = 25\%\\ \%V_{O_2} = \dfrac{3}{1+3}.100\% = 75\%\\ b) m_X = 48a + 32b = 2,88(2)\\ (1)(2) \Rightarrow a = 0,02 ; b = 0,06\\ V_{O_3} = 0,02.22,4 = 0,448(lít) ; V_{O_2} = 0,06.22,4 = 1,344(lít)\)
Đúng 0
Bình luận (0)
2) hỗn hợp khí A gồm ozon và oxi có tỉ khối hơi vs hiđro=19,2 a) xác định % thể tích của A b) tính khối lượng mỗi khí có trong 7,68 gam hh khí trên
\(n_{O_3} = a ; n_{O_2} = b(mol)\\ M_A = 19,2.2 = 38,4(g/mol)\\ m_{khí} = 48a + 32b = 7,68\\ n_{khí} = a + b = \dfrac{7,68}{38,4} = 0,2\\ \Rightarrow a = 0,08 ; b = 0,12\\ \%V_{O_3} = \dfrac{0,08}{0,2}.100\% = 40\% \Rightarrow \%V_{O_2} = 100\% -40\% = 60\%\\ m_{O_3} = 0,08.48 = 3,84(gam) ; m_{O_2} = 0,12.32 = 3,84(gam)\)
Đúng 0
Bình luận (0)