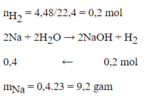Cho 1 mẩu Na cho vào nước (Dnước = 1g/ml) thấy có 1 khí bay ra và tạo 1 dung dịch có tính kiềm. Tính C% của dung dịch sau phản ứng. Biết rằng khối lượng của Na là 23g

Những câu hỏi liên quan
Cho một mẩu Na hoà tan hoàn toàn vào nước sau phản ứng thu được dung dịch có chứa 8 gam NaOH. Khối lượng của Na đã phản ứng và thể tích khí H2 (đktc) đã sinh ra sau phản ứng lần lượt là:
2Na+2H2o->2NaOH+H2
0,2------------------0,2----0,1
n NaOH=0,2 mol
=>m Na=0,2.23=4,6g
=>VH2=0,1.22,4=2,24l
Đúng 3
Bình luận (0)
\(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\)
PTHH: 2Na + 2H2O ---> 2NaOH + H2
0,2 0,2 0,1
\(\rightarrow\left\{{}\begin{matrix}m_{Na}=0,2.23=4,6\left(g\right)\\V_{H_2}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)
PTHH: 2Na+2H2O→2NaOH+H2↑
nNaOH=mNaOH/MNaOH=8/40=0,2(mol)
Theo PTHH ta thấy: nNa=nNaOH=0,2mol
⇒mNa=0,2.23=4,6 gam
Theo PTHH ta cũng thấy:
nH2=1/2.nNaOH=1/2.0,2=0,1 mol
=> VH2= 0,1. 22,4= 2,24(l)
Vậy : mNa=4,6gam; VH2=2,24l
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp X gồm Na và Ba vào 200 ml dung dịch KHCO3 0,6M và Ca(HCO3)2 0,5M. Sau các phản ứng, khối lượng dung dịch giảm 15,34 gam so với dung dịch ban đầu. Lọc tách kết tủa, thu được dung dịch Y. Nhỏ từ từ dung dịch HCl 1M vào Y cho tới khi vừa có khí thoát ra thì thấy dùng hết 230 ml. Phần trăm khối lượng của Na trong X là A. 12,27%. B. 16,77%. C. 14,38%. D. 18,29%.
Đọc tiếp
Cho m gam hỗn hợp X gồm Na và Ba vào 200 ml dung dịch KHCO3 0,6M và Ca(HCO3)2 0,5M. Sau các phản ứng, khối lượng dung dịch giảm 15,34 gam so với dung dịch ban đầu. Lọc tách kết tủa, thu được dung dịch Y. Nhỏ từ từ dung dịch HCl 1M vào Y cho tới khi vừa có khí thoát ra thì thấy dùng hết 230 ml. Phần trăm khối lượng của Na trong X là
A. 12,27%.
B. 16,77%.
C. 14,38%.
D. 18,29%.
Cho 6,8 (gam) hỗn hợp X gồm Mg và Fe vào 300 ml dung dịch H2SO4 loãng a (M) thì thu được 3,7185 lít khí bay ra (ở 25°c, 1 bar) và dung dịch A.
a. Tính % khối lượng mỗi kim loại trong X và khối lượng muối có trong dung dịch tạo thành sau phản ứng và a?
b. Nếu cho hỗn hợp X tác dụng vừa đủ với H2SO4 đặc nóng thì thu được dung dịch A và V lít khí SO2 (ở 25°c, 1 bar) duy nhất. Tính giá trị của V và khối lượng H2SO4 tham gia phản
Đọc tiếp
Cho 6,8 (gam) hỗn hợp X gồm Mg và Fe vào 300 ml dung dịch H2SO4 loãng a (M) thì thu được 3,7185 lít khí bay ra (ở 25°c, 1 bar) và dung dịch A. a. Tính % khối lượng mỗi kim loại trong X và khối lượng muối có trong dung dịch tạo thành sau phản ứng và a? b. Nếu cho hỗn hợp X tác dụng vừa đủ với H2SO4 đặc nóng thì thu được dung dịch A và V lít khí SO2 (ở 25°c, 1 bar) duy nhất. Tính giá trị của V và khối lượng H2SO4 tham gia phản
sửa đề: Tính V và a
\(a.n_{H_2}=\dfrac{3,7185}{24,79}=0,15mol\\ n_{Mg}=a;n_{Fe}=b\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ \Rightarrow\left\{{}\begin{matrix}a+b=0,15\\24a+56b=6,8\end{matrix}\right.\\ \Rightarrow a=0,05;b=0,1\\ \%m_{Mg}=\dfrac{0,05.24}{6,8}\cdot100=17,65\%\\ \%m_{Fe}=100-17,65=82,35\%\)
\(b.Mg+2H_2SO_4\rightarrow MgSO_4+SO_2+2H_2O\\ Fe+2H_2SO_4\rightarrow FeSO_4+SO_2+2H_2O\\ n_{SO_2}=0,05+0,1=0,15mol\\ V_{SO_2}=0,15.24,79=3,7185l\\ n_{H_2SO_4\left(a\right)}=0,05+0,1=0,15mol\\ C_{M\left(H_2SO_4\right)}=\dfrac{0,15}{0,3}=0,5M\)
Đúng 3
Bình luận (0)
Cho 6,8 (gam) hỗn hợp X gồm Mg và Fe vào 300 ml dung dịch H2SO4 loãng a (M) thì thu được 3,7185 lít khí bay ra (ở 25°c, 1 bar) và dung dịch A.
a. Tính % khối lượng mỗi kim loại trong X và khối lượng muối có trong dung dịch tạo thành sau phản ứng và a?
b. Nếu cho hỗn hợp X tác dụng vừa đủ với H2SO4 đặc nóng thì thu được dung dịch A và V lít khí SO2 (ở 25°c, 1 bar) duy nhất. Tính giá trị của V và khối lượng H2SO4 tham gia phản
Đọc tiếp
Cho 6,8 (gam) hỗn hợp X gồm Mg và Fe vào 300 ml dung dịch H2SO4 loãng a (M) thì thu được 3,7185 lít khí bay ra (ở 25°c, 1 bar) và dung dịch A. a. Tính % khối lượng mỗi kim loại trong X và khối lượng muối có trong dung dịch tạo thành sau phản ứng và a? b. Nếu cho hỗn hợp X tác dụng vừa đủ với H2SO4 đặc nóng thì thu được dung dịch A và V lít khí SO2 (ở 25°c, 1 bar) duy nhất. Tính giá trị của V và khối lượng H2SO4 tham gia phản
Để giải bài toán này, ta cần sử dụng các phương trình hoá học và các phương trình tính toán liên quan đến phản ứng hóa học. Dưới đây là cách giải chi tiết:
a. Đầu tiên, ta cần xác định số mol của Mg và Fe trong hỗn hợp X. Ta biểu diễn số mol của Mg là nMg và số mol của Fe là nFe.
Ta có phương trình phản ứng như sau: Mg + H2SO4 → MgSO4 + H2↑ Fe + H2SO4 → FeSO4 + H2↑
Với 6,8 (gam) hỗn hợp X, ta cần tính số mol của hỗn hợp X bằng cách chia khối lượng cho khối lượng mol của hỗn hợp X.
Khối lượng mol của Mg là 24,3 g/mol, khối lượng mol của Fe là 55,8 g/mol. Vậy, khối lượng mol của hỗn hợp X là: (6,8 g) / (24,3 g/mol + 55,8 g/mol) = 0,0677 mol
Tiếp theo, ta cần tính nồng độ của dung dịch H2SO4 (a). Để làm điều này, ta sử dụng công thức:
nH2SO4 = V × a
Trong đó, nH2SO4 là số mol H2SO4, V là thể tích dung dịch H2SO4 (300 ml = 0,3 l), và a là nồng độ của dung dịch H2SO4.
Ta biết rằng số mol H2SO4 phản ứng là nH2SO4 = 0,0677 mol (do số mol của Mg và Fe trong hỗn hợp X là như nhau). Vì vậy, ta có:
0,0677 mol = 0,3 l × a a = 0,0677 mol / 0,3 l a = 0,2257 M
Tiếp theo, ta tính khối lượng của muối có trong dung dịch tạo thành sau phản ứng. Ta biết rằng phản ứng xảy ra theo tỉ lệ 1:1 giữa Mg và muối MgSO4, và tỉ lệ 1:1 giữa Fe và muối FeSO4. Vì vậy, số mol của muối MgSO4 và muối FeSO4 sẽ bằng số mol ban đầu của Mg và Fe trong hỗn hợp X.
Khối lượng muối MgSO4 và muối FeSO4 có thể tính bằng công thức:
Khối lượng muối = số mol × khối lượng mol
Khối lượng muối MgSO4 = nMg × khối lượng mol MgSO4 Khối lượng muối FeSO4 = nFe × khối lượng mol FeSO4
Khối lượng mol MgSO4 là 120,4 g/mol và khối lượng mol FeSO4 là 151,9 g/mol.
Vậy, khối lượng muối có trong dung dịch tạo thành là: Khối lượng muối = (nMg + nFe) × khối lượng mol muối Khối lượng muối = 0,0677 mol × (120,4 g/mol + 151,9 g/mol) = 18,69 g
Cuối cùng, ta tính phần trăm khối lượng của mỗi kim loại trong hỗn hợp X:
Phần trăm khối lượng Mg = (nMg × khối lượng mol Mg) / khối lượng hỗn hợp X × 100% Phần trăm khối lượng Fe = (nFe × khối lượng mol Fe) / khối lượng hỗn hợp X × 100%
Phần trăm khối lượng Mg = (0,0677 mol × 24,3 g/mol) / 6,8 g × 100% Phần trăm khối lượng Fe = (0,0677 mol × 55,8 g/mol) / 6,8 g × 100%
b. Nếu cho hỗn hợp X tác dụng vừa đủ với H2SO4 đặc nóng, phản ứng sẽ xảy ra theo phương trình:
Mg + H2SO4 → MgSO4 + H2↑
Từ phương trình này, ta thấy tỉ lệ giữa số mol Mg và số mol H2SO4 là 1:1. Vì vậy, số mol H2SO4 tham gia phản ứng sẽ bằng số mol Mg trong hỗn hợp X. Ta đã tính được số mol Mg trong hỗn hợp X là 0,0677 mol.
Vậy, khối lượng H2SO4 tham gia phản ứng là: Khối lượng H2SO4 = số mol H2SO4 × khối lượng mol H2SO4
Khối lượng mol H2SO4 là 98 g/mol.
Vậy, khối lượng H2SO4 tham gia phản ứng là: Khối lượng H2SO4 = 0,0677 mol × 98 g/mol = 6,63 g
Để tính giá trị của V, ta sử dụng công thức:
V = số mol khí SO2 × (R × T) / P
Trong đó, số mol khí SO2 là số mol Mg trong hỗn hợp X (0,0677 mol), R là hằng số khí (0,0821 L·atm/(mol·K)), T là nhiệt độ (25 °C = 298 K), và P là áp suất (1 bar).
V = 0,0677 mol × (0,0821 L·atm/(mol·K) × 298 K) / 1 bar V = 1,61 L
Vậy, giá trị của V là 1,61 L và khối lượng H2SO4 tham gia phản ứng là 6,63 g.
Đúng 0
Bình luận (0)
Cho mẩu Na vào nước thấy có 4,48(l) khí bay lên. Tính khối lượng Na đã tham gia phản ứng?
A. 9,2g
B. 4,6g
C. 2g
D. 9,6g
Cho mẩu natri hòa tan hết vào 2 lít nước lấy dư thấy có 4,48 lít khí bay lên ở đktc.
a. Tính khối lượng natri phản ứng?
b. Tính nồng độ mol của dd baZơ tạo thành sau phản ứng. Coi thể tích dung dịch thay đổi không đáng kể
a, \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
Theo PT: \(n_{Na}=2n_{H_2}=0,4\left(mol\right)\Rightarrow m_{Na}=0,4.23=9,2\left(g\right)\)
b, \(n_{NaOH}=2n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow C_{M_{NaOH}}=\dfrac{0,4}{2}=0,2\left(M\right)\)
Đúng 1
Bình luận (0)
M.n ơi giải giúp em 2 câu này với ạ (em đang cần gấp ) 1 hòa tan 4gam NaOH vào 200ml H2O ( khối lượng riêng của nước là 1g/ml) thu được dung dịch A. Nồng độ % của A là bao nhiêu? 2. Khi cho Na vào dung dịch CuSO4 thấy xuất hiện sủi bọt khí và có chất kết tủa xanh trong dung dịch. Chất khí và chất kết tủa đó là 2 chất nào?
Bài 1: Cho 6,9 gam natri (Na) vào 100g nước. Sau phản ứng thu được dung dịch Kali hiđroxit NaOH) và khí hiđro. a. Tính thể tích của khí H2 thu được ở (đktc).b. Tính khối lượng dung dịch thu được sau phản ứng.
Đọc tiếp
Bài 1: Cho 6,9 gam natri (Na) vào 100g nước. Sau phản ứng thu được dung dịch Kali hiđroxit NaOH) và khí hiđro.
a. Tính thể tích của khí H2 thu được ở (đktc).
b. Tính khối lượng dung dịch thu được sau phản ứng.
\(n_{Na}=\dfrac{6,9}{23}=0,3\left(mol\right)\\ 2Na+2H_2O\rightarrow2NaOH+H_2\\ n_{H_2}=\dfrac{0,3}{2}=0,15\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,15.22,4=3,36\left(l\right)\\ b,m_{ddsaup.ứ}=m_{Na}+m_{H_2O}-m_{H_2}=6,9+100-0,15.2=106,6\left(g\right)\)
Đúng 1
Bình luận (0)
Cho m gam một mẩu kim loại Ba tan hết vào 100 ml dung dịch A gồm HCl 0,08M và Al2(SO4)3 0,5M. Sau các phản ứng thu được dung dịch X, kết tủa Y và khí Z. Khối lượng dung dịch X giảm so sới dung dịch A là 14,19 gam. Thêm tiếp V ml dung dịch HCl 1M vào dung dịch X thấy xuất hiện 0,78gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Viết phương trình phản ứng xảy ra và tính giá trị của m, V.
Đọc tiếp
Cho m gam một mẩu kim loại Ba tan hết vào 100 ml dung dịch A gồm HCl 0,08M và Al2(SO4)3 0,5M. Sau các phản ứng thu được dung dịch X, kết tủa Y và khí Z. Khối lượng dung dịch X giảm so sới dung dịch A là 14,19 gam. Thêm tiếp V ml dung dịch HCl 1M vào dung dịch X thấy xuất hiện 0,78gam kết tủa. Biết các phản ứng xảy ra hoàn toàn.
Viết phương trình phản ứng xảy ra và tính giá trị của m, V.
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
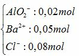 + V ml HCl 1M→ Al(OH)3: 0,01 (mol)
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
Đúng 0
Bình luận (0)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
Đúng 0
Bình luận (0)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời