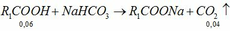cho 90 gam hỗn hợp rượu etylic và axit axetic tác dụng với dung dịch natri cacbonnat ,sau phản ứng thấy 11,2 lít khí cacbonnat thoát ra ở điều kiện tiêu chuẩn .viết phương trình phản ứng xảy ra .tính khối lượng của mỗi chất trong hỗn hợp đầu

Những câu hỏi liên quan
cho 90 gam hỗn hợp rượu etylic và axit axetic tác dụng hoàn toàn với dung dịch Na2CO3 sau phản ứng thấ có 11,2 lít khí CO2 thoát ra
Cho a gam hỗn hợp gồm rượu etylic và axit axetic người ta tiến hành hai thí nghiệm sau thí nghiệm 1 cho a gam hỗn hợp tác dụng với natri sau phản ứng thu được 16,8 lít khí ở điều kiện tiêu chuẩn thí nghiệm 2 cho a gam hỗn hợp trên tác dụng với bari cacbonat sau phản ứng thu được 6,72 lít khí ở điều kiện tiêu chuẩn a tính thành phần phần trăm theo khối lượng các chất trong hỗn hợp ban đầu b tính khối lượng natri cần dùng. Giúp em vs ạ cần gấp
Đọc tiếp
Cho a gam hỗn hợp gồm rượu etylic và axit axetic người ta tiến hành hai thí nghiệm sau thí nghiệm 1 cho a gam hỗn hợp tác dụng với natri sau phản ứng thu được 16,8 lít khí ở điều kiện tiêu chuẩn thí nghiệm 2 cho a gam hỗn hợp trên tác dụng với bari cacbonat sau phản ứng thu được 6,72 lít khí ở điều kiện tiêu chuẩn a tính thành phần phần trăm theo khối lượng các chất trong hỗn hợp ban đầu b tính khối lượng natri cần dùng. Giúp em vs ạ cần gấp
Hòa tan hoàn toàn 17,1 gam hỗn hợp A gồm Mg và Al tác dụng vừa đủ với dung dịch axit clohidric (HCl). Sau phản ứng thu được dung dịch B và 18,48 lít khí hidro thoát ra (đo ở điều kiện tiêu chuẩn). a. Tính các phương trình hóa học xảy ra. b. Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp A
\(a.Mg+2HCl\rightarrow MgCl_2+H_2\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ b.Đặt:\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\\ n_{H_2}=\dfrac{18,48}{22,4}=0,825\left(mol\right)\\ Tacó:\left\{{}\begin{matrix}24x+27y=17,1\\x+\dfrac{3}{2}y=0.825\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,375\\y=0,3\end{matrix}\right.\\ \Rightarrow\%m_{Mg}=\dfrac{0,375.24}{17,1}.100=52,63\%\\ \%m_{Al}=47,37\%\)
Đúng 1
Bình luận (0)
Cho 39,6g hỗn hợp rượu etylic và axit axetic tác dụng vừa đủ với dung dịch natri cacbonat 2M; sau phản ứng thoát ra 2,24 lít khí X (đktc):
a, Tính % khối lượng từng chất trong hỗn hợp ban đầu.
b, Tính nồng độ mol dung dịch sau phản ứng
(Biết thể thích dung dịch thay đổi không đáng kể)
Các bạn giúp mình với nha, mình cần gấp ạ. Cảm ơn bạn nhiều <3
Rượu etylic \(C_2H_5OH\)
Axit axetic \(CH_3COOH\)
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(2CH_3COOH+Na_2CO_3\rightarrow2CH_3COONa+H_2O+CO_2\uparrow\)
0,2 0,1 0,2 0,1 0,1
\(\%m_{CH_3COOH}=\dfrac{0,2\cdot60}{39,6}\cdot100\%=30,3\%\)
\(\%m_{C_2H_5OH}=100\%-30,3\%=69,7\%\)
Đúng 1
Bình luận (1)
a)
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2CH3COOH + Na2CO3 --> 2CH3COONa + CO2 + H2O
0,2<----------0,1<-------------0,2<-------0,1
=> \(m_{CH_3COOH}=0,2.60=12\left(g\right)\)
\(\%m_{CH_3COOH}=\dfrac{12}{39,6}.100\%=30,3\%\)
\(\%m_{C_2H_5OH}=\dfrac{39,6-12}{39,6}.100\%=69,7\%\)
b) dd sau pư chứa \(\left\{{}\begin{matrix}CH_3COONa:0,2\left(mol\right)\\C_2H_5OH:\dfrac{39,6-12}{46}=0,6\left(mol\right)\end{matrix}\right.\)
\(V_{dd}=\dfrac{0,1}{2}=0,05\left(l\right)\)
=> \(\left\{{}\begin{matrix}C_{M\left(CH_3COONa\right)}=\dfrac{0,2}{0,05}=4M\\C_{M\left(C_2H_5OH\right)}=\dfrac{0,6}{0,05}=12M\end{matrix}\right.\)
Đúng 3
Bình luận (1)
cho 45 gam hỗn hợp rượu etylic và axit axetic tác dụng hoàn toàn với dung dịch na2co3,sau phản ứng thấy có 5,6 lít khí c02 thoát ra(ở đktc)
a)viết pt
b)tính khối lượng của mỗi chất đầu trong hỗn hợp đầu
c)dẫn khí co2 thu được ở trên vào lọ đựng 50gam dung dịch NaOh 20%.Hãy tính khối lượng muối cacbonat thu được
giúp mình với mai mình thi ạ,cảm ơn mng trước
a.b.\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25mol\)
\(2CH_3COOH+Na_2CO_3\rightarrow2CH_3COONa+CO_2+H_2O\)
0,5 0,25 ( mol )
\(m_{CH_3COOH}=0,5.60=30g\)
\(\%m_{CH_3COOH}=\dfrac{30}{45}.100=66,67\%\)
\(\%m_{C_2H_5OH}=100\%-66,67\%=33,33\%\)
c.\(m_{NaOH}=50.20\%=10g\)
\(n_{NaOH}=\dfrac{10}{40}=0,25mol\)
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(\dfrac{0,25}{2}\) < \(\dfrac{0,25}{1}\) ( mol )
0,25 0,125 ( mol )
\(m_{Na_2CO_3}=0,125.106=13,25g\)
Đúng 1
Bình luận (0)
a)
2CH3COOH + Na2CO3 --> 2CH3COONa + CO2 + H2O
b) \(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2CH3COOH + Na2CO3 --> 2CH3COONa + CO2 + H2O
0,5<-----------------------------------0,25
=> mCH3COOH = 0,5.60 = 30 (g)
=> mC2H5OH = 45 - 30 = 15 (g)
c) \(n_{NaOH}=\dfrac{50.20\%}{40}=0,25\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,25}{0,25}=1\) => Tạo muối NaHCO3
PTHH: NaOH + CO2 --> NaHCO3
0,25-------------->0,25
=> mNaHCO3 = 0,25.84 = 21 (g)
Đúng 1
Bình luận (0)
Cho x gam rượu etylic tác dụng với lượng dư Natri thu được 16,8 lít khí ở điều kiện tiêu chuẩn
a,Viết phương trình hóa học xảy ra
b, Tính x
c, Cho toàn bộ lượng rượu etylic như trên vào 200 gam dung dịch axit axetic 60% có xúc tác H2SO4 đặc đun nóng. Sau khi phản ứng kết thúc thì thu được bao nhiêu gam etyl axetat( biết hiệu suất của phản ứng này là 60%)
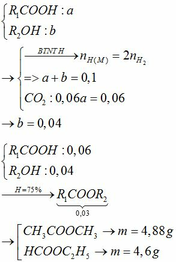
Chia hỗn hợp M gồm axit hữu cơ A (CnH2n+1COOH) và rượu B (CmH2m+1OH) làm ba phần bằng nhau: – Phần 1: cho tác dụng với Na dư thu được 1,12 lít khí. – Phần 2: cho tác dụng với dung dịch NaHCO3 dư thu được 1,344 lít khí. – Phần 3: đun nóng với axit H2SO4 đặc thì thu được 2,22 gam este E. Biết chỉ xảy ra phản ứng este hóa với hiệu suất phản ứng 75%. a. Viết phương trình phản ứng xảy ra. b. Xác định công thức phân tử của A, B và tính khối lượng hỗn hợp M đã sử dụng. Biết các thể tích khí đo ở điều k...
Đọc tiếp
Chia hỗn hợp M gồm axit hữu cơ A (CnH2n+1COOH) và rượu B (CmH2m+1OH) làm ba phần bằng nhau:
– Phần 1: cho tác dụng với Na dư thu được 1,12 lít khí.
– Phần 2: cho tác dụng với dung dịch NaHCO3 dư thu được 1,344 lít khí.
– Phần 3: đun nóng với axit H2SO4 đặc thì thu được 2,22 gam este E. Biết chỉ xảy ra phản ứng este hóa với hiệu suất phản ứng 75%.
a. Viết phương trình phản ứng xảy ra.
b. Xác định công thức phân tử của A, B và tính khối lượng hỗn hợp M đã sử dụng. Biết các thể tích khí đo ở điều kiện tiêu chuẩn.
Cho một miếng natri kim loại(lấy dư) vào 10,6g hỗn hợp có chứa rượu etylic và axit axetic. Sau phản ứng kết thúc, người ta thu được 2,24l khí thoát ra ở điều kiện tiêu chuẩn a, viết pthh b, tính thành phần phần trăm của mỗi chất có trong hỗn hợp ban đầu
\(Đặt:n_{C_2H_5OH}=a\left(mol\right);n_{CH_3COOH}=b\left(mol\right)\left(a,b>0\right)\\ a,PTHH:C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\\ CH_3COOH+Na\rightarrow CH_3COONa+\dfrac{1}{2}H_2\\ n_{H_2\left(tổng\right)}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ b,Ta.lập.hpt:\left\{{}\begin{matrix}46a+60b=10,6\\0,5a+0,5b=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \%m_{C_2H_5OH}=\dfrac{0,1.46}{10,6}.100\approx43,396\%\\\Rightarrow\%m_{CH_3COOH}\approx100\%-43,396\%\approx56,604\%\)
Đúng 1
Bình luận (0)
Cho 24g hỗn hợp gồm Zn và MgO tác dụng vừa đủ với dung dịch H2SO4 thấy thoát ra 11,2 lít khí Hiđro.
a, Viết phương trình phản ứng xảy ra?
b, Tính khối lượng của mỗi chất trong hỗn hợp ban đầu?
c, Tính khối lượng của axit H2SO4 đã tham gia phản ứng.
Ta có: \(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
a. PTHH:
Zn + H2SO4 ---> ZnSO4 + H2 (1)
MgO + H2SO4 ---> MgSO4 + H2O (2)
b. Theo PT(1): \(n_{Zn}=n_{H_2}=0,5\left(mol\right)\)
=> \(m_{Zn}=0,5.65=32,5\left(g\right)\)
(Sai đề nhé.)
Đúng 1
Bình luận (2)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5mol\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
0,5 0,5
b)\(m_{Zn}=0,5\cdot65=32,5\left(g\right)\)
\(m_{ZnO}=\) ko tính đc do lỗi đề
Đúng 1
Bình luận (1)