Hòa tan hết 4,2 gam hỗn hợp Fe và kim loại A hóa trị II vào dung dịch HCl thu được 2,24 lít khí đktc Nếu 5,5 gam kim loại A tác dụng với dung dịch loãng có chứa 14,7 gam H2SO4 thì sau phản ứng axit vẫn còn dư Xác định kim loại A

Những câu hỏi liên quan
Hòa tan hoàn toàn 4 gam hỗn hợp gồm Fe và một kim loại hóa trị II vào dung dịch HCl dư, thu được 2,24 lít khí H2 (đktc). Nếu chỉ dùng 2,4 gam kim loại hóa trị II thì sử dụng không hết 0,5 mol HCl. Xác định tên kim loại hóa trị II.
Hòa tan 12 gam hỗn hợp gồm Fe và một kim loại M hóa trị II vào dung dịch H2SO4 dư thu được 4,48 lít H2 (đktc). Nếu hòa tan 23,8 gam kim loại M vào dung dịch chứa 0,7 mol HCl thì M không tan hết. Tìm M
\(n_{Fe} = a(mol) ; n_M = b(mol)\\ \Rightarrow 56a + Mb = 12\)
\(Fe + 2HCl \to FeCl_2 + H_2\\ M + 2HCl \to MCl_2 + H_2\\ n_{H_2} = a + b = \dfrac{4,48}{22,4} = 0,2(mol)\\ \Rightarrow a = 0,2 - b ( 0< b < 0,2)\)
Suy ra:
56(0,2 - b) + Mb = 12
\(\Rightarrow M = \dfrac{0,8 + 56b}{b}\)
Vì 0 < b < 0,12
Nên M > 62,67(1)
Mặt khác,
\(n_M > \dfrac{1}{2}n_{HCl} = 0,35\\ \Rightarrow M < \dfrac{23,8}{0,35} = 68(2)\)
Từ (1)(2) suy ra: 62,67 < M < 68
Do đó, M = 65(Zn) thì thỏa mãn
Vậy M là Zn(Kẽm)
Đúng 2
Bình luận (0)
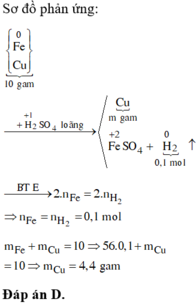
Cho 10 gam hỗn hợp gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng thu được 2,24 lít khí H2 (đktc), dung dịch X và m gam kim loại không tan. Giá trị m là A. 6,4. B. 3,4. C. 4,4. D. 5,6.
Đọc tiếp
Cho 10 gam hỗn hợp gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng thu được 2,24 lít khí H2 (đktc), dung dịch X và m gam kim loại không tan. Giá trị m là
A. 6,4.
B. 3,4.
C. 4,4.
D. 5,6.
Cho 18,6 gam hỗn hợp gồm Fe và kim loại R (hoá trị II không đổi) vào dung dịch chứa 25,55 gam HCl, kết thúc phản ứng thu được 6,72 lít khí (đktc). Nếu cho 2,3275 gam kim loại R vào dung dịch chứa 3,43 gam H2SO4 loãng, sau phản ứng hoàn toàn vẫn còn dư kim loại. Xác định kim loại R?
Đọc tiếp
Cho 18,6 gam hỗn hợp gồm Fe và kim loại R (hoá trị II không đổi) vào dung dịch chứa 25,55 gam HCl, kết thúc phản ứng thu được 6,72 lít khí (đktc). Nếu cho 2,3275 gam kim loại R vào dung dịch chứa 3,43 gam H2SO4 loãng, sau phản ứng hoàn toàn vẫn còn dư kim loại. Xác định kim loại R?
Cho 18,6 gam hỗn hợp gồm Fe và kim loại R (hoá trị II không đổi) vào dung dịch chứa 25,55 gam HCl, kết thúc phản ứng thu được 6,72 lít khí (đktc). Nếu cho 2,3275 gam kim loại R vào dung dịch chứa 3,43 gam H2SO4 loãng, sau phản ứng hoàn toàn vẫn còn dư kim loại. Xác định kim loại R?
Đọc tiếp
Cho 18,6 gam hỗn hợp gồm Fe và kim loại R (hoá trị II không đổi) vào dung dịch chứa 25,55 gam HCl, kết thúc phản ứng thu được 6,72 lít khí (đktc). Nếu cho 2,3275 gam kim loại R vào dung dịch chứa 3,43 gam H2SO4 loãng, sau phản ứng hoàn toàn vẫn còn dư kim loại. Xác định kim loại R?
Cho 10 gam hỗn hợp gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng thu được 2,24 lít khí hiđro (ở đktc), dung dịch X và m gam kim loại không tan. Giá trị của m là A. 6,4 gam B. 3,4 gam C. 4,4 gam D. 5,6 gam
Đọc tiếp
Cho 10 gam hỗn hợp gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng thu được 2,24 lít khí hiđro (ở đktc), dung dịch X và m gam kim loại không tan. Giá trị của m là
A. 6,4 gam
B. 3,4 gam
C. 4,4 gam
D. 5,6 gam
Đáp án C
nFe = nH2 = 0,1 mol
Chất rắn không tan là Cu
=> m = 10 – mFe = 10 – 0,1 . 56 = 4,4g
Đúng 0
Bình luận (0)
Cho 10 gam hỗn hợp gồm Fe và Cu tác dụng với dung dịch H 2 SO 4 loãng, dư. Sau phản ứng thu được 2,24 lít khí hiđro (ở đktc), dung dịch X và m gam kim loại không tan. Xác định giá trị của m.
Phương trình hóa học của phản ứng:
Cu + H 2 SO 4 → Không phản ứng
Fe + H 2 SO 4 → FeSO 4 + H 2
n H 2 = 2,24/22,4 = 0,1 mol
n Fe = 0,1 x 56 = 5,6g. Khối lượng Cu không hòa tan là
m = 10 - 5,6 = 4,4g
Đúng 0
Bình luận (0)
Cho 10g hỗn hợp gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng, thu được 2,24 lít khí H2 (đktc), dung dịch X và m gam kim loại không tan. Giá trị của m là A. 6,4. B. 3,4. C. 4,4. D. 5,6.
Đọc tiếp
Cho 10g hỗn hợp gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng, thu được 2,24 lít khí H2 (đktc), dung dịch X và m gam kim loại không tan. Giá trị của m là
A. 6,4.
B. 3,4.
C. 4,4.
D. 5,6.
Đáp án C
nFe = nH2 = 0,1 => mFe = 5,6g => mCu = 10 – 5,6 = 4,4g => Chọn C.
Đúng 0
Bình luận (0)
Cho 10g hỗn hợp gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng, thu được 2,24 lít khí H2 (đktc), dung dịch X và m gam kim loại không tan. Giá trị của m là A. 6,4 B. 3,4 C. 4,4 D. 5,6
Đọc tiếp
Cho 10g hỗn hợp gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng, thu được 2,24 lít khí H2 (đktc), dung dịch X và m gam kim loại không tan. Giá trị của m là
A. 6,4
B. 3,4
C. 4,4
D. 5,6
Đáp án C
nFe = nH2 = 0,1
mFe = 5,6g
mCu = 10 – 5,6 = 4,4g
Đúng 0
Bình luận (0)