đốt cháy 1kg than trong khí o2, biết than có 10% tạp chất không cháy tính:
- thể tích oxi(đktc) cần thiết để đốt cháy 1kg than trên
-khối lượng co2(đktc) sinh ra trong phản ứng trên
Đốt cháy 1kg than trong Không Khó O2 , biết trg than có 10% tạp chất không khí . Tính :
a)Thế tích oxi(đktc) cần thiết để đốt cháy 1kg than trên
Đổi 1kg = 1000g
mC = 1000 . (100% - 10%) = 900 (g)
nC = 900/12 = 75 (mol)
PTHH: C + O2 -> (t°) CO2
Mol: 75 ---> 75
VO2 = 75 . 22,4 . 5 = 8400 (l)
Đốt cháy 1 kg than trong khí oxi, biết trong than có 5% tạp chất không cháy. Tính thể tích oxi(đktc) cần thiết để đốt cháy 1kg than trên.
Lượng than nguyên chất:
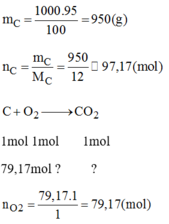
V O 2 = n O 2 .22,4 = 79,17.22,4 = 1773,4(l)
Hj mí chế :V t ms lập nik có vài câu hỏi Hóa nên nhờ mí chế giải giùm há
Đốt cháy 1kg than trong khí oxi bik trog than có 5% tạp chất ko cháy
a/ tính thể tích oxi (đktc) cần thiết để đốt cháy 1 kg than trên
b/Tính thể tích khí cacbonic trong p/ ứng trên
a/ trong 1 kg than có 5% tạp chất ko cháy => 95% khí cacbon cháy dc ( ko bik khoảng nì đúng ko >: mik ko chắc về cách trình bày chặng này bạn thông cảm )
=> Khối lượng cacbon có trong 1kg than:
\(1.95\%=0,95\)(kg) \(=950g\)
CTHH :\(C+O_2\rightarrow CO_2\)
1 : 1 : 1
475 : 475 : 475
\(n_c=\frac{m_c}{M_c}=\frac{950}{2}=475\left(mol\right)\)
\(n_{O_2}=\frac{475.1}{1}=475\left(mol\right)\)
\(V_{O_2}=n_{O_2}.22,4=475.22,4=10640\left(l\right)\)
B/ \(n_{CO_2}=\frac{475.1}{1}=475\left(mol\right)\)
\(V_{CO_2}=n_{CO_2}.22,4=475.22,4=10640\left(l\right)\)
Đốt cháy 1 cân than trong khí O2, biết than có 5% tạp chất không cháy.
a) Tính thể tích khí O2 (ở đktc cần thiết để đốt cháy 1 cân than)
b) Tính thể tích khí CO2.
mC = 1000.95% = 950 (g)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
Ta có: \(n_C=\dfrac{950}{12}=\dfrac{475}{6}\left(mol\right)\)
Theo PT: \(n_{O_2}=n_{CO_2}=n_C=\dfrac{475}{6}\left(mol\right)\)
a+b, \(V_{O_2}=V_{CO_2}=\dfrac{475}{6}.22,4\approx1773,33\left(l\right)\)
Đốt cháy 1 kg than trong khí oxi , biết trong than có 5 % tạp chất ko cháy.
a) Tính thể tích khí oxi (dktc) cần thiết để đốt cháy 1 kg than trên?
b) Tính thể tich khí cacbonic (dktc) sinh ra trong phản ứng ?
a)
n C = (1000 - 1000.5%)/12 = 475/6 mol
C + O2 --to--> CO2
n O2 = n C = 475/6 mol
=> V O2 = 22,4 . 475/6 = 1773,33(lít)
b) V CO2 = V O2 = 1773,33(lít)
Đốt cháy 1 kg than trong khí oxi, biết trong than có 5% tạp chất không cháy. Tính thể tích khí cacbonic (đktc) sinh ra trong phản ứng.
Lượng than nguyên chất:
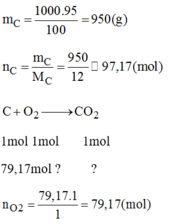
n C O 2 = n O 2 = 79,17(mol) → V C O 2 = V O 2 = 1773,4(l)
giúp em mấy câu này với ạ, em đang cần gấp. Em cảm ơn.
Câu 1: Đốt cháy hoàn toàn 2,5kg than đá có lẫn 16% tạp chất không cháy được
a/Tính thể tích khi oxi cần dùng(đktc)?
b/Tính khối lượng khí CO2 sinh ra sau phản ứng?
Câu 2:Đốt cháy hoàn toàn 18,6g photpho trong oxi
a/ tính thể tích oxi cần dùng(đktc)
b/Tính khối lượng sản phẩm?
c/Tính khối lượng KCLO3 cần dùng để điều chế được oxi nói trên?
Câu 3: Đốt cháy hoàn toàn a gam than đá có lẫn 25% tạp chất không cháy được thì cần dùng hết 9,52 m3(đktc)
a/ tính khối lượng khí co2 sinh ra?
b/tính a gam?
Bạn chia nhỏ câu hỏi ra được không:v, nhiều thế này mn ngại làm
Đốt cháy hoàn toàn 7,5 gam than đá có chứa 4% tạp chất không cháy. Thể tích khí oxi cần dùng (đktc) để đốt cháy hết lượng than đá trên là *
\(n_C=\dfrac{7,5.96\%}{12}=0,6\left(mol\right)\\ C+O_2-^{t^o}\rightarrow CO_2\\ n_{O_2}=n_C=0,6\left(mol\right)\\ \Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\)
giúp em mấy câu này với ạ, em đang cần gấp. Em cảm ơn.
Câu 1: Đốt cháy hoàn toàn 2,5kg than đá có lẫn 16% tạp chất không cháy được
a/Tính thể tích khi oxi cần dùng(đktc)?
b/Tính khối lượng khí CO2 sinh ra sau phản ứng?
Đổi 2,5kg = 2500g
mC = 2500 . (100% - 16%) = 2100 (g)
nC = 2100/12 = 175 (mol)
PTHH: C + O2 -> (t°) CO2
Mol: 175 ---> 175 ---> 175
VO2 = 175 . 22,4 = 3920 (l)
mCO2 = 44 . 175 = 7700 (g)
\(m_C=\dfrac{2,5.\left(100-16\right)}{100}=2,1kg\)
\(m_C=2,1kg=2100g\)
\(n_C=\dfrac{m_C}{M_C}=\dfrac{2100}{12}=175mol\)
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
175 175 175 ( mol )
\(V_{O_2}=n_{O_2}.22,4=175.22,4=3920l\)
\(m_{CO_2}=n_{CO_2}.M_{CO_2}=175.44=7700g\)
Phần trăm khối lượng cacbon có trong than đá:
\(100\%-16\%=84\%\)
Khối lượng cacbon:
\(m_C=\dfrac{2,5\cdot84\%}{100\%}=2,1kg\Rightarrow n_C=175mol\)
\(C+O_2\underrightarrow{t^o}CO_2\)
175 175 175
\(V_{O_2}=175\cdot22,4=3920ml=3,92l\)
\(m_{CO_2}=175\cdot44=7700g=7,7kg\)