Hoà tan hoàn toàn 1 kim loại M vào 200ml dung dịch HCL 1M. Tính thể tích khí thu được

Những câu hỏi liên quan
Hoà tan hoàn toàn 16.25gam kim loại M(chưa rõ hoá trị) vào dung dịch axit HCL. Khi phản ứng kết thúc thu được 5.6 lít khí hiđrô (ở đktc). a) Xác định kim loại M. b) Tính thể tích dung dịch HCL 0,2M cần dùng để hoà tan hết lượng kim loại này.
a) Gọi Kl cần tìm là X có hóa trị chưa biết là n
2X+ 2nHCl = 2XCln+ nH2
Có nH2=0,25 mol --> nX= 0,5/n mol ---> mX=0,5.MX/n=16,25 --> MX=32,5n
n=1 => MX=32,5( không có Kl nào tm)
n=2 => MX=65( Zn)
b) nHCl= 2nH2=2.0,25=0,5 mol
==> VddHCl cần = 0,5/0,2=2,5 lit
Đúng 0
Bình luận (0)
hòa tan hoàn toàn 19,5 gam một kim loại M ( M có hóa trị 2 trong hợp chất ) dung dịch HCl 1M dư thu được dung dịch A và 6,72 lít khí H2 (ở đktc )
a) xác định kim loại M.
b) đẻ trung hòa axits dư trong A cần 200ml dung dịch NaOH 1M. tính thể tích dung dịch HCl 1M đã dùng và nồng độ mol của dung dịch A ( coi thể tích dung dịch A bằng thể tích dung dịch HCl ban đầu )
nH2=\(\frac{6,72}{22,4}=0,3\)mol
PTHH
M+2HCl--> MCl2+H2
0,3mol<---------------0,3mol
=>MM=\(\frac{19,5}{0,3}=64\)
=> km loại là kẽm (Zn)
b) nNaOH=0,2.1=0,2 mol
PTHH
NaOH+HCl-->NaCl + H2O
0,2 mol--> 0,2 mol
---> thể tích HCl 1M đã dùng là V=\(\frac{0,2+0,3}{1}=0,5\)lít
=> CM(ZnCl2)=\(\frac{0,3}{0,5}=0,6M\)
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 19,2 gam hỗn hợp A gồm Fe và một kim loại R có hoá trị II vào dung dịch axit HCl (dư) thì thu được 8,96 lít khí (đo ở đktc). Mặt khác khi hoà tan hoàn toàn 9,2 gam kim loại R trong 1000 ml dung dịch HCl 1M thu được dung dịch B, cho quì tím vào dung dịch B thấy quì tím chuyển thành mau đỏ. Hãy xác định R và tính khối lượng của mỗi kim loại trong 19,2 gam
hỗn hợp A.
Tham khảo: https://hoidap247.com/cau-hoi/1175785
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 7,2g kim loại magie vào 300ml dung dịch HCl thu được V lít khí H2 ở đktc 1. Viết PTHH 2. Tính nồng độ mol dung dịch HCl đã dùng 3. Tính thể tích H2 sinh ra ở đktc
\(1,n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,3---->0,6------------------>0,3
\(2,C_{M\left(HCl\right)}=\dfrac{0,6}{0,3}=2M\\ 3,V_{H_2}=0,3.22,4=6,72\left(l\right)\)
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn 5,2 gam hỗn hợp gồm Mg và Fe bằng dung dịch HCl 1M thì thu được 3,36 lít khí H2 (đktc).
1) Tính thành phần phần trăm theo khối lượng mỗi kim loại có trong hỗn hợp.
2) Tính thể tích dung dịch HCl đã dùng.
\(1)n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ Mg+2HCl\to MgCl_2+H_2\\ Fe+2HCl\to FeCl_2+H_2\)
Từ giả thiết và theo PT:
\(\begin{cases} 24n_{Mg}+56n_{Fe}=5,2\\ n_{Mg}+n_{Fe}=0,15 \end{cases}\\ \Rightarrow n_{Mg}=0,1(mol);n_{Fe}=0,05(mol)\)
\(\Rightarrow \begin{cases} \%m_{Mg}=\dfrac{0,1.24}{5,2}.100\%=46,15\%\\ \%m_{Fe}=100-46,15=53,85\% \end{cases}\\ 2)\Sigma n_{HCl}=2n_{H_2}=0,3(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,3}{1}=0,3(l)=300(ml)\)
Đúng 3
Bình luận (1)
Hoà tan hoàn toàn 13g kẽm vào dung dịch Hcl loãng
a) tính thể tích khí hidro thu được ở dktc
B) 1 oxit kim loại R thì vừa đủ và thu được 0.1 mol kim loại. Tìm R và công thức hoá học .
Hoà tan hoàn toàn m gam hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt A. Thêm dần dần dung dịch HCl 1M vào dung dịch A nhận thấy khi bắt đầu thấy xuất hiện kết tủa thì thể tích dung dịch HCl 1M đã cho vào là 100ml còn khi cho vào 200ml hoặc 600ml dung dịch HCl 1M thì đều thu được a gam kết tủa. Tính m A. 17,64 B. 16,24 C. 20,48 D. 22,24
Đọc tiếp
Hoà tan hoàn toàn m gam hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt A. Thêm dần dần dung dịch HCl 1M vào dung dịch A nhận thấy khi bắt đầu thấy xuất hiện kết tủa thì thể tích dung dịch HCl 1M đã cho vào là 100ml còn khi cho vào 200ml hoặc 600ml dung dịch HCl 1M thì đều thu được a gam kết tủa. Tính m
A. 17,64
B. 16,24
C. 20,48
D. 22,24
Hoà tan hoàn toàn m gam hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt A. Thêm dần dần dung dịch HCl 1M vào dung dịch A nhận thấy khi bắt đầu thấy xuất hiện kết tủa thì thể tích dung dịch HCl 1M đã cho vào là 100ml còn khi cho vào 200ml hoặc 600ml dung dịch HCl 1M thì đều thu được a gam kết tủa. Tính a và m. A. a 7,8g; m 19,5g B. a 15,6g; m 19,5 C. a 7,8g; m 39g D. a 15,6g; m 27,7g
Đọc tiếp
Hoà tan hoàn toàn m gam hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt A. Thêm dần dần dung dịch HCl 1M vào dung dịch A nhận thấy khi bắt đầu thấy xuất hiện kết tủa thì thể tích dung dịch HCl 1M đã cho vào là 100ml còn khi cho vào 200ml hoặc 600ml dung dịch HCl 1M thì đều thu được a gam kết tủa. Tính a và m.
A. a = 7,8g; m = 19,5g
B. a = 15,6g; m = 19,5
a = 7,8g; m = 39g
D. a = 15,6g; m = 27,7g
Đáp án A
Khi cho hỗn họp gồm Na2O và A12O3 có phản ứng:
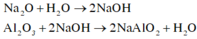
Vì sau một thời gian cho HCl vào dung dịch A mới xuất hiện kết tủa nên A gồm NaA1O2 và NaOH dư
Thứ tự các phản ứng xảy ra:
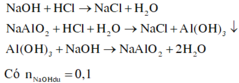
Vì khi cho 200ml hoặc 600ml dung dịch HCl 1M đều thu được a gam kết tủa nên khi cho 200ml dung dịch HCl thì chưa có sự hòa tan kết tủa và khi cho 600ml dung dịch HCl thì đã có sự hòa tan kết tủa.
Do đó:
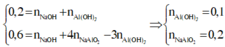
Áp dụng định luật bảo toàn nguyên tố cho Al và Na có
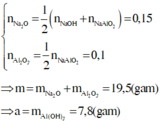
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 5,85 gam bột kim loại M vào dung dịch HCl, thu được 7,28 lít khí H 2 đktc. Kim loại M là
A. Mg
B. Al
C. Zn
D. Fe
Hoà tan hoàn toàn m gam hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt X. Thêm dần dần dung dịch HCl 1M vào dung dịch X nhận thấy khi bắt đầu thấy xuất hiện kết tủa thì thể tích dung dịch HCl 1M đã cho vào là 100ml còn khi cho vào 200ml hoặc 600ml dung dịch HCl 1M thì đều thu được a gam kết tủa. Giá trị của a và m lần lượt là A. a 7,8 ; m 19,5 B. a 15,6 ; m 19,5 C. a 7,8 ; m 39 D. a 15,6 ; m 27,7
Đọc tiếp
Hoà tan hoàn toàn m gam hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt X. Thêm dần dần dung dịch HCl 1M vào dung dịch X nhận thấy khi bắt đầu thấy xuất hiện kết tủa thì thể tích dung dịch HCl 1M đã cho vào là 100ml còn khi cho vào 200ml hoặc 600ml dung dịch HCl 1M thì đều thu được a gam kết tủa. Giá trị của a và m lần lượt là
A. a = 7,8 ; m = 19,5
B. a = 15,6 ; m = 19,5
C. a = 7,8 ; m = 39
D. a = 15,6 ; m = 27,7
Bắt đầu xuất hiện kết tủa n H C l = n N a O H ( d u ) = 0 , 1 S ố m o l H C l s a u k h i p h ả n ứ n g v ớ i N a O H n H C l ( 1 ) = 0 , 2 - 0 , 1 = 0 , 1 ; n H C l ( 2 ) = 0 , 6 - 0 , 1 = 0 , 5
Do khi cho vào 200ml hoặc 600ml HCl thì đều thu được cùng một lượng kết tủa nên ở TN1 kết tủa chưa tan, ở TN2 kết
tủa tan 1 phần
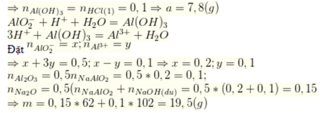
Đúng 0
Bình luận (0)




















