Đốt 1,26g bột sắt trong khí oxit thu đc 1,74g oxit sắt. Xác định công thức hóa học của oxit sắt

Những câu hỏi liên quan
Cho 1,5g một oxit sắt tác dụng vs khí video thu đc 1,05g sắt a.Viết pthh b.Tìm công thức hóa học của oxit sắt
a. \(Fe_2O_x+xH_2\rightarrow2Fe+xH_2O\)
b. \(n_{Fe}=\dfrac{m}{M}=\dfrac{1,05}{56}=0,01875\left(mol\right)\)
\(Fe_2O_x+xH_2\rightarrow2Fe+xH_2O\)
1 : 2
0,009375 : 0,01875
\(\Rightarrow M_{Fe_2O_x}=\dfrac{m}{n}=\dfrac{1,5}{0,009375}=160\) (g/mol)
\(\Rightarrow56.2+16x=160\)
\(\Rightarrow x=\dfrac{160-56.2}{16}=3\)
-Vậy CTHH của oxit sắt là Fe2O3
Đúng 1
Bình luận (2)
sắt (II) oxit hay sắt (III) oxit vậy bạn ???
Đúng 0
Bình luận (1)
Cho 1,5g một oxit sắt tác dụng vs khí video thu đc 1,05g sắt a.Viết pthh b.Tìm công thức hóa học của oxit sắt
a. \(Fe_xO_y+yH_2\rightarrow xFe+yH_2O\)
b. \(n_{Fe}=\dfrac{m}{M}=\dfrac{1,05}{56}=0,01875\)
\(Fe_xO_y+yH_2\rightarrow xFe+yH_2O\)
1 : x
\(\dfrac{0,01875}{x}\) : 0,01875
\(\Rightarrow M_{Fe_xO_y}=\dfrac{m}{n}=\dfrac{1,5}{\dfrac{0,01875}{x}}=80x\)
\(\Rightarrow56x+16y=80x\)
\(\Rightarrow16y=24x\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{16}{24}=\dfrac{2}{3}\)
\(\Rightarrow x=2;y=3\)
-Vậy CTHH của oxit sắt là Fe2O3
Đúng 2
Bình luận (0)
Câu 45: Đốt cháy kim loại sắt trong không khí thu được oxit sắt từ. Phương trình chữ của phản ứng hóa học là: A. Sắt + oxit sắt từ ® Khí oxi B. Sắt + khí oxi ® oxit sắt từ C. Khí oxi + oxit sắt từ ® Sắt D. oxit sắt từ ® Sắt + khí oxi giúp mik nha mn!! Huhu mik ngu Hóa quá mà
Đọc tiếp
Câu 45: Đốt cháy kim loại sắt trong không khí thu được oxit sắt từ. Phương trình chữ của phản ứng hóa học là:
A. Sắt + oxit sắt từ ® Khí oxi
B. Sắt + khí oxi ® oxit sắt từ
C. Khí oxi + oxit sắt từ ® Sắt
D. oxit sắt từ ® Sắt + khí oxi
giúp mik nha mn!! Huhu mik ngu Hóa quá mà
Đốt cháy hoàn toàn 19,2 g đồng?
a) tính thể tích oxi cần dùng (đktc)
b) cho kim loại sắt chưa rõ hóa trị vào lượng khí Oxi trên thu được 16 g oxit,xác định công thức hóa học của oxit
a, \(n_{Cu}=\dfrac{19,2}{64}=0,3\left(mol\right)\)
PT: \(2Cu+O_2\underrightarrow{t^o}2CuO\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Cu}=0,15\left(mol\right)\Rightarrow V_{O_2}=0,15.22,4=3,36\left(l\right)\)
b, Gọi CTHH của oxit là FexOy.
Có: nO (trong oxit) = 2nO2 = 0,3 (mol)
⇒ mFe = 16 - mO = 16 - 0,3.16 = 11,2 (g) \(\Rightarrow n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
⇒ x:y = 0,2:0,3 = 2:3
Vậy: CTHH cần tìm là Fe2O3.
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 2,24g Fe, thu được 3,2g oxit sắt. Xác định công thức phân tử của oxit sắt
Cách 1: PTHH tổng quát có dạng:
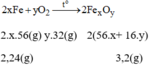
Theo PTHH trên, ta có tỉ lệ:
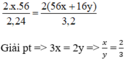
Vậy x = 2; y = 3.
Công thức hóa học của phân tử oxit sắt là F e 2 O 3
Cách 2: Khối lượng Oxi trong oxit là: 3,2 – 2,24 = 0,96 g
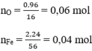
Tỉ lệ n F e : n O = 0,04 : 0,06 = 2:3
⇒ Trong 1 phân tử oxit có 2 nguyên tử Fe, 3 nguyên tử O ⇒ CT oxit là: F e 2 O 3
Đúng 0
Bình luận (0)
Khử hoàn toàn 12 gam bột một loại oxit sắt bằng khí CO dư, sau khi phản ứng kết thúc, toàn bộ khí thoát ra được dẫn vào dung dịch nước vôi trong dư thu được 22,5 gam kết tủa. Xác định công thức của oxit sắt
Xem chi tiết
Oxit sắt : FexOy
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CO_2} = n_{CaCO_3} =\dfrac{22,5}{100} = 0,225(mol)\\ Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2\\ n_{oxit} = \dfrac{n_{CO_2}}{y} = \dfrac{0,225}{y}(mol)\\ \Rightarrow \dfrac{0,225}{y}(56x + 16y) = 12\\ \Rightarrow \dfrac{x}{y} = \dfrac{2}{3}\)
Vậy CTHH của oxit : Fe2O3
Đúng 4
Bình luận (1)
Gọi oxit sắt là: FexOy.
PT: FexOy + yCO → xFe + yCO2 (1)
CO2 + Ca(OH)2 → CaCO3 + H2O (2)
Ta có: nCaCO3=22,5/100=0,225(mol)
Theo PT(2), ta có: nCO2=nCaCO3=0,225(mol)
Ta có: noxit sắt=0,225 . 1/y=0,225/y
=> (0,225/y)(56x + 16y)=12
Xét PT trên, ta có: x/y=2/3
=> x=2, y=3.
=> CTHH của oxit sắt là: Fe2O3.
Đúng 1
Bình luận (0)
Cho khí CO dư đi qua 13,92 gam một oxit sắt đã nung nóng, sau khi phản ứng thu được khí A và chất rắn B. Hòa tan hoàn toàn B trong dung dịch H2SO4 loãng dư, sau phản ứng hoàn toàn thu được 4,032 lít H2 (đktc). Xác định công thức hóa học của oxit sắt?
\(n_{H_2}=\dfrac{4,032}{22,4}=0,18\left(mol\right)\)
PTHH: Fe + H2SO4 ---> FeSO4 + H2
0,18 <------------------------ 0,18
\(\rightarrow n_O=\dfrac{13,92-0,18.56}{16}=0,24\left(mol\right)\)
CTHH: FexOy
=> x : y = 0,18 : 0,24 = 3 : 4
CTHH Fe3O4
Đúng 4
Bình luận (0)
Khử 23,2 gam một oxit sắt bằng CO , sau phản ứng thu được 16,8 (g) sắt
a) Tính thể tích khí CO2 thoát ra (đktc)
b) Xác định công thức hóa học của oxit ấy
Gọi số mol CO=mol CO2= a mol
Bảo toàn klg=>23,2+28a=44a+16,8
=>a=0,4 mol
=>VCO2=0,4.22,4=8,96 lit
Gọi CT oxit là Fe2On
Bảo toàn Fe: nFe tạo thành=nFe trong oxit ban đầu=16,8/56=0,3 mol
=>n oxit sắt=0,15 mol
=>M oxit sắt=23,2/0,15=464/3 =>n=8/3 CT oxit sắt là Fe3O4
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
a)Cho 0,3mol FexOy tham gia phản ứng nhiệt nhôm thấy tạo ra 0,4mol Al2O3. Xác định công thức oxit sắt?
b)Đốt cháy ko hoàn toàn 1 lượng sắt đã dùng hết 2,24 lít O2 ở đktc, thu đc hỗn hợp A gồm các oxit sắt và sắt dư. Khử hoàn toàn A bằng khí CO dư, khí đi ra sau pứ đc dãn vào bình đựng nước vôi trong dư. Tính khối lượng kết tủa thu đc






























