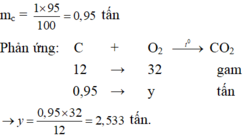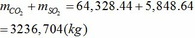Bài 3: Đốt cháy hoàn toàn 1 kg than chứa 90%C và 10% tạp chất không cháy được. Tính khối lượng không khí cần dùng với khối lượng cần dùng với khối lượng CO2 sinh ra trong phản ứng cháy này. Biết rằng VKK = 5. VO2
Bài 4: Đốt cháy 1 hỗn hợp gồm 2,7g bột Al cần 33,6 CO2 (đktc) và bột Mg. Hỏi khối lượng hỗn hợp trong mỗi loại ban đầu
Bài 5 : Cho khí A nhẹ hơn khi SO2 là 0,25 lần có thành phần phần trăm về khối lượng của các nguyên tố 75% C, 25% H . Xác định CTHH của A
b) Trộn 0,5 lít khí A với 1,5 lít khí O2 . Sau phản ứng, khí nào còn dư, dư bao nhiêu? Biết các khí ở cùng điều kiện , tỉ lệ về số mol bằng tỉ lệ thể tích PTHH: A+ O2 --------> CO2 + H2O