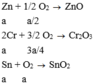trộn 190cm3 oxi với 120cm3 hh khí X gồm N2,H2,CH4. Đốt cháy hoàn toàn hh X, sau đó làm lạnh, thu được hh Y có thể tích là 110 cm^3. Cho Y qua dd NaOH dư, khí thoát ra có thể tích là 40cm^3. Thể tích mỗi khí trong hh X. Bk các khí đo ở cùng đktc

Những câu hỏi liên quan
hh khí X gồm 1 ankan, 1 anken, 1 ankin . tỉ khối của X so với H2 bằng 1. Dẫn 5,6 lít X qua dd AgNO3 dư trong NH3, thu được 7,35g kết tủa và còn lại hh khí Y có thể tích giảm 20% so với ban đầu. Đốt cháy hoàn toàn Y , thu được 6,72 lít CO2. Các thể tích khí đo ở đktc
Xác định CTCT của các chất trong X
tỉ khối là 13 chứ
nX = 0,25
n↓ = nAnkin = 0,25.20% = 0,05
=>M↓ = 147: C3H3Ag
->Ankin là C3H4 (0,05 mol)
nY = 0,2; nCO2 = 0,3
=>Số C = nCO2/nY = 1,5
Ankan là CH4
mY = mX – mC3H4 = 4,5
=>nH2O = \(\dfrac{4,5}{0,3.12}.\dfrac{1}{2}\) = 0,45
nCH4 = nH2O – nCO2 = 0,15 và nCxH2x = nY – nCH4 = 0,05
nCO2 = 0,15.1 + 0,05x = 0,3
=>x = 3
=> Anken là C3H6
Đúng 4
Bình luận (0)
cho 13,44 lít hh X gồm H2 và C2H2 có tỉ khối đối với N2 = 0,5. Mặc khác đốt cháy hoàn toàn 5,6g hh X có thành phần như trên trong bình kín chứa 28,8g O2. Phản ứng xong làm lạnh để ngưng tụ hết hơi nước thu được khí Y (thể tích tính ở đktc)
a) viết PTHH xảy ra
b) tính % theo thể tích và khối lượng của X
a) PTTH: \(2H_2+O_2\rightarrow2H_2O\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+H_2O\)
b) Ta có: \(\left\{{}\begin{matrix}\overline{M}_{hhkhí}=0,5\cdot28=14\\n_{hhkhí}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\end{matrix}\right.\)
Theo phương pháp đường chéo, ta có: \(\dfrac{n_{H_2}}{n_{C_2H_2}}=\dfrac{12}{12}=1\)
\(\Rightarrow n_{H_2}=n_{C_2H_2}=0,3\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,3}{0,6}\cdot100\%=50\%\\\%V_{C_2H_2}=50\%\\\%m_{H_2}=\dfrac{0,3\cdot2}{5,6}\cdot100\%\approx10,71\%\\\%m_{C_2H_4}=89,29\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
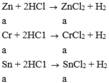
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là A. 2, 016 lít. B. 1,008 lít. C. 0,672 lít. D. 1,344 lít.
Đọc tiếp
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là
A. 2, 016 lít.
B. 1,008 lít.
C. 0,672 lít.
D. 1,344 lít.
Cho 11,424 lít (đktc) hỗn hợp khí X gồm H2 và hai h.c A,B mạch hở (B hơn A một ngtử cacbon) vào bình khí có sẵn bột Ni. Nung hỗn hợp X, sau một thời gian thu được hh Y gồm 6 h.c có tỉ khối hơi đối với H2 là 17,63a. Đốt cháy hoàn toàn hỗn hợp Y trong oxi dư thu được 14,112 lít (đktc) khí CO2 và 11,52 gam H2O. Xác định CTPT của 2 h.c A và B.b. HH Y làm mất màu tối đa V lít dd Br2 M và thoát ra 1,568 lít (đktc) hh khí Z. Tính V và tổng thể tích các khí A, B trong hh Y. Biết phản ứng xảy ra hoàn to...
Đọc tiếp
Cho 11,424 lít (đktc) hỗn hợp khí X gồm H2 và hai h.c A,B mạch hở (B hơn A một ngtử cacbon) vào bình khí có sẵn bột Ni. Nung hỗn hợp X, sau một thời gian thu được hh Y gồm 6 h.c có tỉ khối hơi đối với H2 là 17,63
a. Đốt cháy hoàn toàn hỗn hợp Y trong oxi dư thu được 14,112 lít (đktc) khí CO2 và 11,52 gam H2O. Xác định CTPT của 2 h.c A và B.
b. HH Y làm mất màu tối đa V lít dd Br2 M và thoát ra 1,568 lít (đktc) hh khí Z. Tính V và tổng thể tích các khí A, B trong hh Y. Biết phản ứng xảy ra hoàn toàn.
c. Viết các pt điều chế polietilen và etyl axetat từ chất A, các chất vô cơ cần thiết khác và đk xem như có đủ.
Hh khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hh X bằng một lượng oxi vừa đủ, thu được 550 ml hh Y gồm khí và hơi nước. Nếu cho Y đi qua dd axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân từ của hai hiđrocacbon là A. CH4 và C2H6. B. C2H4 và C3H6. C. C2H6 và C3H8. D. C3H6 và C4H8.
Đọc tiếp
Hh khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hh X bằng một lượng oxi vừa đủ, thu được 550 ml hh Y gồm khí và hơi nước. Nếu cho Y đi qua dd axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân từ của hai hiđrocacbon là
A. CH4 và C2H6.
B. C2H4 và C3H6.
C. C2H6 và C3H8.
D. C3H6 và C4H8.
Đáp án B
Khi các chất khí đo ở cùng điều kiện thì tỉ lệ mol cũng là tỉ lệ thể tích
TH1: Hai anken

TH2: Hai ankan
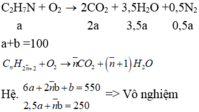
Đúng 0
Bình luận (0)
mọi người giúp em câu này với:chia hh X gồm 4 hidrocacbon(có thể là ankan, anken, ankin) thành 2 phần nhau.p1: cho qua dd br2 dư thấy có 64g br2 pư và thu đc hh khí Y thoát ra khỏi bình. đốt cháy hoàn toàn Y thu đc 22g co2 và 14.4g h2o.p2: đốt cháy hết p2 cần 49,28 lít O2 đktc và thu đc 28.8g h2o.a)tính khối lượng hh Xb) tính tỉ khối hơi của X với H2 (giúp em câu này với :) )c)tìm các hidrocacbon biết KL mol của mỗi hidrocacbon ko quá 50g/mol.
Đọc tiếp
mọi người giúp em câu này với:chia hh X gồm 4 hidrocacbon(có thể là ankan, anken, ankin) thành 2 phần = nhau.p1: cho qua dd br2 dư thấy có 64g br2 pư và thu đc hh khí Y thoát ra khỏi bình. đốt cháy hoàn toàn Y thu đc 22g co2 và 14.4g h2o.p2: đốt cháy hết p2 cần 49,28 lít O2 đktc và thu đc 28.8g h2o.a)tính khối lượng hh Xb) tính tỉ khối hơi của X với H2 (giúp em câu này với :) )c)tìm các hidrocacbon biết KL mol của mỗi hidrocacbon ko quá 50g/mol.
đốt cháy hoàn toàn 3,36 lít hh ch4 và c2h4 trong không khí , cần dùng 8,96 lít oxi a. tính thể tích mỗi hh b.khối lượng mỗi khí trong hỗn hợp c. nếu dẫn toàn bộ hh khí qua dd br2 1M . Tính Thể Tích dd br2 phản ứng
a, Ta có \(n_{CH_4}+n_{C_2H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\left(1\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Theo PT: \(n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,05\left(mol\right)\\n_{C_2H_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{CH_4}=0,05.22,4=1,12\left(l\right)\\V_{C_2H_4}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
b, \(m_{CH_4}=0,05.16=0,8\left(g\right)\)
c, \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}=0,1\left(mol\right)\Rightarrow V_{ddBr_2}=\dfrac{0,1}{1}=0,1\left(l\right)\)
\(m_{C_2H_4}=0,1.28=2,8\left(g\right)\)
Đúng 1
Bình luận (0)
Hỗn hợp khí Y gồm CO,CO2. Trộn Y với kk theo tỉ lệ thể tích 1 : 4, sau khi đốt cháy hết khí CO thì %V của khí N2 trong hh mới tăng 3,36% so với trước phản ứng.Tính %V các khí trong hh Y. Biết trong kk thì N2 chiếm 80% thể tích và còn lại là oxi. Các khí đo ở đktc
Hổn hợp X gồm propan, etilen, propin. Dẫn 2,24 lít hổn hợp X qua dd brom dư thấy có 20,8g brom phản ứng . Đốt cháy hoàn toàn khí thoát ra thu được 1,44 gam H2O. a. Viết các pthh xảy ra và tính phần trăm thể tích mỗi khí có trong hh X B. Dẫn 9,3 gam hh X qua dd AgNO3/ NH3 dư thu được bao nhiêu gam kết tủa