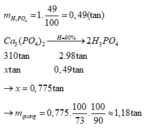Để điều chế 4,05 tấn nhôm cần bao nhiêu tấn nhôm oxit,biết hiệu suất qúa trình là 90%

Những câu hỏi liên quan
để có được 2,7 tấn nhôm nguyên chất cần bao nhiêu tấn quặng boxit chứa 80% nhôm oxit. Biết hiệu suất H của quá trình là 90%
2,7 tấn = 2700 kg
$n_{Al} = \dfrac{2700}{27} = 100(kmol)$
$\Rightarrow n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 50(kmol)$
$m_{Al_2O_3} = 50.102 = 5100(kg)$
$\Rightarrow m_{Al_2O_3\ đã\ dùng} = 5100 : 90\% = 5666,67(kg)$
$\Rightarrow m_{boxit} = 5666,67 : 80\% = 7083,3375(kg)$
Đúng 1
Bình luận (0)
Từ 1 tấn quặng boxit chứa 48,5% nhôm oxit sản xuất được bao nhiêu tấn nhôm . Biết hiệu suất quá trình là 90% .Nêu vai trò của criolit
Xem chi tiết
Khối lượng của Al2O3 trong 1 tấn quặng = 48,5%.1000 = 0,485 tấn
2Al2O3 (điện phân nóng chảy )--> 4Al + 3O2
=> mAl = \(\dfrac{0,485.4}{102.2}.27\)= 0,257 tấn
Do hiệu suất phản ứng là 90% => mAl thực tế thu được = 0,257.90% =0,231 tấn
vài trò criolit trong quá trình điện phân là tạo hỗn hợp có nhiệt độ nóng chảy thấp ; làm tăng độ dẫn điện ;tạo xỉ, ngăn nhôm nóng chảy bị oxi hóa trong không khí.
Đúng 0
Bình luận (0)
Một loại quặng boxit chứa 48,5% Al2O3. Từ 1 tấn quặng boxit nói trên có thể điều chế được bao nhiêu kilogam nhôm? (Biết hiệu suất của của quá trình điều chế là 90%)
Xem chi tiết
\(m_{Al_2O_3}=1\cdot48,5:100=0,485\left(tấn\right)\\\Rightarrow\dfrac{0,485}{102}=\dfrac{m_{Al\left(100\%\right)}}{27}\\ \Rightarrow m_{Al\left(100\%\right)}=0,128\left(tấn\right)\\ m_{Al\left(90\%\right)}=0,128\cdot90:100=0,1155\left(tấn\right)\)
Đúng 2
Bình luận (1)
Một loại quặng bôxit chứa 48,5% Al2O3. Từ 1 tấn quặng bôxit nói trên có thể điều chế được bao nhiêu kilôgam nhôm ? (Biết hiệu suất của quá trình điều chế là 90% ).
Giải thích từng bước giùm mik nha!!
\(m_{Al_2O_3}=1000000\cdot48,5\%=485000\left(g\right)\\ n_{Al_2O_3}=\dfrac{485000}{102}\approx4750\left(mol\right)\\ PTHH:2Al_2O_3\rightarrow4Al+3O_2\\ \Rightarrow n_{Al}=2n_{Al_2O_3}=9500\left(mol\right)\\ \Rightarrow m_{Al}=9500\cdot27=256500\left(g\right)=256,5\left(kg\right)\\ \Rightarrow m_{Al\left(\text{thực tế}\right)}=256,5\cdot90\%=230,85\left(kg\right)\)
Đúng 2
Bình luận (0)
Người ta dùng quặng boxit để sản xuất Al. Hàm lượng Al 2 O 3 trong quặng là 40%. Để có được 4 tấn nhôm nguyên chất cần bao nhiêu tấn quặng ? Biết rằng hiệu suất của quá trình sản xuất là 90%.
Thực tế do một số nguyên nhân, chất tham gia phản ứng không tác dụng hết, nghĩa là hiệu suất dưới 100%. Người ta có thể tính hiệu suất phản ứng như sau :
1. Dựa vào một trong các chất tham gia phản ứng, công thức tính :

2.Dựa vào một trong các chất tạo thành, công thức tính :
2 Al 2 O 3 → 4Al + 3 O 2
Dựa vào phương trình ta có: Cứ 204g Al 2 O 3 thì tạo ra 108g Al
⇒ Để tạo ra 4 tấn Al thì khối lượng Al 2 O 3 cần = 4.204/108 = 7,55g
Hiệu suất phản ứng là 90%, có nghĩa là 7,55 tấn Al 2 O 3 chỉ chiếm 90% khối lượng phải dùng.
Khối lượng oxit phải dùng : 7,55x100/90 = 8,39 tấn
Khối lượng quặng boxit: 8,39x100/40 = 20,972 tấn
Đúng 2
Bình luận (0)
bài 1: người ta dung quặng nhôm bôxit để sản xuất nhôm theo sơ đồ sau: 2Al2O3 4Al + 3O2 hàm lượng Al2O3 trong quặng bôxit là 40%. để có 4 tấn nhôm nguyên chất cần bao nhiêu tấn quặng. biết hiệu suất phản ứng của cả quá trình là 90%. bài 2: có thể bao nhiêu kg nhôm từ 1 tấn quặng bôxit chứa 95% nhôm, biết hiệu suấ phản ứng là 98%
Đọc tiếp
bài 1: người ta dung quặng nhôm bôxit để sản xuất nhôm theo sơ đồ sau:
2Al2O3 = 4Al + 3O2
hàm lượng Al2O3 trong quặng bôxit là 40%. để có 4 tấn nhôm nguyên chất cần bao nhiêu tấn quặng. biết hiệu suất phản ứng của cả quá trình là 90%.
bài 2: có thể bao nhiêu kg nhôm từ 1 tấn quặng bôxit chứa 95% nhôm, biết hiệu suấ phản ứng là 98%
2Al2O3--->4Al+3O2
ta có
cứ 204 tấn Al2O3_____108 tấn Al
--> 4 tấn AL cần 7,56 tấn Al2O3
vì hàm lượng quặng chỉ chứa 40% nên lượng quặng ban đầu là 18,9 tấn
H=90%
-->khối lượng quặng cần là 21 tấn
Đúng 0
Bình luận (3)
trong công nghiệpnguồn nguyên liệu sản xuất nhôm là quặng hematitcó chứa Al2o3 vnhóm được điều chế bằng cách điện phân nóng chảy Al203 với chất xúc tác trong bể điện phân thu được nhôm và khí ôxidưới 1 tấn quặng hematit (25% tạp chất)khi điều chế được bao nhiêu kilôgam rau biết hiệu suất chỉ đạt 90%
Từ quặng photphorit, có thể điều chế axit photphoric theo sơ đồ sau: Biết hiệu suất chung của cả quá trình là 90%. Để điều chế được 1 tấn dung dịch H3PO4 49%, cần bao nhiêu tấn quặng photphorit chứa 73% Ca3(PO4)2 về khối lượng? A. 1,32tấn B. 1,23tấn C. 1,81tấn D. 1,18tấn
Đọc tiếp
Từ quặng photphorit, có thể điều chế axit photphoric theo sơ đồ sau:
![]()
Biết hiệu suất chung của cả quá trình là 90%. Để điều chế được 1 tấn dung dịch H3PO4 49%, cần bao nhiêu tấn quặng photphorit chứa 73% Ca3(PO4)2 về khối lượng?
A. 1,32tấn
B. 1,23tấn
C. 1,81tấn
D. 1,18tấn
Tính khối lượng nhôm cacbua kỹ thuật (chứa 70%Al4C3; còn lại là tạp chất trơ) cần thiết để điều chế được 1 tấn metan. Biết hiệu suất đạt 80%
Ta có :
\(n_{CH_4} = \dfrac{1.1000.1000}{16} = 62500(mol)\)
Phương trình hóa học :
\(Al_4C_3 + 12H_2O \to 4Al(OH)_3 + 3CH_4\)
Theo PTHH :
\(n_{Al_4C_3\ phản\ ứng} = \dfrac{n_{CH_4}}{3} = \dfrac{62500}{3}\ mol\\ n_{Al_4C_3\ đã\ dùng} = \dfrac{\dfrac{62500}{3}}{80\%} = \dfrac{78125}{3}\ mol\)
\(\Rightarrow m_{Al_4C_3} = \dfrac{78125}{3}.144=3750000(gam)\\ \Rightarrow m_{nhôm\ cacbua\ kỹ\ thuật} = \dfrac{3750000}{70\%} = 5357142,9(gam)\)
Đúng 1
Bình luận (0)