Dẫn 10 lít hỗn hợp Co và SO2 qua dung dịch BA(OH)2 dư, sau pu thu đc 81,375g kết tủa.
Tính thành phần %theo thể tích mỗi khí trg hỗn hợp ban đầu.
Help me. Ai đó giúp tuôi đi. Bế tắc cả mấy tuần :vvvvvvvv
3. Dẫn 10 lít hỗn hợp khí CO và SO2 qua dung dịch Ba(OH)2 dư. Sau phản ứng thu được 81,375
gam kết tủa. Tính thành phần % theo thể tích mỗi khí trong hỗn hợp ban đầu? (Biết thể tích các
khí đo ở đktc).
![]()
![]()
nBaSO3 = \(\dfrac{81,375}{217}=0,375\left(mol\right)\)
Pt: SO2 + Ba(OH)2 --> BaSO3 + H2O
0,375 mol<------------0,375 mol
% VSO2 = \(\dfrac{0,375\times22,4}{10}.100\%=84\%\)
% VCO = 100% - 84% = 16%
Dẫn luồng khí CO dư đi qua 20,05 gam hỗn hợp hai oxit ZnO và F e 2 O 3 ở nhiệt độ cao, thu được hỗn hợp hai kim loại và khí C O 2 . Dẫn khí C O 2 sinh ra vào dung dịch C a ( O H ) 2 dư, thu được 35 gam kết tủa.
Viết phản ứng xảy ra.
Tính khối lượng mỗi kim loại tạo thành.
Tính thành phần phần trăm theo khối lượng mỗi oxit trong hỗn hợp ban đầu.
Bài 3: Đốt cháy hết 11,2 lít (đktc) hỗn hợp gồm Metan và Axetilen, cho sản phẩm qua dung dịch Ca(OH)2 dư thu được 80g kết tủa. Tính thành phần phần trăm thể tích mỗi chất khí trong hỗn hợp ban đầu.
\(n_{hh}=\dfrac{11,2}{22,4}=0,5mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_2}=y\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{80}{100}=0,8mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,8 0,8 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,5\\x+2y=0,8\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,2}{0,5}.100=40\%\)
\(\%V_{C_2H_2}=100\%-40\%=60\%\)
Gọi a (mol) và b (mol) lần lượt là số mol của khí metan (CH4) và khí axetilen (C2H2).
Giả thiết: a+b=11,2/22,4=0,5 (1).
Số mol kết tủa CaCO3 là 80/100=0,8 (mol) bằng số mol sản phẩm khí CO2 (do dung dịch Ca(OH)2 dư).
Ta có: a+2b=0,8 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra a=0,2 (mol) và b=0,3 (mol).
Thành phần phần trăm thể tích mỗi chất khí trong hỗn hợp ban đầu:
%Vmetan=0,2/0,5.100%=40%, suy ra %Vaxetilen=100%-40%=60%.
Có V lít hỗn hợp khí X gồm CO và H2. Chia hỗn hợp thành 2 phần bằng nhau. - Đốt cháy hoàn toàn phần thứ nhất bằng oxi. Sau đó dẫn sản phẩm đi qua dung dịch Ba(OH)2 (dư) thu được 39,4 gam kết tủa trắng. - Dẫn phần thứ 2 đi qua bột sắt (II) oxit nóng dư. Phản ứng xong thu được 16,8 gam kim loại sắt. a. Viết phương trình phản ứng xảy ra. b. Xác định V. Tính tỉ khối của hỗn hợp khí X.
P1:
\(n_{BaCO_3}=n_{CO_2}=\dfrac{39.4}{197}=0.2\left(mol\right)\)
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
\(\Rightarrow n_{CO}=n_{CO_2}=0.2\left(mol\right)\)
P2:
\(n_{Fe}=\dfrac{16.8}{56}=0.3\left(mol\right)\)
\(Fe_2O_3+3CO\underrightarrow{^{^{t^0}}}2Fe+3CO_2\)
\(...........0.2...\dfrac{2}{15}\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(..........0.25.0.3-\dfrac{2}{15}\)
\(V_{hh}=\left(0.2+0.25\right)\cdot2\cdot22.4=20.16\left(l\right)\)
Đề thiếu !
Dẫn 6,72 lit hỗn hợp khí X gồm propan, etilen và axetilen đi qua dung dịch brom dư, thấy còn 1,68 lít khí không hấp thụ. Nếu dẫn 6,72 lit hỗn hợp khí X trên qua dung dịch AgNO3/NH3 thấy có 24,24 gam kết tủa. Các thể tích khí đo ở đktc. Tính thành phần phần trăm theo thể tích và theo khối lượng của mỗi khí trong hỗn hợp.
1,68 lit khí không bị dung dịch Br2 hấp thụ là propan
![]()
![]()
![]()
![]()
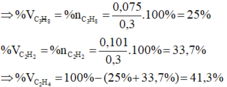
![]()
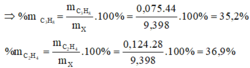
![]()
Đốt cháy 1,7g CO và CH4 trong bình chứa khí Oxi dư, dẫn sản phẩm cháy đi qua bình đựng Ca(OH)2 dư thu được 8g kết tủa. Tình thành phần % theo thể tích của mỗi khí trong hỗn hợp ban đầu và khối lượng của Ca(OH)2 đã tham gia phản ứng.
Cho 10 lít hỗn hợp khí N2 và CO2 (đktc) đi qua 2 lít dung dịch Ca(OH)2 0,02M thu được 1g kết tủa. Xác định thành phần % theo thể tích của CO2 trong hỗn hợp.
Số mol Ca(OH)2 = 2.0,02 = 0,04 mol
Số mol Ca(OH)2 = 2.0,02 = 0,04 mol
Số mol CaCO3 = 1_100=0,01 mol
Bài toán này có thể là 1 trong 2 trường hợp sau:
TH1: Số mol CO2 không đủ tác dụng với số mol Ca(OH)2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Số mol CO2 = số mol CaCO3 =0,01 mol
=>Thể tích CO2 = 22,4.0,01=0,224 lít
Vậy %thể tích CO2 = (0,224.100)/10=2,24%
TH2: Số mol CO2 nhiều hơn số mol Ca(OH)2 tham gia phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O (1)
CaCO3 + CO2 + H2O → Ca(HCO3)2 (2)
Theo (1): số mol CO2 (1) = số mol CaCO3 = Số mol Ca(OH)2 = 0,04 mol
Ta có: Số mol CaCO3 (2) = 0,04-0,01 = 0,03 (mol)
Theo (2): Số mol CO2(2) = số mol CaCO3 (2) = 0,03 (mol)
Vậy tổng số mol CO2 phản ứng (1) và (2) là 0,04 + 0,03 = 0,07 mol
Do đó %thể tích CO2 = (0,07.22,4.100)/10 = 15,68%
Cho 10 lít (đktc) hỗn hợp khí gồm N2 và CO2 tác dụng với 2 lít dung dịch Ca(OH)2 0,02 mol/l thu được 1 gam kết tủa. Thành phần % theo thể tích N2 trong hỗn hợp ban đầu là:
A. 2,24% hoặc 84,32%
B. 2,24% hoặc 15,68%
C. 15,68% hoặc 97,76%
D. 84,32% hoặc 97,76%
Đáp án D
Ta có nCa(OH)2= 2.0,02= 0,04 mol; nCaCO3= 1/100= 0,01 mol
Ta có nCa(OH)2 > nCaCO3 nên có 2 trường hợp:
- TH1: Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
Theo PT (1): nCaCO3= nCO2= 0,01 mol →VCO2=0,01.22,4=0,224 lít
→%VCO2= 2,24%→ %VN2= 100%- 2,24%=97,76%
- TH2: Ca(OH)2 phản ứng hết:
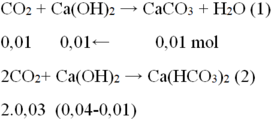
Ta có: nCO2= 0,01+ 2.0,03= 0,07 mol →VCO2= 0,07.22,4=1,568 lít
→%VCO2= 15,68%→ %VN2= 100%- 15,68%=84,32%