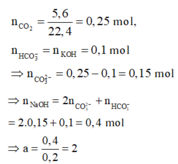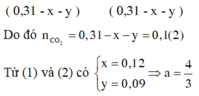dân 5,6 lít khí CO2 (đktc) vào bình chứa 200ml dung dịch NaOH nồng độ a M ; dung dịch thu được cso khả năng tác dụng tối đa 100ml dung dịch KOH 1M . Gía trị của a là ?

Những câu hỏi liên quan
Cho 5,6 lít CO2 (đktc) tan hết trong 200ml dung dịch NaOH nồng độ a M; dung dịch thu được có khả năng tác dụng tối đa 100 ml dung dịch KOH 1M. Giá trị của a là:
A. 0,75.
B. 1,5.
C. 2.
D. 2,5.
Cho 5,6 lít CO2 (đktc) tan hết trong 200ml dung dịch NaOH nồng độ a M; dung dịch thu được có khả năng tác dụng tối đa 100 ml dung dịch KOH 1M. Giá trị của a là:
A. 0,75
B. 1,5
C. 2
D. 2,5
Chọn đáp án C
Có n C O 2 = 5 , 6 22 , 4 = 0 , 25 m o l
n H C O 3 - = n K O H = 0 , 1 m o l
⇒ n C O 3 2 - = 0 , 25 - 0 , 1 = 0 , 15 m o l
⇒ n N a O H = 2 n C O 3 2 - + n H C O 3 - = 0 , 4 m o l
⇒ a = 0 , 4 0 , 2 = 2
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 2,24 lít khí CO2 (đktc) vào dung dịch X có chứa x mol Na2CO3 và y mol NaOH thu được dung dịch chứa 2 muối có cùng nồng độ mol. Mặt khác rót từ từ dung dịch có chứa 0,31 mol HCl vào hỗn hợp dung dịch X cũng thu được 2,24 lít khí CO2 (đktc). Đặt
a
x
y
, giá trị của a là A 4/3 B. 0,75 C. Đ/a khác D. 1
Đọc tiếp
Hấp thụ hoàn toàn 2,24 lít khí CO2 (đktc) vào dung dịch X có chứa x mol Na2CO3 và y mol NaOH thu được dung dịch chứa 2 muối có cùng nồng độ mol. Mặt khác rót từ từ dung dịch có chứa 0,31 mol HCl vào hỗn hợp dung dịch X cũng thu được 2,24 lít khí CO2 (đktc).
Đặt a = x y , giá trị của a là
A 4/3
B. 0,75
C. Đ/a khác
D. 1
Dẫn 2,24 lít khí co2 (đktc) đi qua bình chứa 200ml dung dịch Ba(OH)2 sản phẩm là Baco3 và H2O. Câu A . Viết phương trình hóa học. Câu B . Nồng độ mol của dd Ba(OH)2 đã dùng. ( Ba=137,C=12,O=16,H=1)
\(Ba\left(OH\right)_2+CO_2->BaCO_3+H_2O\)
0,1.................0,1
n CO2 = 2,24:22,4=0,1 mol
\(C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,1}{0,2}=0,5M\)
Đúng 2
Bình luận (0)
Sục 5,6 lít khí CO2 (đktc) vào 200ml dung dịch hỗn hợp NaOH 1M, Ba(OH)2 0,5M, KOH 0,5M. Kết thúc phản ứng thu được m gam kết tủa. Trị số của m là:
A. 49,25 gam
B. 21,7 gam
C. 54,25 gam
D. 19,7 gam
Đáp án D
Ta có: nCO2= 5,6/22,4=0,25 mol
nBa(OH)2= 0,2. 0,5= 0,1 mol;
nNaOH= 0,2.1= 0,2 mol;
nKOH= 0,2.0,5= 0,1 mol
nOH-= 0,1.2 + 0,2 + 0,1= 0,5 mol; nBa2+= 0,1 mol
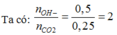
→ CO2 phản ứng với OH- theo PT sau:
CO2+ 2OH- → CO32-+ H2O (1)
0,25 0,5 0,25 mol
Ba2++ CO32- → BaCO3 (2)
Ta có 0,1 < 0,25 nên Ba2+ phản ứng hết
→ nBaCO3= nBa2+= 0,1 mol
→ mBaCO3= 0,1.197= 19,7 gam
Đúng 0
Bình luận (0)
Dẫn 5,6 lít khí CO2 (đktc) vào bình chứa 200ml dung dịch NaOH nồng độ a M ; dung dịch thu được có khả năng tác dụng tối đa 100ml dung dịch KOH 1M . Gía trị của a là ?
nCO2 = \(\dfrac{\text{5,6 }}{22,4}\) = 0,25 mol.
nNaOH = 0,2a mol.
nKOH = 0,1 mol.
Do pư tối đa nên sản phẩm phản ứng là muối cacbonat Na2CO3 và K2CO3
=> \(\dfrac{1}{2}\).(0,2a + 0,1) = 0,25 => a= 2
Đúng 1
Bình luận (0)
NaOH+CO2->Na2CO3(1)
Na2CO3+CO2+H2O->2NaHCO3(2)
2NaHCO3+2KOH->Na2CO3+K2CO3+2H2O(3)
nKOH=0.1mol
->nNaHCO3=0.1mol
->nNa2CO3=0.15mol
->nNaOH=0.15x2+0.1=0.4mol
a=0.4:0.2=2M
Đúng 1
Bình luận (0)
dd sau pư td đc với KOH => dd có chứa NaHCO3
2KOH+2NaHCO3 - > K2CO3 + Na2CO3+2H2O
0,1mol.....0,1mol
CO2+NaOH - > NaHCO3
0,1mol...0,1mol
nCO2=0,25
=> nCO2 pư tạo muối Na2CO3= 0,25-0,1 = 0,15.
CO2+2NaOH- > Na2CO3+H2O
0,15mol...0,3mol
=>nNaOH = 0,3 + 0,1 = 0,4 (mol)
=> a = \(\dfrac{0,4}{0,2}=2\left(M\right)\)
Đúng 1
Bình luận (0)
Sục 7,84 lít khí CO2 (đktc) vào 200 ml dung dịch NaOH 2M thu được 200 ml dung dịch X. Dung dịch Y chứa HCl 1M và H2SO4 x M. Cho từ từ đến hết 100 ml dung dịch Y vào 200 ml dung dịch X thu được 5,6 lít khí CO2 (đktc) và dung dịch Z. Cho BaCl2 dư vào dung dịch Z thu được m gam kết tủa. Giá trị của m là: A. 23,30 gam B. 43,00 gam C. 46,60 gam D. 34,95 gam
Đọc tiếp
Sục 7,84 lít khí CO2 (đktc) vào 200 ml dung dịch NaOH 2M thu được 200 ml dung dịch X. Dung dịch Y chứa HCl 1M và H2SO4 x M. Cho từ từ đến hết 100 ml dung dịch Y vào 200 ml dung dịch X thu được 5,6 lít khí CO2 (đktc) và dung dịch Z. Cho BaCl2 dư vào dung dịch Z thu được m gam kết tủa. Giá trị của m là:
A. 23,30 gam
B. 43,00 gam
C. 46,60 gam
D. 34,95 gam
Đáp án A
Ta có: n C O 2 = 0,35 mol; nNaOH = 0,2.2 = 0,4 mol
→ T = n N a O H n C O 2 = 0 , 4 0 , 35 = 1 , 14
→ Tạo 2 muối
CO2+ NaOH → NaHCO3
x x x mol
CO2+ 2NaOH →Na2CO3+ H2O
y 2y y mol
Ta có: n C O 2 = x+y = 0,35 mol; nNaOH = x+2y = 0,4 mol
→x = 0,3 và y = 0,05
Dung dịch X chứa 0,3 mol NaHCO3 và 0,05 mol Na2CO3
Trong 100 ml dung dịch Y có: nHCl = 0,1 mol; n H 2 S O 4 = 0,1x mol
→ n H + = 0,1+ 0,2x mol; n S O 4 2 - = 0,1x mol
Cho từ từ 100 ml dung dịch Y vào 200 ml dung dịch X thu được n C O 2 = 0,25 mol
H++ CO32- → HCO3-
0,05←0,05→ 0,05
H+ + HCO3- → CO2+ H2O
0,25 0,25← 0,25 mol
Ta có:
n H + = 0,05+ 0,25 = 0,1+ 0,2x → x = 1 mol/l
Dung dịch Z có chứa Na+ ; HCO3- ; SO42-: 0,1x = 0,1 mol
Ba2+ + SO42- → BaSO4 ↓
n B a S O 4 = n S O 4 2 - = 0,1 mol → m B a S O 4 = 0,1.233 = 23,3 gam
Đúng 0
Bình luận (0)
Dung dịch X là dung dịch Ba(OH)2 có nồng độ x mol/l. Hấp thụ hoàn toàn 2,464 lít khí CO2 (ở đktc) vào 200ml dung dịch X, thu được 3a gam kết tủa. Mặt khác, nếu hấp thụ hoàn toàn 3,136 lít khí CO2 (ở đktc) vào 200ml dung dịch X, thu được 2a gam kết tủa. Tính x
Ba(OH)2 + CO2 -> BaCO3 + H2O (1)
BaCO3 + CO2 + H2O -> Ba(HCO3)2 (2)
TN1: 2,464 lít CO2 (đktc) vào 200ml dung dịch X thì thu được 3a gam kết tủa.
TN2: 3,136 lít CO2 (đktc) vào 200ml dung dịch X thì thu được 2a gam kết tủa
=> Lượng CO2 ở TN2 tăng mà kết tủa lại giảm
*TN1: Chỉ xảy ra (1)
nCO2 = 0,11 mol
nBa(OH)2 = 0,2x mol
=> nBaCO3 (1) = 0,2 x mol
=> 3a = 0,2x . 197 = 39,2 x (I)
* TN2: Xảy ra cả (1)(2)
nCO2 = 0,14 mol
=> nCO2 (2) = 0,14 - 0,11 = 0,3 mol
=> nBaCO3 (2) = 0,3 mol
=> nBaCO3 còn lại = 0,2 x - 0,3 mol
=> 2a = (0,2 x - 0,3).197 = 39,2x - 59,1
=> 3a = (39,2x - 59,1). 1,5 = 58,8x - 88,65 (II)
Từ (I) và (II) => 39,2 x = 58,8x - 88,65
=> x = 4,5 M
Đúng 0
Bình luận (0)
Cho 5,6 lít khí CO2 ( đktc ) đi qua 164 ml dung dịch NaOH 20% ( D = 1,22g/ ml ) . Xác định nồng độ % của các chất trong dung dịch tạo thành.
\(n_{CO_2}=0,25(mol)\\ n_{NaOH}=\dfrac{164.1,22.20}{100.40}\approx1(mol)\\ T=\dfrac{1}{0,25}>2\\ \Rightarrow PTHH:CO_2+2NaOH\to Na_2CO_3+H_2O\\ n_{NaOH(p/ứ)}=0,5(mol);n_{Na_2CO_3}=0,25(mol)\\ \Rightarrow n_{NaOH(dư)}=0,5(mol);m_{CO_2}=0,25.44=11(g)\\ \Rightarrow \begin{cases} C\%_{Na_2CO_3}=\dfrac{0,25.106}{11+200}.100\%=12,56\%\\ C\%_{NaOH}=\dfrac{0,5.40}{11+200}.100\%=9,48\% \end{cases}\)
Đúng 1
Bình luận (0)