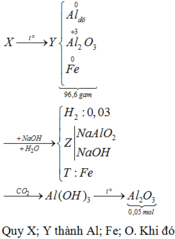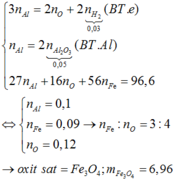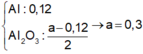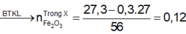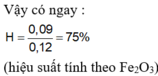Nung nóng 23,4 gam Fe(NO3)2 (trong điều kiện không có không khí) với hiệu suất phản ứng là 90%. Tính khối lượng chất rắn thu được sau phản ứng

Những câu hỏi liên quan
giúp mình với mọi người ơi .....
nung 13,17 g Cu(NO3)2 trong điều kiện không có không khí , sau phản ứng thu được 8,36 g chất rắn , tính hiệu suất phân hủy CU(NO3)2
Sửa đề : 13,17 → 13,16
Gọi \(n_{Cu(NO_3)_2\ pư} = a(mol)\)
\(2Cu(NO_3)_2 \xrightarrow{t^o} 2CuO + 4NO_2 + O_2\\ n_{CuO} = n_{Cu(NO_3)_2\ pư} = a(mol)\\ \Rightarrow m_{chất\ rắn\ sau\ pư} = m_{CuO} + m_{Cu(NO_3)_2\ dư}\\ \Rightarrow 8,36 = 80a + 13,16 - 188a\\ \Rightarrow a = \dfrac{2}{45}\\ H = \dfrac{\dfrac{2}{45}.188}{13,16}.100\% = 63,49\%\)
Đúng 1
Bình luận (1)
Hỗn hợp X gồm Al,
F
e
2
O
3
có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí (giả sử chỉ xảy ra phản ứng khử
F
e
2
O
3
thành Fe). Hòa tan hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít khí
H...
Đọc tiếp
Hỗn hợp X gồm Al, F e 2 O 3 có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí (giả sử chỉ xảy ra phản ứng khử F e 2 O 3 thành Fe). Hòa tan hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít khí H 2 (đktc) và 12,4 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là:
A. 45%
B. 50%
C. 71,43%
D. 75%
2Al + F e 2 O 3 → A l 2 O 3 + 2Fe
Sau phản ứng cho hỗn hợp rắn tác dụng với dd NaOH thấy có khí thoát ra, suy ra có Al dư.
Vậy hỗn hợp rắn: Fe, A l 2 O 3 , Al (dư) và F e 2 O 3 (nếu dư).
Theo định luật bảo toàn khối lượng, ta có:
m X = m r ắ n tan + m r ắ n k h ô n g tan
= 21,67 - 12,4 = 9,27g
Mà m r ắ n tan = m A l d u + m A l 2 O 3
2Al + 2NaOH + 2 H 2 O
→ 2 N a A l O 2 + 3 H 2 1
Theo PTHH (1), ta có:
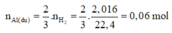
⇒ m A l d u = 0,06.27 = 1,62g
⇒ m A l 2 O 3 p u = m r a n tan - m A l d u
= 9,27-1,62=7,65 g
⇒ n A l 2 O 3 p u = 0,075mol
⇒ n A l p u = n F e s p = 2 n A l 2 O 3 p u
= 0,075.2 = 0,15 mol
Ta có:
m ran khong tan = mFe (sp) = mFe2O3(neu dư)
⇒ m F e 2 O 3 (neu dư)=12,4-0,15.56 = 4g
⇒ n F e 2 O 3 dư = 4/160 = 0,025 mol
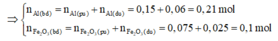
Giả sử phản ứng hoàn toàn thì Al sẽ dư → Tính hiệu suất phản ứng nhiệt nhôm theo F e 2 O 3 .
⇒ H = 0,075.100/0,1 = 75%
⇒ Chọn D.
Đúng 0
Bình luận (0)
Thực hiện phản ứng nhiệt nhôm (trong điều kiện không có không khí, hiệu suất 100%) với 9,66 gam hỗn hợp X gồm Al và một oxit sắt, thu được hỗn hợp rắn Y. Hòa tan Y bằng dung dịch NaOH dư, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Z, chất không tan T và 0,03 mol khí. Sục khí CO2 dư vào dung dịch Z, lọc lấy kết tủa nung đến khối lượng không đổi thu được 5,1 gam một chất rắn. Công thức oxit sắt và khối lượng của nó trong hỗn hợp X là A. Fe3O4 và 2,76 gam B. Fe3O4 và 6,96 gam C. FeO và...
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm (trong điều kiện không có không khí, hiệu suất 100%) với 9,66 gam hỗn hợp X gồm Al và một oxit sắt, thu được hỗn hợp rắn Y. Hòa tan Y bằng dung dịch NaOH dư, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Z, chất không tan T và 0,03 mol khí. Sục khí CO2 dư vào dung dịch Z, lọc lấy kết tủa nung đến khối lượng không đổi thu được 5,1 gam một chất rắn. Công thức oxit sắt và khối lượng của nó trong hỗn hợp X là
A. Fe3O4 và 2,76 gam
B. Fe3O4 và 6,96 gam
C. FeO và 7,20 gam
D. Fe2O3 và 8,00 gam
Một loại quặng A chứa 90% fe3o4, còn lại là tạp chất không tham gia phản ứng. Cho khí hidro qua m gam quặng A nung nóng thu được chất rắn B có khối lượng bằng 80% khối lượng quặng ban ban đầu. Tính hiệu suất phản ứngGIÚP MIK VỚI MN ƠI, MIK SẮP THI HU...
Xem chi tiết
Coi :
\(m_A = 232(gam)\\ \Rightarrow n_{Fe_3O_4} = 232.90\% : 232 = 0,9(mol)\\ \text{Gọi hiệu suất phản ứng là a}\Rightarrow n_{Fe_3O_4\ pư} = 0,9a(mol)\\ Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O\\ n_{Fe} = 0,9a.3 = 2,7a(mol)\\ n_{Fe_3O_4\ dư} = 0,9 - 0,9a(mol)\\ m_B = 2,7a.56 + (0,9 - 0,9a).232 = 232.80\%\\ \Rightarrow a = 0,4028 = 40,28\%\)
Đúng 1
Bình luận (0)
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 27,3 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hỗn hợp chất rắn sau phản ứng bằng dd NaOH dư thu được 4,032 lít H2 (đktc) và 14,88 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là: A. 60%. B. 80%. C. 75%. D. 71,43%.
Đọc tiếp
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 27,3 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hỗn hợp chất rắn sau phản ứng bằng dd NaOH dư thu được 4,032 lít H2 (đktc) và 14,88 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là:
A. 60%.
B. 80%.
C. 75%.
D. 71,43%.
Câu 7: 1. Khử 34,8g Fe3O4 bằng khí H2 dư. Tính khối lượng chất rắn thu được sau phản ứng biết hiệu suất của phản ứng đạt 90%.2. Nung 20g hỗn hợp Al, Mg, Zn trong không khí dư. Sau khi phản ứng kết thúc thu được 29,6g hỗn hợp chất rắn A. Cho A tác dụng với lượng dư H2SO4.a. Viết PTHH xảy rab. Tính khối lượng muối sunfat thu được sau phản ứngc. Nếu cho toàn bộ kim loại trên tác dụng với dung dịch HCl dư hãy tính thể tích khí H2 thu được ở đktc
Đọc tiếp
Câu 7:
1. Khử 34,8g Fe3O4 bằng khí H2 dư. Tính khối lượng chất rắn thu được sau phản ứng biết hiệu suất của phản ứng đạt 90%.
2. Nung 20g hỗn hợp Al, Mg, Zn trong không khí dư. Sau khi phản ứng kết thúc thu được 29,6g hỗn hợp chất rắn A. Cho A tác dụng với lượng dư H2SO4.
a. Viết PTHH xảy ra
b. Tính khối lượng muối sunfat thu được sau phản ứng
c. Nếu cho toàn bộ kim loại trên tác dụng với dung dịch HCl dư hãy tính thể tích khí H2 thu được ở đktc
\(n_{Fe_3O_4}=\dfrac{34,8}{232}=0,15\left(mol\right)\)
\(pthh:Fe_3O_4+H_2\underrightarrow{t^o}Fe+H_2O\)
0,15 0,15
=> \(m_{Fe}=\dfrac{90.0,15}{100}.56=7,56\left(g\right)\)
Đúng 0
Bình luận (0)
Câu 7 :
1) \(n_{Fe3O4}=\dfrac{34,8}{232}=0,15\left(mol\right)\)
Pt : \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O|\)
1 4 3 4
0,15 0,45
\(n_{Fe}=\dfrac{0,15.3}{1}=0,45\left(mol\right)\)
\(m_{Fe\left(Lt\right)}=0,45.56=25,2\left(g\right)\)
⇒ \(m_{Fe\left(tt\right)}=25,2.90\%=22,68\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Cho hỗn hợp Mg và Al có tỉ lệ mol 4 : 1 vào 200 ml dung dịch Cu(NO3)2 0,75M và Fe(NO3)3 1M. Sau phản ứng thu được dung dịch X và 14,08 gam hỗn hợp rắn Y. Cho NaOH dư vào X, lọc lấy kết tủa nung nóng trong không khí đến khối lượng không đổi thu được chất rắn có khối lượng là A. 19,20 gam B. 22,26 gam C. 36,00 gam D. 22,40 gam.
Đọc tiếp
Cho hỗn hợp Mg và Al có tỉ lệ mol 4 : 1 vào 200 ml dung dịch Cu(NO3)2 0,75M và Fe(NO3)3 1M. Sau phản ứng thu được dung dịch X và 14,08 gam hỗn hợp rắn Y. Cho NaOH dư vào X, lọc lấy kết tủa nung nóng trong không khí đến khối lượng không đổi thu được chất rắn có khối lượng là
A. 19,20 gam
B. 22,26 gam
C. 36,00 gam
D. 22,40 gam.
Chọn đáp án A
mCu tối đa = 0,2´0,75´64 = 9,6 gam và mFe tối đa = 0,2´56 = 11,2 gam
Vì 9,6 + 11,2 > 14,08 Þ Fe2+ dư, Mg và Al bị oxi hóa hết Þ nFe trong Y = (14,08 – 9,6)/56 = 0,08
Đặt nMg = 4a Þ nAl = a; BTE Þ 2´4a + 3a = 0,2 + 0,15´2 + 0,08´2 Þ a = 0,06
Þ Trong X chứa 0,24 mol Mg2+ + 0,06 mol Al3+ + 0,12 mol Fe2+
Þ Chất rắn sau cùng gồm: 0,24 mol MgO và 0,06 mol Fe2O3
Vậy mChất rắn = 0,24´40 + 0,06´160 = 19,2 gam
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít H2 (đktc) và 12,4 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là: A. 60% B. 71,43% C. 80% D. 75%
Đọc tiếp
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít H2 (đktc) và 12,4 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là:
A. 60%
B. 71,43%
C. 80%
D. 75%
Đáp án D
2 Al + Fe 2 O 3 → t o Al 2 O 3 + 2 Fe
Hỗn hợp sau phản ứng gồm A12O3, Fe, Al và Fe2O3.
Khi cho hỗn hợp vào dung dịch NaOH dư thì chỉ có Al và A12O3 tan, chất rắn còn lại gồm Fe và Fe2O3

Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al,
Fe
2
O
3
có khối lượng 40,1 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 4,032 lít
H
2
(đktc) và 27,68 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là: A. 80% B. 75% C. 60% D. 71,43%
Đọc tiếp
Hỗn hợp X gồm Al, Fe 2 O 3 có khối lượng 40,1 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 4,032 lít H 2 (đktc) và 27,68 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là:
A. 80%
B. 75%
C. 60%
D. 71,43%