Một oxit của phi kim X có tỉ khối hơi của X so với Hidro bằng 22. Tìm X và cho biết cấu tạo nguyên tử của X

Những câu hỏi liên quan
1.Một oxit (A) của ni tơ có tỉ khối hơi của A so với không khí là 1,59.Tìm công thức A
2.Một oxit của phi kim(X) có tỉ khối của(X) so với hiđro bằng 22.Tìm công thức(X)
Câu 1 :
Gọi công thức tổng quát của A là : \(N_xO_y\)
Ta có : \(d_{N_xO_y/kk}=1,59\)
\(\Rightarrow M_{N_xO_y}=1,59\times d_{kk}=1,59.29=46,11\)
Lại có : \(xN+yO=46,11=>14x+16y=46,11\)
Giả sử : \(\dfrac{14x}{46,11}=30,34\%=>x\approx1\)
y = \(\dfrac{46,11-14}{16}\approx2\)
Vậy A là : NO2
Đúng 1
Bình luận (1)
Gọi công thức của phi kim là \(A_xO_y\)
=> \(M_{A_xO_y}=22.2=44\left(đv.C\right)\)=> ( y = 1;2)
Với y = 1 => CTHH: \(A_2O\)
<=> \(2.A+16=44\Rightarrow A=14\left(đv.C\right)\)
<=> A là N; => CT oxit là N2O
Với y = 2 => CTHH: \(AO\)
<=> \(A+O=\Leftrightarrow A+16=44\Leftrightarrow A=28\left(loại\right)\)
Đúng 0
Bình luận (1)
Phân tử chất hữu cơ X có 2 nguyên tố C, H. Tỉ khối hơi của X so với hidro là 22. Công thức phân tử của X là A.
C
4
H
8
B.
C
3
H
8
C.
C
3
H
6
D.
C
6
H
6
Đọc tiếp
Phân tử chất hữu cơ X có 2 nguyên tố C, H. Tỉ khối hơi của X so với hidro là 22. Công thức phân tử của X là
A. C 4 H 8
B. C 3 H 8
C. C 3 H 6
D. C 6 H 6
Este X có tỉ khối hơi so với He bằng 22. Số đồng phân cấu tạo của X là
A. 5.
B. 2.
C. 4
D. 3
Chọn C
MX = 22.4 = 88 ⇒ X là C4H8O2
HCOO-CH2-CH2-CH3; HCOO-CH(CH3)2; CH3COOC2H5; C2H5COOCH3
Đúng 0
Bình luận (0)
Este X có tỉ khối hơi so với He bằng 22. Số đồng phân cấu tạo của X là
A. 5.
B. 2.
C. 4.
D.3
MX = 22.4 = 88
=> X là C4H8O2.
=> Chọn C
HCOO-CH2-CH2-CH3
HCOO-CH(CH3)2;
CH3COOC2H5;
C2H5COOCH3.
Đúng 0
Bình luận (0)
Este X có tỉ khối hơi so với He bằng 22. Số đồng phân cấu tạo của X là:
A. 4.
B. 3.
C. 5.
D. 2.
Chọn đáp án A
Ta có MEste = 22×4 = 88 ⇒ CTPT este là C4H8O2.
Đồng phân este của X gồm:
HCOOCH2CH2CH3 || HCOOCH(CH3)CH3.
CH3COOC2H5 || C2H5COOCH3
Vậy có tất cả 4 đồng phân este ứng với CTPT C4H8O2
Đúng 0
Bình luận (0)
Este X có tỉ khối hơi so với He bằng 22. Số đồng phân cấu tạo của X là
A. 5
B. 2
C. 4
D. 3
Đáp án : C
MX = 22.4 = 88g => Este X là C4H8O2
=> Các đồng phân cấu tạo :
HCOOCH2CH2CH3 ; HCOOCH(CH3)2; CH3COOC2H5 ; C2H5COOCH3
Đúng 0
Bình luận (0)
Hợp chất X no, mạch hở có phần trăm khối lượng C và H lần lượt bằng 66,67% và 11,11% còn lại là O. tỉ số hơi của X so với oxi bằng 2,25 -Tìm công thức phân tử của X -X không tác dụng với dung dịch AgNO3 trong NH3 nhưng khi tác dụng với hidro sinh ra X1. X1 tác dụng được với natri giải phóng hidro. Viết công thức cấu tạo va gọi tên của hợp chất X?
Đọc tiếp
Hợp chất X no, mạch hở có phần trăm khối lượng C và H lần lượt bằng 66,67% và 11,11% còn lại là O. tỉ số hơi của X so với oxi bằng 2,25
-Tìm công thức phân tử của X
-X không tác dụng với dung dịch AgNO3 trong NH3 nhưng khi tác dụng với hidro sinh ra X1. X1 tác dụng được với natri giải phóng hidro. Viết công thức cấu tạo va gọi tên của hợp chất X?
a) Ta có:
%O = 100% - %C - %H = 100% - 66,67% - 11,11% = 22,22%
⇒ MX = 2,25.32 = 72
Gọi công thức phân tử của X là CxHyOz
Ta có tỉ số:
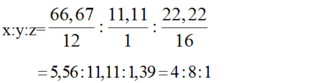
⇒ Công thức đơn giản nhất của X là C4H8O
Gọi công thức phân tử của X là (C4H8O)n
⇒ MX = (4.12 + 8 + 16)n = 72n = 72 ⇒ n = 1
⇒ Công thức phân tử của X là C4H8O
b) X không tác dụng được với dung dịch AgNO3 trong NH3, khi tác dụng với hiđro sinh ra X1, X1 tác dụng natri giải phóng hiđro ⇒ X là xeton
CTCT và tên gọi của X là:
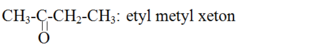
Đúng 0
Bình luận (0)
Nguyên tố R tạo một oxit RO2 (chất D) và một hợp chất RHn (chất E). Cho biết khối lượng riêng hơi của E ở dktc là 1,5179g/ml và phân tử khối của D là 32/17 phân tử khối của E.a) Tìm nguyên tố Rb) M là kim loại hóa trị I, tạo được muối X có công thức M2RO3. Hòa tan 12,6g X trong 100ml dd HCl lấy dư có D 1,2g/ml. Sau phản ứng thu được 126,2g dd. Tìm kim loại M
Đọc tiếp
Nguyên tố R tạo một oxit RO2 (chất D) và một hợp chất RHn (chất E). Cho biết khối lượng riêng hơi của E ở dktc là 1,5179g/ml và phân tử khối của D là 32/17 phân tử khối của E.
a) Tìm nguyên tố R
b) M là kim loại hóa trị I, tạo được muối X có công thức M2RO3. Hòa tan 12,6g X trong 100ml dd HCl lấy dư có D = 1,2g/ml. Sau phản ứng thu được 126,2g dd. Tìm kim loại M
a) MD = R + 32 (g/mol)
ME = R + n (g/mol)
Theo đề bài \(\dfrac{M_D}{M_E}\)= \(\dfrac{R+32}{R+n}\)= \(\dfrac{32}{17}\) => \(\left\{{}\begin{matrix}n=2\\R=32\end{matrix}\right.\) là giá trị thỏa mãn
Vậy R là lưu huỳnh (S)
b) m 100ml dung dịch HCl = 1,2.100 = 120 gam
M2SO3 + 2HCl → 2MCl + SO2↑ + H2O
m dung dịch sau phản ứng = m M2SO3 + m dung dịch HCl - m SO2 = 126,2 gam
=> 12,6 + 120 - 126,2 = mSO2
<=> mSO2 = 6,4 gam , nSO2 = 6,4 : 64 = 0,1 mol
Theo phương trình phản ứng , nM2SO3 = nSO2 = 0,1 mol
=> MM2SO3 = \(\dfrac{12,6}{0,1}\)= 126 (g/mol)
=> MM = (126 - 32 - 16.3) : 2 = 23 g/mol
Vậy M là natri (Na)
Đúng 3
Bình luận (2)
Bài 1 một nguyên tố r tạo hợp chất khí với hidro có công thức RH3 trong oxit bậc cao nhất của R nguyên tố chiếm 74,07% về khối lượngb xác định nguyên tố đóa So sánh tính phi kim của R với C (Z4) và O (Z6)Bài 2 a Viết cấu hình electron nguyên tử của các nguyên tố O (Z8) Xác định vị trí ( ô,chu kì, nhóm) của nguyên tố trong bảng hệ thống tuần hoàn các nguyên tố hóa họcb Viết công thức electron và công thức cấu tạo của các phân tử: HCL, N2Bài 3 a Viết cấu hình electron nguyên tử của các nguyên tố...
Đọc tiếp
Bài 1 một nguyên tố r tạo hợp chất khí với hidro có công thức RH3 trong oxit bậc cao nhất của R nguyên tố chiếm 74,07% về khối lượng
b xác định nguyên tố đó
a So sánh tính phi kim của R với C (Z=4) và O (Z=6)
Bài 2 a Viết cấu hình electron nguyên tử của các nguyên tố O (Z=8) Xác định vị trí ( ô,chu kì, nhóm) của nguyên tố trong bảng hệ thống tuần hoàn các nguyên tố hóa học
b Viết công thức electron và công thức cấu tạo của các phân tử: HCL, N2
Bài 3 a Viết cấu hình electron nguyên tử của các nguyên tố C (Z=6) Xác định vị trí ( ô,chu kì, nhóm) của nguyên tố trong bảng hệ thống tuần hoàn các nguyên tố hóa học
b Viết công thức electron và công thức cấu tạo của các phân tử: CO2, H2
Bài 4 Hợp chất oxit cao nhất có công thức là R2O5, trong hợp chất khí với hidro chứa 91,18% khối lượng R
a Xác định R. Viết CT hợp chất khí với hideo và CT oxi cao nhất (nếu có)
b So sánh tính phi kim của R với Si (Z=14) và S (Z=16)
Giúp em với ạ em cảm ơn!!!












