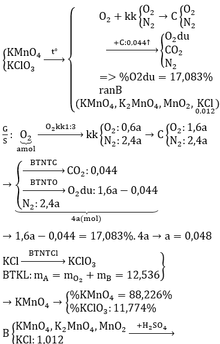
Đun nóng 98 g KClO3. Sau 1 thời gian thu được sau phản ứng là 88,4 g chất rắn. Tính thể tích O2 tạo thành ( ở đktc )
Tính thành phần phần trăm khối lượng của các chất trong chất rắn thu được sau phản ứng biết khi đun nóng KClO3 phân hủy theo cả 2 hướng sau :
KClO3 ------> KCl + O2 (1)
KClO3 -------> KCl + KClO4 (2)