Đốt cháy hoàn toàn 3,52 g hợp chất X, thu được 3,2 g sắt ( III ) oxit và 0,896 lít khí sunfurơ ( đktc ). Xác định công thức phân tử X, biết khối lượng mol của X là 88 g/mol

Những câu hỏi liên quan
Đốt cháy hoàn toàn 3,52g hỗn hợp X, thu được 3,2g sắt (III) oxit và 0,896lit khí sunfuro (đktc). Xác định công thức phân tử của X, biết khối lượng mol của X là 88g/mol.
\(=>nSO2=\dfrac{V\left(đktc\right)}{22,4}=\dfrac{0,896}{22,4}=0,04mol\)(khí sunfuro là SO2)
\(=>nS=nSO2=0,04mol=>mS=32.0,04=1,28g\)
\(=>nFe2O3=\dfrac{3,2}{160}=0,02mol=>nFe=2nFe2O3=0,04mol\)
\(=>mFe=2,24g\)
\(=>mS+mFe=2,24+1,28=3,52g=m\left(hh\right)\)
=>hỗn hợp X gồm Fe,S \(=>ct:FexOy\)
\(=>x:y=nFe:nS=0,04:0,04=1:1\)
=> ct thực nhiệm X là \(\left(FeS\right)a\)
theo bài ra \(=>\left(56+32\right)a=88=>a=1\)
=>ct phân tử của X là FeS
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 3,52g hỗn hợp X, thu được 3,2g sắt (III) oxit và 0,896lit khí sunfuro (đktc). Xác định công thức phân tử của X, biết khối lượng mol của X là 88g/mol.
Khi đốt cháy X thu được F e 2 O 3 và S O 2 nên trong X có Fe, S và có thể có O.
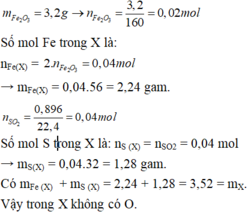
Gọi công thức phân tử hợp chất X có dạng F e x S y
Ta có tỉ lệ:
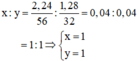
Công thức của hợp chất X là (FeS)n
M F e S n = 88 ⇔ (56 + 32)n = 88 ⇔ n = 1
Vậy công thức hóa học của phân tử X là FeS.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3.52g hợp chất X thu được 3.2g sắt oxit và 0.896l khí SO2(đktc). Xác định cong thức phân tử của X, biết khối lượng mol của X là 88.
Vì khi đốt cháy hợp chất X thu được sắt oxit và SO2 => các nguyên tố cấu tạo nên hợp chất là Fe và S
gọi CT cả X là 2FexSy --+O2---> xFe2Oy + 2ySO2 (1)
nFexOy= 3,52/88=0,04
theo (1) nSO2=2y/2 *nFexOy=0,896/22,4 => y=1
lại có 56x+32.y=88=>x=1
=> CTPT của X là FeS.
Đúng 0
Bình luận (2)
Đốt cháy hoàn toàn 3,2 g bột hiđrocacbon A thu được 4,48l khí CO2 (đktc) và 7,2g H2O. Biết rằng A có khối lượng mol là 16g. Xác định công thức phân tử của hiđrocacbon A.
Gọi CTPT của hiđrocacbon A là \(C_xH_y\)(\(x,y\) nguyên dương)
\(m_H=2\cdot\dfrac{7,2}{18}=0,8\left(g\right)\\ m_C=12\cdot\dfrac{4,48}{22,4}=2,4\left(g\right)\\ \Rightarrow\dfrac{12x}{2,4}=\dfrac{y}{0,8}=\dfrac{16}{3,2}\\ \Rightarrow x=1;y=4\)
Vậy CTPT của hiđrocacbon A là \(CH_4\)
Đúng 4
Bình luận (0)
đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ X thu được 11,2 lít CO2 và 10,8 gam nước. Biết rằng X có khối lượng mol là 72 (g/mol)
a) xác định công thức phân tử của X
b)viết tất cả các công thức cấu tạo có thể của X
a, \(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\Rightarrow n_H=0,6.2=1,2\left(mol\right)\)
Ta có: mC + mH = 0,5.12 + 1,2.1 = 7,2 (g)
→ X chỉ gồm C và H.
Gọi CTPT của X là CxHy.
⇒ x:y = 0,5:1,2 = 5:12
→ CTPT của X có dạng là (C5H12)n
Mà: MX = 72 (g/mol)
\(\Rightarrow n=\dfrac{72}{12.5+2.12}=1\)
Vậy: X là C5H12.
b, CTCT: CH3CH2CH2CH2CH3
CH3CH(CH3)CH2CH3
CH3C(CH3)2CH3
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 4,5g hợp chất hữu cơ X thu được 3,36 lít khí C02 ( đktc ) và 2,7g H2o
A. xác định công thức phân tử X , biết khối lượng mol của X là 60g
B. viết công thức cấu tạo của X biết X làm quỳ tím hóa đỏ
\(n_C=n_{CO_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(n_{H_2O}=\dfrac{2.7}{18}=0.15\left(mol\right)\Rightarrow n_H=0.15\cdot2=0.3\left(mol\right)\)
\(m_O=4.5-0.15\cdot12-0.3=2.4\left(g\right)\)
\(n_O=\dfrac{2.4}{16}=0.15\left(mol\right)\)
\(CT:C_xH_yO_z\)
\(x:y:z=0.15:0.3:0.15=1:2:1\)
\(CTnguyên:\left(CH_2O\right)_n\)
\(M_X=30n=60\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow n=2\)
\(CT:C_2H_4O_2\)
\(CTCT:\)
\(CH_3-COOH\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ X thu được 11,2 lít CO2 (đktc) và 10,8 gam nước. Biết rằng 7,2 gam X có số mol bằng số mol của 3,2 gam khí oxi.
a) Xác định công thức phân tử của X.
b) Viết tất cả các công thức cấu tạo có thể có của X.
Đọc tiếp
Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ X thu được 11,2 lít CO2 (đktc) và 10,8 gam nước. Biết rằng 7,2 gam X có số mol bằng số mol của 3,2 gam khí oxi.
a) Xác định công thức phân tử của X.
b) Viết tất cả các công thức cấu tạo có thể có của X.
\(n_C=n_{CO_2}=0,5\left(mol\right);n_H=2.n_{H_2O}=2.\dfrac{10,8}{18}=1,2\left(mol\right)\\ m_C+m_H=0,5.12+1,2.1=7,7,2\\ \Rightarrow X.ko.có.oxi\left(O\right)\\ \Rightarrow CTTQ:C_xH_y\left(x,y:nguyên,dương\right)\\ x:y=n_C:n_H=0,5:1,2=5:12\\a, \Rightarrow x=5;y=12\Rightarrow CTPT.X:C_5H_{12}\\ b,CH_3-CH_2-CH_2-CH_2-CH_3\\ CH_3-CH\left(CH_3\right)-CH_2-CH_3\\ CH_3-C\left(CH_3\right)_2-CH_3\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn a gam chất hữu cơ A cần phải dùng 13,44 lít khí Oxi ở (đktc)thu được 26,4 g CO2 và 10,8 g H2 a)Xác định công thức đơn giản nhất của A b)Xác định công thức phân tử của A biết 170g/mol < MA < 190g/mol
a)
nCO2 = 26,4 : 44 = 0,6 mol => nC = 0,6 mol
nH2O = 10,8 : 18 = 0,6 mol => nH = 1,2 mol
nO = 13,44 : 22,4 = 0,6 mol
nC : nH : nO = 0,6 : 1,2 : 0,6 = 1:2:1
=> Công thức đơn giản : (CH2O)n
b) Có 170 < MA < 190
=> 170 < 30n < 190
=> 30n = 180 => n = 6
=> Công thức phân tử : C6H12O6
Đúng 1
Bình luận (0)
\(a)n_C = n_{CO_2} = \dfrac{26,4}{44} =0,6(mol)\\ n_{H_2O} = \dfrac{10,8}{18} = 0,6(mol) \Rightarrow n_H = 0,6.2 = 1,2(mol)\\ n_{O_2} = \dfrac{13,44}{22,4} = 0,6(mol) \Rightarrow n_O = 0,6.2 + 0,6 - 0,6.2 = 0,6(mol)\\ n_C : n_H : n_O = 0,6 : 1,2 : 0,6 = 1 : 2 : 1\\ CTĐGN : CH_2O\\ b) CTPT : (CH_2O)_n\\ \Rightarrow 170 < (12 + 2 + 16)n < 190 \\ \Leftrightarrow 5,6 < n < 6,3 \Rightarrow n = 6\\ CTPT : C_6H_{12}O_6\)
Đúng 1
Bình luận (0)
Bài tập: Đốt cháy hoàn toàn 26,1l gam hợp chất hữu cơ A, sau phản ứng thu được 79,2 gam khí cacbonic và 40,5 gam hơi nước. Xác định công thức phân tử của A? Biết khối lượng mol của A là 58 g/mol.
\(n_{CO_2}=\dfrac{79,2}{44}=1,8\left(mol\right)\)
=> nC = 1,8 (mol)
\(n_{H_2O}=\dfrac{40,5}{18}=2,25\left(mol\right)\)
=> nH = 4,5 (mol)
Xét mC + mH = 1,8.12 + 4,5.1 = 26,1 (g)
=> A chứa C, H
nC : nH = 1,8 : 4,5 = 2 : 5
=> CTPT: (C2H5)n
Mà MA = 58 (g/mol)
=> n = 2
=> CTPT: C4H10
Đúng 3
Bình luận (2)


























