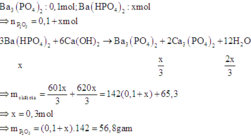cho 4,26 gam P2O5 tác dụng với 200 gam dung dịch Ba(OH)2 Cm=x thì thu được dung dịch x gồm 1 chất tan A và 4,55 gam kết tủa B. tính nồng độ C% của B trong dụng dịch sau phản ứng

Những câu hỏi liên quan
Hòa tan hoàn toàn một lượng AlCl3 và một lượng Al2(SO4)3 vào nước thu được 200 gam dung dịch X, chia dung dịch X thành hai phần: – Phần 1: cho tác dụng với BaCl2 dư thu được 13,98 gam kết tủa trắng. – Phần 2: cho tác dụng với 476 ml dung dịch Ba(OH)2 1M, sau khi phản ứng xong thu được 69,024 gam kết tủa. Biết khối lượng phần 2 gấp n lần khối lượng phần 1 (n là số nguyên dương) và lượng chất tan trong phần 2 nhiều hơn lượng chất tan trong phần 1 là 32,535 gam. Tính nồng độ phần trăm của các chất...
Đọc tiếp
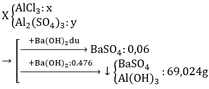
Hòa tan hoàn toàn một lượng AlCl3 và một lượng Al2(SO4)3 vào nước thu được 200 gam dung dịch X, chia dung dịch X thành hai phần:
– Phần 1: cho tác dụng với BaCl2 dư thu được 13,98 gam kết tủa trắng.
– Phần 2: cho tác dụng với 476 ml dung dịch Ba(OH)2 1M, sau khi phản ứng xong thu được 69,024 gam kết tủa. Biết khối lượng phần 2 gấp n lần khối lượng phần 1 (n là số nguyên dương) và lượng chất tan trong phần 2 nhiều hơn lượng chất tan trong phần 1 là 32,535 gam.
Tính nồng độ phần trăm của các chất có trong dung dịch X.
Cho Ba(OH)2 vào muối Al sẽ có 2TH sau:
TH1: kết tủa Al(OH)3 chưa bị hòa tan
Al3+ + 3OH– → Al(OH)3↓
→ nAl(OH)3 = nAl3+ → nAl(OH)3 = xn + 0,04n
TH2: kết tủa Al(OH)3 bị hòa tan một phần
Al3+ + 3OH– → Al(OH)3↓
(xn + 0,04n)→ 3(xn + 0,04n) (xn + 0,04n)
Al(OH)3 + OH– → AlO2– + 2H2O
0,952 – 3(xn + 0,04n) ←0,952
→ nAl(OH)3 = 4xn + 0,16n – 0,952

Đúng 0
Bình luận (0)
Cho m gam P2O5 phản ứng với dung dịch Ba(OH)2 thu được 60,1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với lượng vừa đủ với dung dịch Ca(OH)2 sau phản ứng thu được m + 65,3 gam chất rắn. Giá trị của m là A. 60,24 B. 56,8 C. 54,2 D. 51,6
Đọc tiếp
Cho m gam P2O5 phản ứng với dung dịch Ba(OH)2 thu được 60,1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với lượng vừa đủ với dung dịch Ca(OH)2 sau phản ứng thu được m + 65,3 gam chất rắn. Giá trị của m là
A. 60,24
B. 56,8
C. 54,2
D. 51,6
Bài 2. Cho 500 mL dung dịch X chứa FeCl3 và MgCl2 tác dụng vừa đủ với 200 mL dung dịch KOH 2,5M, sau phản ứng thu được 16,5 gam kết tủa. Tính nồng độ mol của các chất tan trong dung dịch X.
Gọi: \(\left\{{}\begin{matrix}n_{FeCl_3}=x\left(mol\right)\\n_{MgCl_2}=y\left(mol\right)\end{matrix}\right.\)
PT: \(FeCl_3+3KOH\rightarrow Fe\left(OH\right)_{3\downarrow}+3KCl\)
______x_________3x_________x (mol)
\(MgCl_2+2KOH\rightarrow Mg\left(OH\right)_{2\downarrow}+2KCl\)
____y_________2y_________y (mol)
Ta có: \(n_{KOH}=0,2.2,5=0,5\left(mol\right)\)
⇒ 3x + 2y = 0,5 (1)
m kết tủa = 16,5 ⇒ 107x + 58y = 16,5 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
\(\Rightarrow C_{M_{FeCl_3}}=C_{M_{MgCl_2}}=\dfrac{0,1}{0,5}=0,2\left(M\right)\)
Đúng 3
Bình luận (0)
\(FeCl_3+3KOH\rightarrow Fe\left(OH\right)_3\downarrow+3KCl\\ MgCl_2+2KOH\rightarrow Mg\left(OH\right)_2\downarrow+2KCl\)
\(n_{KOH}=0,2\cdot2,5=0,5\left(mol\right)\)
Đặt nFeCl₃ trong 500ml X là a mol, nMgCl₂ trong 500ml X là b mol
\(\Rightarrow\left\{{}\begin{matrix}3a+2b=0,5\\107a+58b=16,5\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
\(\Rightarrow C_MFeCl_3=\dfrac{0,1}{0,5}=0,2\left(M\right)\\ C_MMgCl_2=\dfrac{0,1}{0,5}=0,2\left(M\right)\)
Đúng 1
Bình luận (0)
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau: – Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn. – Phần 2: cho tác dụng với 200 ml dung...
Đọc tiếp
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau:
– Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn.
– Phần 2: cho tác dụng với 200 ml dung dịch CuSO4 1,5M. Sau khi kết thúc phản ứng tách bỏ chất rắn, cô cạn phần dung dịch thì thu được 46 gam muối khan.
a) Viết phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính phần trăm khối lượng các chất trong X.

Bảo toàn nguyên tố M: nMSO4 = 0,25mol
Bảo toàn nguyên tố Cu: nCuSO4 dư = 0,1 mol
=> M = 24 (Mg)
b.

Đúng 1
Bình luận (0)
Cho 300ml dung dịch H3PO4 1M tác dụng với 300ml dung dịch Ca(OH)2 1M, sau phản ứng thu được m gam muối kết tủa và dung dịch B. Tính khối lượng kết tủa và nồng độ chất có trong B?
\(n_{Ca\left(OH\right)_2}=0,3\left(mol\right)\\ n_{H_3PO_4}=0,3\left(mol\right)\\ Vì:\dfrac{n_{Ca\left(OH\right)_2}}{n_{H_3PO_4}}=\dfrac{0,3}{0,3}=1\\ \Rightarrow Tạo.1.muối:CaHPO_4\\ Ca\left(OH\right)_2+H_3PO_4\rightarrow CaHPO_4+2H_2O\\ m_{\downarrow}=0\\ n_{CaHPO_4}=n_{Ca\left(OH\right)_2}=0,3\left(mol\right)\\ C_{MddCaHPO_4}=\dfrac{0,3}{0,3+0,3}=0,5\left(M\right)\)
Đúng 3
Bình luận (0)
Giải giúp e vs ạ e cảm ơn
Bài 2: Cho 200ml dung dịch Na2CO3 1M tác dụng vừa đủ với 200 gam dung dịch Ba (OH) 2 . a. Viết PTHH xảy ra. b. Tính khối lượng chất kết tủa thu được. c. Tính nồng độ % của dung dịch Ba (OH) 2 dùng cho phản ứng trên.
a.
\(Na_2CO_3+Ba\left(OH\right)_2\rightarrow BaCO_3+2NaOH\)
b.
\(n_{BaCO_3}=n_{Na_2CO_3}=0,2.1=0,2\left(mol\right)\\ m_{kt}=197.0,2=39,4\left(g\right)\)
c.
\(n_{Ba\left(OH\right)_2}=n_{Na_2CO_3}=0,2\left(mol\right)\\ C\%_{Ba\left(OH\right)_2}=\dfrac{0,2.171.100\%}{200}=17,1\%\)
Đúng 3
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp gồm AlCl3 và Al2(SO4)3 vào nước thu được dung dịch X, chia dung dịch X thành 2 phần: - Phần 1 đem tác dụng với dung dịch BaCl2 dư thu được 13,98 gam kết tủa trắng. - Phần 2 đem tác dụng với 476 ml dung dịch Ba(OH)2 1M, sau phản ứng xong thu được 69,024g kết tủa.Biết khối lượng phần 2 gấp n lần phần 1 (n nguyên) và lượng chất tan trong phần 2 nhiều hơn trong phần 1 là 32,535 gam. Tính nồng độ C% của các chất tan có trong dung dịch X
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp gồm AlCl3 và Al2(SO4)3 vào nước thu được dung dịch X, chia dung dịch X thành 2 phần:
- Phần 1 đem tác dụng với dung dịch BaCl2 dư thu được 13,98 gam kết tủa trắng.
- Phần 2 đem tác dụng với 476 ml dung dịch Ba(OH)2 1M, sau phản ứng xong thu được 69,024g kết tủa.
Biết khối lượng phần 2 gấp n lần phần 1 (n nguyên) và lượng chất tan trong phần 2 nhiều hơn trong phần 1 là 32,535 gam. Tính nồng độ C% của các chất tan có trong dung dịch X
Sục 13,44 lít CO2 ( đktc) vào 200 ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M . Sau phản ứng thu được m1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với 200ml dung dịch BaCl2 1,2M; KOH 1,5M thu được m2 gam kết tủa. Giá trị của m2 là A. 47,28 gam B. 66,98 gam C. 39,4 gam D. 59,1 gam
Đọc tiếp
Sục 13,44 lít CO2 ( đktc) vào 200 ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M . Sau phản ứng thu được m1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với 200ml dung dịch BaCl2 1,2M; KOH 1,5M thu được m2 gam kết tủa. Giá trị của m2 là
A. 47,28 gam
B. 66,98 gam
C. 39,4 gam
D. 59,1 gam
Đáp án D
nOH- = 0.8 có nCO2 = 0,6< nOH- < 2nCO2 => tạo 2 muối CO2 + 2OH- → CO32- + H2O x -----> 2x -----> x CO2 + OH- → HCO3- y ------> y -----> y x + y = 0.6 và 2x + y = 0.8
=> x = 0,2 và y = 0,4 nCO32- = x = 0,2 < nBa2+ = 0,3
=> nBaCO3= 0.2 mol dd X: 0,1 mol Ba2+; 0,4 mol HCO3-; 0,2 mol Na+ nBaCl2 = 0,24 = nBa2+ => tổng nBa2+ = 0.34 nKOH = 0,3 = nOH- < nHCO3- => OH- hếtHCO3- + OH- → CO32- + H2O 0,3<-----0,3 -----> 0,3 nCO32- = 0,3; nBa2+ = 0,34
=> nBaCO3 = 0,3 => m2 = 0,3 . 197 = 59,1g
Đúng 0
Bình luận (0)
Sục 13,44 lít CO2 ( đktc) vào 200 ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M . Sau phản ứng thu được m1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với 200ml dung dịch BaCl2 1,2M; KOH 1,5M thu được m2 gam kết tủa. Giá trị của m2 là A. 47,28 gam B. 66,98 gam C. 39,4 gam D. 59,1 gam
Đọc tiếp
Sục 13,44 lít CO2 ( đktc) vào 200 ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M . Sau phản ứng thu được m1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với 200ml dung dịch BaCl2 1,2M; KOH 1,5M thu được m2 gam kết tủa. Giá trị của m2 là
A. 47,28 gam
B. 66,98 gam
C. 39,4 gam
D. 59,1 gam
Đáp án : D
,nCO2 = 0,6 mol ; nOH = 0,8 mol ; nBa2+ = 0,3 mol
=> nCO3 = 0,2 mol = nBaCO3 ; nHCO3- = 0,4 mol
,nBa2+ dư = 0,1 mol
Thêm nBaCl2 = 0,24 mol ; nKOH = 0,3 mol
=> nCO3 = nKOH = 0,3 mol = nBaCO3
=> mkết tủa = 59,1g
Đúng 0
Bình luận (0)