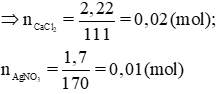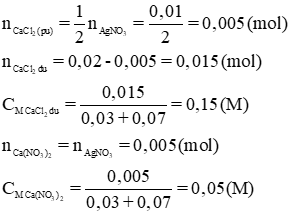Trộn 30ml dung dịch có chứa 1,11 g CaCl\(_2\) với 70 ml dung dịch có chứa 2,4g AgNO\(_3\).
a) Hãy cho biết hiện tượng quan sát được và viết phương trình hóa học.
b) Tính khối lượng chất rắn sinh ra.
c) Tính nồng độ mol của chất còn lại trong dung dịch sau phản ứng. Cho rằng thể tích của dung dịch thay đổi không đáng kể.