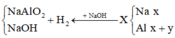
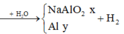Hỗn hợp X gồm Na và Al. Cho m gam X vào 1 lượng nước dư thì thoát ra V lít khí. Nếu cũng cho m gam X vào dd NaOH dư thì được 1,75V lít khí. Hãy tính thành phần % theo khối lượng của Na trong hỗn hợp

Những câu hỏi liên quan
Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dd NaOH (dư) thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là (biết các thể tích khí đo trong cùng điều kiện) A. 39,87% B. 29,87% C. 49,87% D. 77,31%
Đọc tiếp
Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dd NaOH (dư) thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là (biết các thể tích khí đo trong cùng điều kiện)
A. 39,87%
B. 29,87%
C. 49,87%
D. 77,31%
Ta thấy 1,75 lít > 1 lít
Chứng tỏ phần tác dụng với nước thì n Na = n NaOH không tác dụng hết n Al, còn phần sau là mới tác dụng hết
Na + H2O --> NaOH + 1/2.H2
x ---- ------ --------> x -----> x/2
Al + NaOH + H2O --> NaAlO2 + 3/2.H2
x <-----x ------------ ------- ------- ------- -> 3x/2
=> x/2 + 3x/2 = 1 <=> x = 0.5
Ta tính số mol do Al sinh ra là = 1.75 - 0.5/2 = 1,5 mol
Al + NaOH + H2O --> NaAlO2 + 3/2.H2
1 <---------- --------- ---------- ----------- 1,5 mol
% m Al = ( 1.27 ) / (1.27 + 0.5.23 ) x 100% = 70,13%
=> %Na = 29,87%
=> Đáp án B
Đúng 1
Bình luận (0)
Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH (dư) thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là A. 39,87% B. 29,87% C. 49,87% D. 77,31%
Đọc tiếp
Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH (dư) thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là
A. 39,87%
B. 29,87%
C. 49,87%
D. 77,31%
Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH dư thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là A. 39,87%. B. 77,31%. C. 29,87%. D. 49,87%.
Đọc tiếp
Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH dư thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là
A. 39,87%.
B. 77,31%.
C. 29,87%.
D. 49,87%.
Đáp án C
Gọi số mol của Na và Al trong hỗn hợp X lần lượt là x và y mol
Vì tỉ lệ thể tích cũng là tỉ lệ số mol => coi như thí nghiệm 1 thu được a mol khí và thí nghiệm 2 thu được 1,75a mol
Cho hỗn hợp X vào nước, Na phản ứng hết tạo NaOH và Al phản ứng với NaOH và còn dư => tính số mol theo NaOH
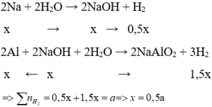
Cho hỗn hợp X tác dụng với dung dịch NaOH dư => Na phản ứng hết với H2O và Al phản ứng hết với NaOH
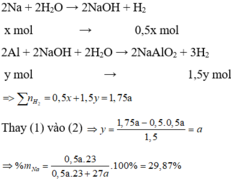
Đúng 0
Bình luận (0)
Đề như này: Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH dư thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X làĐáp án trả lời:Gọi số mol của Na và Al trong hỗn hợp X lần lượt là x và y molVì tỉ lệ thể tích cũng là tỉ lệ số mol coi như thí nghiệm 1 thu được a mol khí và thí nghiệm 2 thu được 1,75a molCho hỗn hợp X vào nước, Na phản ứng hết tạo NaOH và Al phản ứng với NaOH và còn dư tính số mo...
Đọc tiếp
Đề như này: Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH dư thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là
Đáp án trả lời:
Gọi số mol của Na và Al trong hỗn hợp X lần lượt là x và y mol
Vì tỉ lệ thể tích cũng là tỉ lệ số mol => coi như thí nghiệm 1 thu được a mol khí và thí nghiệm 2 thu được 1,75a mol
Cho hỗn hợp X vào nước, Na phản ứng hết tạo NaOH và Al phản ứng với NaOH và còn dư => tính số mol theo NaOH.
Thế cho em hỏi tại sao biết nhôm dư chứ không phải NaOH dư ạ. nếu hỗn hợp đó gồm 1 tấn Na và chỉ có 1g Al thì vẫn dư sao
Ta thấy ở trường hợp 2 cho m gam X vào dung dịch NaOH dư thì được 1,75V lít khí
Còn ở trường hợp 1 cho hỗn hợp X vào nước, Na phản ứng hết tạo NaOH và Al phản ứng với NaOH thì thoát ra V lít khí
=> Số mol H2 ở TH2 1,75V lít > Số mol H2 ở TH 1 V lít
Chứng tỏ phần tác dụng với nước thì nNa = nNaOH không tác dụng hết nAl, còn phần sau là mới tác dụng hết.
Đúng 0
Bình luận (0)
hỗn hợp X gồm Na và Al .Cho m gam X vào một lượng dư nước thì thoát ra V lít khí . Nếu cũng cho m gam X vào dd A .Cho dd A vào dd NaOH dư thì được 1,75 V lít khí .Thành phần % theo khối lg của Na trong X là ?
hỗn hợp X gồm Na và Al .Cho m gam X vào một lượng dư nước thì thoát ra V lít khí . Nếu cũng cho m gam X vào dd A .Cho dd A vào dd NaOH dư thì được 1,75 V lít khí .Thành phần % theo khối lg của Na trong X là ?
Ta thấy 1,75 lít > 1 lít
Chứng tỏ phần tác dụng với nước thì n Na = n NaOH không tác dụng hết n Al, còn phần sau là mới tác dụng hết
Na + H2O --> NaOH + 1/2.H2
x ---- ------ --------> x -----> x/2
Al + NaOH + H2O --> NaAlO2 + 3/2.H2
x <-----x ------------ ------- ------- ------- -> 3x/2
=> x/2 + 3x/2 = 1 <=> x = 0.5
Ta tính số mol do Al sinh ra là = 1.75 - 0.5/2 = 1,5 mol
Al + NaOH + H2O --> NaAlO2 + 3/2.H2
1 <---------- --------- ---------- ----------- 1,5 mol
% m Al = ( 1.27 ) / (1.27 + 0.5.23 ) x 100% = 70,13%
=> %Na = 29,87%
Đúng 2
Bình luận (1)
Câu 7 (ĐHKB – 2007): Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH dư thì được 1,75V lít khí, (biết thể tích các khí đo trong cùng điều kiện), thành phần phần trăm theo khối lượng của Na trong X là?
A. 39,87% B. 77,31% C. 49,87% D. 29,87%
Coi V = 22,4(lít)
Thí nghiệm 1 : $Al$ dư
$n_{H_2} = 1(mol)$
Gọi $n_{Na} = a(mol)$
$2Na + 2H_2O \to 2NaOH + H_2$
$2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
Theo PTHH :
$n_{H_2} = 0,5a + 1,5a = 1 \Rightarrow a = 0,5(mol)$
Thí nghiệm 2 : $Al$ hết
Gọi $n_{Al} = b(mol)$
Theo PTHH :
$n_{H_2} = \dfrac{1}{2}n_{Na} + \dfrac{3}{2}n_{Al}$
$\Rightarrow \dfrac{1}{2}.0,5 + \dfrac{3}{2}b = 1,75$
$\Rightarrow b = 1(mol)$
Ta có :
$\%m_{Na} = \dfrac{0,5.23}{0,5.23 + 1.27}.100\% = 29,87\%$
Đáp án D
Đúng 3
Bình luận (1)
Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thóat ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH (dư) thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là (biết các thể tích khí đo trong cùng điều kiện) A. 39,87% B. 29,87% C. 49,12% D. 77,31%
Đọc tiếp
Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thóat ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH (dư) thì được 1,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X là (biết các thể tích khí đo trong cùng điều kiện)
A. 39,87%
B. 29,87%
C. 49,12%
D. 77,31%
cho hỗn hợp x gồm Na và Al Cho m gam X tác dụng với một lượng H2O dư thì thoát ra V lít khí. Nếu cũng cho m gam X tác dụng với dd NaOH dư thu được 1,75V lít khí. Thành phần % theo khối lượng của Al trong hh X:
A 60,13% B 70,13% C 40,13% D 29,87%
Cho V lít = 1 lít ; số lít coi như là số mol cho dễ tính
Ta thấy 1,75 lít > 1 lít
Chứng tỏ phần tác dụng với nước thì n Na = n NaOH không tác dụng hết n Al
Còn phần sau là mới tác dụng hết
Na + H2O --> NaOH + 1/2.H2
x ---- ------ --------> x -----> x/2
Al + NaOH + H2O --> NaAlO2 + 3/2.H2
x <-----x ------------ ------- ------- ------- -> 3x/2
=> x/2 + 3x/2 = 1 <=> x = 0.5
Ta tính số mol do Al sinh ra là = 1.75 - 0.5/2 = 1,5 mol
Al + NaOH + H2O --> NaAlO2 + 3/2.H2
1 <---------- --------- ---------- ----------- 1,5 mol
% m Al = ( 1.27 ) / (1.27 + 0.5.23 ) x 100% = 70,13%
Đúng 0
Bình luận (0)
Hh X gồm Na và A1. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dd NaOH (dư) thì được 1 ,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X 1à (biết các thể tích khí đo trong cùng điều kiện, cho Na: 23, A1: 27) A. 39, 87% B. 73,1% C. 49, 87% D. 29,87%
Đọc tiếp
Hh X gồm Na và A1. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dd NaOH (dư) thì được 1 ,75V lít khí. Thành phần phần trăm theo khối lượng của Na trong X 1à (biết các thể tích khí đo trong cùng điều kiện, cho Na: 23, A1: 27)
A. 39, 87%
B. 73,1%
C. 49, 87%
D. 29,87%
Đáp án D
Do các khí đo ở cùng điều kiện nên ta “có thể” coi V như số mol để tính cho đơn giản.
TH1:
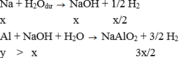
TH2:
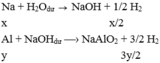
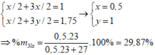
Đúng 1
Bình luận (0)