trong một ống nghiệm, người ta đã hòa tan 5g CuSO4.5H2O rồi thả vào đó một miếng kẽm. Có bao nhiêu gam đồng nguyên chất thoát ra sau phản ứng, biết rằng đã lấy thừa kẽm
Đun nóng một hỗn hợp gồm có 0,650 gam bột kẽm và 0,224 gam bột lưu huỳnh trong ống nghiệm đậy kín không có không khí.Sau phản ứng người ta thu được chất nào trong ống nghiệm ? Khối lượng là bao nhiêu ?
n Zn = 0,65/65 = 0,01 mol; n S = 0,224/32 = 0,007 mol
Zn + S → ZnS (1)
Theo (1) sau phản ứng trong ống nghiệm thu được:
n ZnS = 0,007 mol
m ZnS = 0,007x97 = 0,679 (g)
n Zn dư = (0,01 - 0,007) = 0,003 mol
m Zn dư = 65.0,003 = 0,195g
Có hai lá kẽm khối lượng như nhau. Một lá cho vào dung dịch đồng(II) nitrat, lá kia cho vào dung dịch chì(II) nitrat. Sau cùng một thời gian phản ứng, khối lượng lá kẽm thứ nhất giảm 0,05 gam. Khối lượng lá kẽm thứ 2 tăng hay giảm là bao nhiêu gam ? Biết rằng trong cả 2 phản ứng trên, khối lượng kẽm bị hoà tan bằng nhau.
n Zn = x
Theo đầu bài ta có : 65x - 64x = 0,05
=> x = 0,05 (mol) ; m Zn = 0,05 x 65 = 3,25 (gam).
Zn + Pb NO 3 2 → Zn NO 3 2 + Pb↓
0,05 mol 0,05 mol
Khối lượng lá kẽm thứ 2 tăng: ( 0,05 x 207) - 3,25 = 7,1 (gam).
Hòa tan hoàn toàn m gam kẽm cần vừa đủ 150g dung dịch HCl 14,6% thấy thoát ra V lít H2(đktc)a.Tính khối lượng kẽm đã phản ứng.b.Tính thể tích khí H2 đã thoát ra.c.Tính nồng độ % của dung dịch thu được sau phản ứng.
a, \(m_{HCl}=150.14,6\%=21,9\left(g\right)\Rightarrow n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{Zn}=n_{ZnCl_2}=n_{H_2}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,3.65=19,5\left(g\right)\)
b, \(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, Ta có: m dd sau pư = 19,5 + 150 - 0,3.2 = 168,9 (g)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{0,3.136}{168,9}.100\%\approx24,16\%\)
Đun nóng một hỗn hợp gồm có 0,650g bột kẽm và 0,224g bột lưu huỳnh trong ống nghiệm đậy kín không có không khí. Sau phản ứng, người ta thu được chất nào trong ống nghiệm? Khối lượng là bao nhiêu?
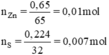
⇒ S phản ứng hết, Zn phản ứng dư
Phương trình hóa học của phản ứng
Zn + S 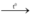 ZnS
ZnS
nZn phản ứng = 0,007 mol ⇒ nZnS = 0,007 mol.
Khối lượng các chất sau phản ứng:
mZn dư = (0,01 – 0,007) × 65 = 0,195g.
mZnS = 0,007 × 97 = 0,679g.
Cho một lá kẽm có khối lượng 8,5 gam vào dung dịch FeSO4, sau phản ứng lấy lá kẽm ra làm khô, cân được 7,6 gam (giả thiết toàn bộ sắt sinh ra bám hết vào lá kẽm). Lượng Zn đã phản ứng là
A. 13gam.
B. 3,25gam.
C. 6,5gam.
D. 8,7gam.
Đáp án C
Zn + Fe2+ → Zn2+ + Fe
Mol x → x
=> Dmgiảm = mZn pứ - mFe tạo ra
=> 8,5 – 7,6 = 65x – 56x => x = 0,1 mol
=> mZn pứ = 65.0,1 = 6,5g
Câu 1: hòa tan hoàn toàn một đọa kẽm trong ống nghiệm đựng dung dịch axit sunfuric , sau phản ứng thu đc kẽm sunfat và 2,24 lít khí A ( ở đktc )
a, Viết PTHH
b, Tính m của kẽm đã phản ứng
Câu 2: cho 11,2g sắt tác dụng vs dung dịch chứa 10,95g axit clohidric tạo ra sắt (II) clorua và khí hidro
a, Viết PTHH
b, Chất nào dư, m là bao nhiêu ?
c, Tính thể tích của khí hidro ở đktc
Câu 3: để hòa tan hoàn toàn 7g một kim loại hóa trị II cần dùng dung dịch axit chứa 9,125g , xác định tên của kim loại R trên
Câu 1 :
\(n_{H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(0.1.....................................0.1\)
\(m_{Zn}=0.1\cdot65=6.5\left(g\right)\)
Câu 2 :
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(n_{HCl}=\dfrac{10.95}{36.5}=0.3\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(1..............2\)
\(0.2...........0.3\)
\(LTL:\dfrac{0.2}{1}>\dfrac{0.3}{2}\Rightarrow Fedư\)
\(m_{Fe\left(dư\right)}=\left(0.2-0.15\right)\cdot56=2.8\left(g\right)\)
\(V_{H_2}=0.15\cdot22.4=3.36\left(l\right)\)
Câu 3 :
Axit HCl em nhé !
\(n_{HCl}=\dfrac{9.125}{36.5}=0.25\left(mol\right)\)
\(R+2HCl\rightarrow RCl_2+H_2\)
\(0.125..0.25\)
\(M_R=\dfrac{7}{0.125}=56\left(\dfrac{g}{mol}\right)\)
\(R:Fe\left(Sắt\right)\)
Hòa tan hoàn toàn 5,91 gam NaCl và KBr vào 100 ml dung dịch hỗn hợp Cu(NO3)2 0,1M và AgNO3 a mol/l, thu được 11,38 gam kết tủa. Cho miếng kẽm vào dung dịch Y, sau khi phản ứng xong lấy miếng kẽm ra khỏi dung dịch, thấy khối lượng miếng kẽm tăng 1,1225 gam. Giá trị của a là:
A. 0,85
B. 0,5
C. 0,775
D. 0,7
Đáp án A
Khi cho kẽm vào dung dịch Y, sau khi phản ứng xong thì thấy khối lượng thanh kẽm tăng nên trong Y phải có ion Ag+. Do AgNO3 dư nên đặt

1scvbandtqtfwwđ
hòa tan hoàn toàn 65 gam kẽm vào ống nghiệm chứa lượng dư axit clohidric (HCL). Sau phản ứng thu được dung dịch muối kẽm clorua (ZnCl2) và khí hidro ( ở dktc).
a viết pt hóa học của phản ứng xảy ra.(Ghi rõ điều kiện phản ứng nếu có)
b tính khối lượng muối thu được?
c tính thể tích Hidro sinh ra ở dktc.
help ;-;
\(a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.n_{Zn}=\dfrac{65}{65}=1\left(mol\right)\\ n_{ZnCl_2}=n_{Zn}=1\left(mol\right)\\ \Rightarrow m_{ZnCl_2}=1.136=136\left(g\right)\\ c.n_{H_2}=n_{Zn}=1\left(mol\right)\\ \Rightarrow V_{H_2}=1.22,4=22,4\left(l\right)\)