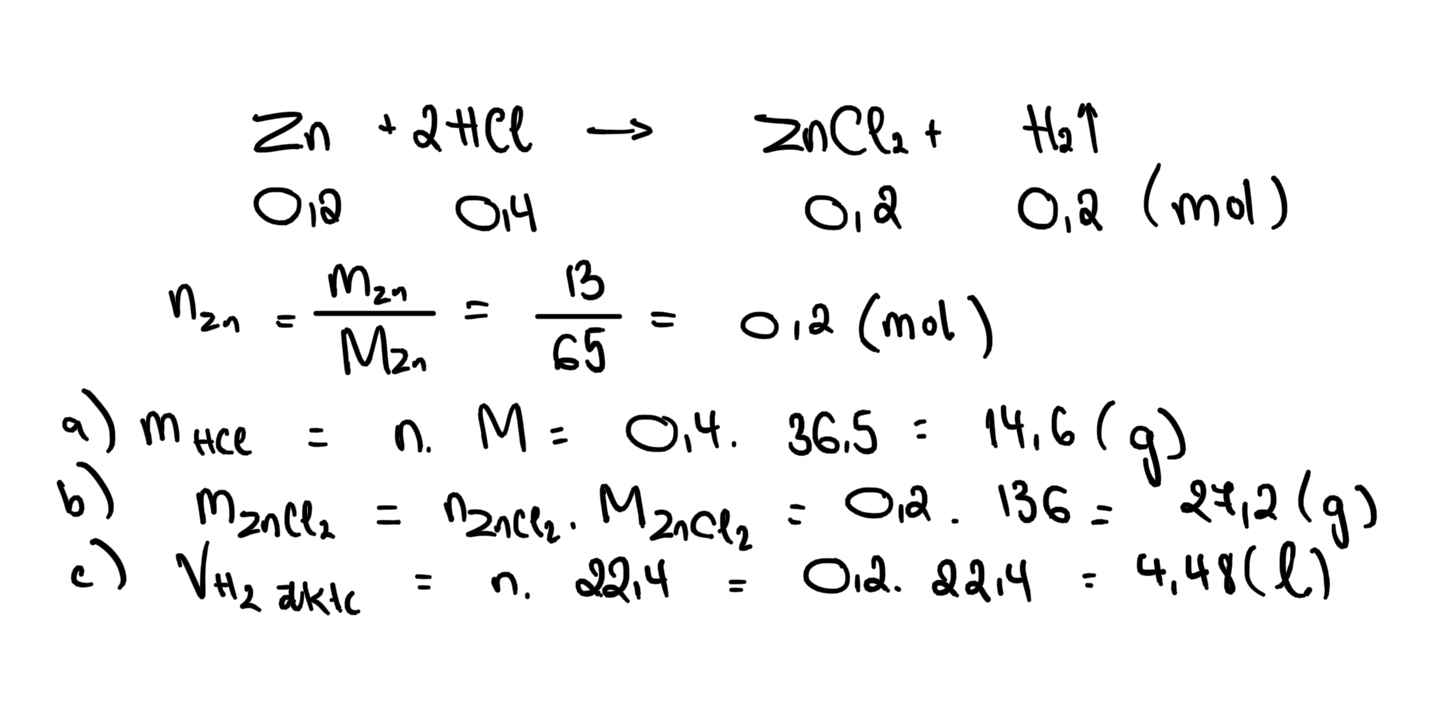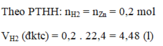Cho sơ đồ sau:
Zn + HCl -----> ZnCl2 + H2
a) Tính thể tích H2 sinh ra (đktc) khi cho 67,2g Zn vào dung dịch HCl
b) Khi cho 25,2g Fe tác dụng vs axit. Tính khối lượng HCl tham gia và thể tích H2 sinh ra (đktc)
c) Muốn thu 26,88l H2 (đktc) cần phải dùng khối lương HCl bao nhiêu?
GIÚP MK VS![]()