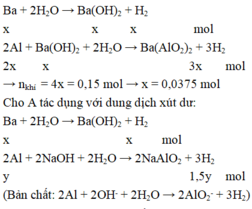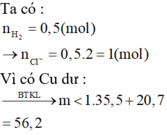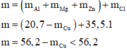A là hỗn hợp gồm Ba, Mg, Al
- Cho m(gam) A vào nước đến phản ứng xong thoát ra 8,96l khí H2 (đktc)
- Cho m(gam) A vào dd NaOH dư thoát ra 12,32l khí H2 (đktc)
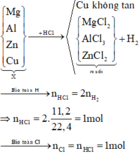
- Cho m(gam) A vào dd HCl dư thoát ra 13,44l khí H2 (đktc)
Tòm khối lượng và % theo khối lượng của mỗi kim loại trong A