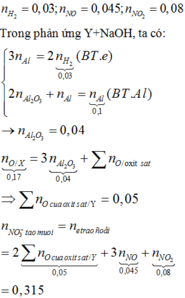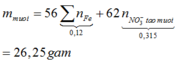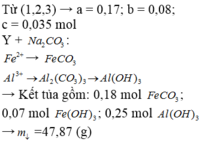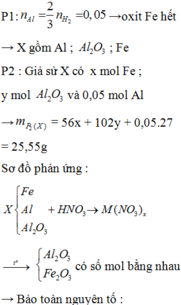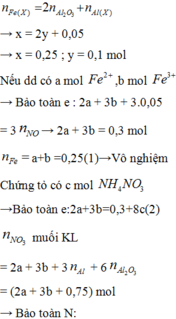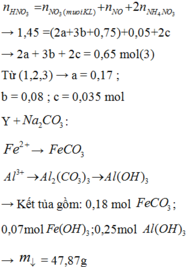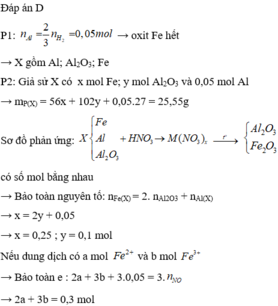Một loại đá chứa CaCO3 và MgCO3 được hòa tan hết bằng 400ml HNO3 thoát ra 6,72 dm3 khí CO2 (đktc). Sau phản ứng phải trung hòa lượng axit dư trong dung dịch bằng 100g dung dịch NaOH 8% rồi đem cô cạn thì nhận được 63g muối khan. Tính khối lượng mỗi chất ban đầu, viết công thức của đá và tính nồng độ mol dung dịch HNO3 đã dùng.

Những câu hỏi liên quan
1 loại đá chứa CaCO3 và MgCO3 hòa tan hết bằng 400 ml HNO3 thu 6.72 l CO2(ĐKTC). Cho dung dịch sau phản ứng tác dụng vừa đủ với 100 g NaOH 8 phần trăm để trung hòa dung dịch thu được rồi cô cạn được 63 g muối khan. Tính khối lượng mỗi chất, viết công thức của đá và CM HNO3
Gọi số mol MgCO3,CaCO3 là a,b
=> aCO3 + 2HNO3 → a(NO3)2 + H2O + CO2.
Lập hệ phương trình: \(\begin{cases}148a+164b=46\\a+b=0,3\end{cases}\) \(\Rightarrow\begin{cases}a=0,2\\b=0,1\end{cases}\)
Đúng 0
Bình luận (2)
goi x,y la so mol MgCO3,CaCO3. XCO3+2HNO3->X(NO3)2 + H2O + CO2.
tu tren suy ra he:148x+164y=46
x+y=0,3
suy ra x=0,2 ; y=0,1
=> ......
Đúng 0
Bình luận (2)
nCO2=\(\dfrac{6,72}{22,4}\)=0,3(mol),
mNaOH= C%. mdd= 8%.100=8g
nNaOH= \(\dfrac{m}{M}=\dfrac{8}{40}\) =0,2 mol
NaOH + HNO3 ------>NaNO3 + H2O
1 mol 1 mol 1 mol
0,2 mol 0,2 mol 0,2 mol
khối lượng của NaNO3 là mNaNO3=0,2 . 85 =17(g)
khối lượng của hỗn hợp muối Ca(NO3)2 và Mg(NO3)2 là:
63-17=46 (g)
Gọi nCa(NO3)2= a (mol) ,nMg(NO3)2= b (mol)
PTHH: CaCO3 + 2HNO3 --->Ca(NO3)2 + H2O + CO2 (1)
2mol 1 mol 1 mol
2a mol a mol a mol
MgCO3 + 2HNO3 ---->Mg(NO3)2 + H2O + CO2 (2)
2 mol 1mol 1 mol
2b mol b mol b mol
Ta cóhệ: a+b =0,3 (mol)
164a + 148b =46
=> a= 0,1 (mol) và b=0,2 (mol)
nHNO3 PƯ với CaCO3 và MgCO3 là
nHNO3 = 2.0,1 + 2.0,2 = 0,6 (mol)
=>nHNO3 trong 400 ml dd HNO3 là nHNO3=0,6+0,2=0,8 (mol)
CM HNO3 = \(\dfrac{0,8}{0,4}\) =2 M
Đúng 0
Bình luận (2)
Hòa tan hoàn toàn hỗn hợp Na2CO3 và K2CO3 bằng 400ml dung dịch HCl 1,5M thoát ra 5,6 lít khí CO2 đktc và dung dịch A.Trung hòa axit còn dư trong A bằng NaOH vừa đủ rồi cô cạn thì thu được 39,9g muối khan.Tìm % khối lượng hỗn hợp ban đầu
PTHH:
Na2CO3 + 2HCl -----> 2NaCl + H2O + CO2 (1)
K2CO3 + 2HCl -----> 2KCl + H2O + CO2 (2)
NaOH + HCl ----> NaCl + H2O (3)
Gọi n Na2CO3 = a , n K2CO3 = b (mol)
Theo pt(1)(2) tổng n CO2= a+b=\(\frac{5,6}{22,4}\)=0,25 (I)
n HCl = 1,5 . 0,4= 0,6 (mol)
Theo pt(1)(2) tổng n HCl pư=2 (a+b)=0,5 (mol)
==> n HCl dư= 0,1 mol
Theo pt(3) n NaCl= n HCl=0,1 mol ==> m NaCl=5,85 (g)
Theo pt(1)(2) n NaCl=2a ==> m NaCl= 117a
n KCl=2b ==> m KCl= 149b
===> 117a + 149b + 5,85 = 39,9
-----> 117a + 149b = 34,05 (II)
Từ (I)và (II) ==> a=0,1 và b=0,15
==>m hh = 0,1 . 106 + 0,15 . 138= 31,3(g)
m Na2CO3=10,6 (g)
%m Na2CO3 = \(\frac{10,6}{31,3}\) . 100%= 33,87%
%m K2CO3 = 10% - 33,87% = 66,13%
Đúng 0
Bình luận (1)
Hòa tan 3,2 gam oxit của một kim loại hóa trị x bằng 200 gam dung dịch H2SO4 loãng. Khi thêm vào hỗn hợp sau phản ứng một lượng CaCO3 vừa đủ thấy thoát ra 0,224 dm3 CO2 (đktc), sau đó cô cạn dung dịch thu được 9,36 gam muối khan. Xác định oxit kim loại trên và nồng độ % H2SO4 đã dùng.
Gọi CT oxit : \(R_2O_x\)
Ta có \(n_{R_2O_x}=\dfrac{3,2}{2R+16x}\left(mol\right)\)
PTHH: \(R_2O_x+xH_2SO_4\rightarrow R_2\left(SO_4\right)_x+xH_2O\) (1)
\(\dfrac{3,2}{2R+16x}\)---->\(\dfrac{3,2}{2R+16x}.x\)-->\(\dfrac{3,2}{2R+16x}\) (mol)
\(H_2SO_{4\left(dư\right)}+CaCO_3\rightarrow CaSO_4+CO_2+H_2O\) (2)
\(n_{CO_2}=\dfrac{0,244}{22,4}=0,01\left(mol\right)\)
Theo PT (2) : \(n_{CO_2}=n_{CaSO_4}=n_{H_2SO_4dư}=0,01\left(mol\right)\)
Ta có : \(m_{muối}=\text{}\dfrac{3,2}{2R+16x}.\left(2R+96x\right)+0,01.136=9,36\left(g\right)\)
\(\dfrac{3,2}{2R+16x}\).(2R+96x)=8
Lập bảng :
| x | 1 | 2 | 3 |
| R | 18,67 | 37,33 | 56 |
| Kết luận | Loại | Loại | Chọn (Fe) |
=> Oxit là Fe2O3
\(\Sigma n_{H_2SO_4}=0,02.3+0,01=0,07\left(mol\right)\)
=> \(C\%_{H_2SO_4}=\dfrac{0,07.98}{200}.100=3,43\%\)
Đúng 1
Bình luận (0)
Trộn 0,1 mol Al với 0,03 mol Fe2O3 và 0,02 mol Fe3O4 thu được hỗn hợp X. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong bình kín không có không khí, sau một thời gian đem hòa tan hỗn hợp Y thu được bằng dung dịch NaOH dư thấy thoát ra 0,672 lít khí H2 (đktc) và còn hỗn hợp rắn khôngtan Z. Đem hòa tan hết Z bằng dung dịch HNO3 đặc, đun nóng thu được dung dịch T và 2,8 lít (đktc) hỗn hợp hai khí NO và NO2 có tỉ khối so với H2 là 20,12. Cô cạn T thấy không có khí mùi khai thoát ra và thu được m gam...
Đọc tiếp
Trộn 0,1 mol Al với 0,03 mol Fe2O3 và 0,02 mol Fe3O4 thu được hỗn hợp X. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong bình kín không có không khí, sau một thời gian đem hòa tan hỗn hợp Y thu được bằng dung dịch NaOH dư thấy thoát ra 0,672 lít khí H2 (đktc) và còn hỗn hợp rắn không
tan Z. Đem hòa tan hết Z bằng dung dịch HNO3 đặc, đun nóng thu được dung dịch T và 2,8 lít (đktc) hỗn hợp hai khí NO và NO2 có tỉ khối so với H2 là 20,12. Cô cạn T thấy không có khí mùi khai thoát ra và thu được m gam rắn khan. Giá trị của m là
A. 26,25
B. 29,04
C. 24,39
D. 27,80
Nung 51,1 g hỗn hợp gồm FeO, Fe2O3, Fe3O4, Al đến khi phản ứng hoàn toàn được hỗn hợp X. Chia X thành 2 phần bằng nhau: Phần 1 cho tác dụng với dung dịch NaOH dư thu được 1,68 lít khí. Phần 2 hòa tan hết trong dung dịch chứa 1,45 mol HNO3 thu được dung dịch Y chỉ chứa muối tan và 3,36 lít NO thoát ra. Cô cạn Y, lấy chất rắn đem nung trong không khí đến khối lượng không đổi được 2 sản phẩm rắn có số mol bằng nhau. Các khí đều đo ở đktc. Nếu đem Y tác dụng với lượng dư dung dịch Na2CO3 thì thu...
Đọc tiếp
Nung 51,1 g hỗn hợp gồm FeO, Fe2O3, Fe3O4, Al đến khi phản ứng hoàn toàn được hỗn hợp X. Chia X thành 2 phần bằng nhau:
Phần 1 cho tác dụng với dung dịch NaOH dư thu được 1,68 lít khí.
Phần 2 hòa tan hết trong dung dịch chứa 1,45 mol HNO3 thu được dung dịch Y chỉ chứa muối tan và 3,36 lít NO thoát ra. Cô cạn Y, lấy chất rắn đem nung trong không khí đến khối lượng không đổi được 2 sản phẩm rắn có số mol bằng nhau.
Các khí đều đo ở đktc. Nếu đem Y tác dụng với lượng dư dung dịch Na2CO3 thì thu được bao nhiêu gam kết tủa
A. 58,25
B. 47,87
C. 46,25
D. 47,25
Nung 51,1 g hỗn hợp gồm FeO, Fe2O3, Fe3O4, Al đến khi phản ứng hoàn toàn được hỗn hợp X. Chia X thành 2 phần bằng nhau: Phần 1 cho tác dụng với dung dịch NaOH dư thu được 1,68 lít khí. Phần 2 hòa tan hết trong dung dịch chứa 1,45 mol HNO3 thu được dung dịch Y chỉ chứa muối tan và 3,36 lít NO thoát ra. Cô cạn Y, lấy chất rắn đem nung trong không khí đến khối lượng không đổi được 2 sản phẩm rắn có số mol bằng nhau. Các khí đều đo ở đktc. Nếu đem Y tác dụng với lượng dư dung dịch Na2CO3 thì thu...
Đọc tiếp
Nung 51,1 g hỗn hợp gồm FeO, Fe2O3, Fe3O4, Al đến khi phản ứng hoàn toàn được hỗn hợp X. Chia X thành 2 phần bằng nhau:
Phần 1 cho tác dụng với dung dịch NaOH dư thu được 1,68 lít khí.
Phần 2 hòa tan hết trong dung dịch chứa 1,45 mol HNO3 thu được dung dịch Y chỉ chứa muối tan và 3,36 lít NO thoát ra. Cô cạn Y, lấy chất rắn đem nung trong không khí đến khối lượng không đổi được 2 sản phẩm rắn có số mol bằng nhau.
Các khí đều đo ở đktc. Nếu đem Y tác dụng với lượng dư dung dịch Na2CO3 thì thu được bao nhiêu gam kết tủa
A. 58,25
B. 46,25
C. 47,25
D. 47,87
Nung 51,1 g hỗn hợp gồm FeO, Fe2O3, Fe3O4, Al đến khi phản ứng hoàn toàn được hỗn hợp X. Chia X thành 2 phần bằng nhau: Phần 1 cho tác dụng với dung dịch NaOH dư thu được 1,68 lít khí. Phần 2 hòa tan hết trong dung dịch chứa 1,45 mol HNO3 thu được dung dịch Y chỉ chứa muối tan và 3,36 lít NO thoát ra. Cô cạn Y, lấy chất rắn đem nung trong không khí đến khối lượng không đổi được 2 sản phẩm rắn có số mol bằng nhau. Các khí đều đo ở đktc. Nếu đem Y tác dụng với lượng dư dung dịch Na2CO3 thì thu...
Đọc tiếp
Nung 51,1 g hỗn hợp gồm FeO, Fe2O3, Fe3O4, Al đến khi phản ứng hoàn toàn được hỗn hợp X. Chia X thành 2 phần bằng nhau:
Phần 1 cho tác dụng với dung dịch NaOH dư thu được 1,68 lít khí.
Phần 2 hòa tan hết trong dung dịch chứa 1,45 mol HNO3 thu được dung dịch Y chỉ chứa muối tan và 3,36 lít NO thoát ra. Cô cạn Y, lấy chất rắn đem nung trong không khí đến khối lượng không đổi được 2 sản phẩm rắn có số mol bằng nhau.
Các khí đều đo ở đktc. Nếu đem Y tác dụng với lượng dư dung dịch Na2CO3 thì thu được bao nhiêu gam kết tủa
A. 58,25
B. 46,25
C. 47,25
D. 47,87
Nung 61,32 gam hỗn hợp rắn gồm Al và các oxit sắt trong khí trơ ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp X. Chia X thành 2 phần bằng nhau. - Phần một cho tác dụng với dung dịch NaOH dư thu được 2,016 lít khí (đktc). - Phần hai hòa tan hết trong dung dịch chứa 1,74 mol HNO3 thu được dung dịch Y chỉ chứa các muối và 4,032 lít NO (đktc) thoát ra. Cô cạn dung dịch Y, lấy rắn thu được đem nung ngoài không khí đến khối lượng không đổi thu được hai chất rắn có số mol bằng nhau....
Đọc tiếp
Nung 61,32 gam hỗn hợp rắn gồm Al và các oxit sắt trong khí trơ ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp X. Chia X thành 2 phần bằng nhau.
- Phần một cho tác dụng với dung dịch NaOH dư thu được 2,016 lít khí (đktc).
- Phần hai hòa tan hết trong dung dịch chứa 1,74 mol HNO3 thu được dung dịch Y chỉ chứa các muối và 4,032 lít NO (đktc) thoát ra. Cô cạn dung dịch Y, lấy rắn thu được đem nung ngoài không khí đến khối lượng không đổi thu được hai chất rắn có số mol bằng nhau. Nếu cho Y tác dụng với dung dịch Na2CO3 dư thì thu được a gam kết tủa.
Giá trị của a là
A. 58,20.
B. 50,40.
C. 57,93.
D. 50,91.
Đáp án A
Ta có khối lượng mỗi phần là 30,66 gam.
Cho phần một tác dụng với NaOH dư thu được 0,09 mol H2 do vậy trong X chứa Al dư.
Vậy trong mỗi phần chứa Fe, Al2O3 và Al dư 0,06 mol.
Cho phần 2 tác dụng với 1,74 mol HNO3 thu được 0,18 mol NO. Cô cạn dung dịch Y thu được các muối, nung rắn tới khối lượng không đổi thu được rắn chứa Al2O3 và Fe2O3 có số mol bằng nhau.
Gọi số mol của Fe, Al2O3 trong mỗi phần lần lượt là a, b
=> 56a+102b+0,06.27= 30,66
Và a= 2b+0,06
Giải hệ: a=0,3; b=0,12.
Gọi x là số mol NH4NO3 có thể tạo ra.
Bảo toàn N: n N O 3 - t r o n g m u o i K L = 1 , 74 - 0 , 18 - 2 x = 1 , 56 - 2 x
Bảo toàn e: 1,56-2x= 0,12.6+0,18.3+8x
Vậy NO3– trong muối là 1,5 mol.
Muối trong Y gồm Al(NO3)3 0,3 mol, Fe(NO3)2 0,3 mol và NH4NO3 0,03 mol.
Cho Y tác dụng với Na2CO3 dư thu được kết tủa là Al(OH)3 0,3 mol và FeCO3 0,3 mol.
=> a= 58,2 gam
Đúng 0
Bình luận (0)
Nung 61,32 gam hỗn hợp rắn gồm Al và các oxit sắt trong khí trơ ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp X. Chia X thành 2 phần bằng nhau. - Phần một cho tác dụng với dung dịch NaOH dư thu được 2,016 lít khí (đktc). - Phần hai hòa tan hết trong dung dịch chứa 1,74 mol HNO3 thu được dung dịch Y chỉ chứa các muối và 4,032 lít NO (đktc) thoát ra. Cô cạn dung dịch Y, lấy rắn thu được đem nung ngoài không khí đến khối lượng không đổi thu được hai chất rắn có số mol bằng nhau....
Đọc tiếp
Nung 61,32 gam hỗn hợp rắn gồm Al và các oxit sắt trong khí trơ ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp X. Chia X thành 2 phần bằng nhau.
- Phần một cho tác dụng với dung dịch NaOH dư thu được 2,016 lít khí (đktc).
- Phần hai hòa tan hết trong dung dịch chứa 1,74 mol HNO3 thu được dung dịch Y chỉ chứa các muối và 4,032 lít NO (đktc) thoát ra. Cô cạn dung dịch Y, lấy rắn thu được đem nung ngoài không khí đến khối lượng không đổi thu được hai chất rắn có số mol bằng nhau. Nếu cho Y tác dụng với dung dịch Na2CO3 dư thì thu được a gam kết tủa.
Giá trị của a là
A. 58,20
B. 50,40
C. 57,93
D. 50,91
Đáp án A
Ta có khối lượng mỗi phần là 30,66 gam.
Cho phần một tác dụng với NaOH dư thu được 0,09 mol H2 do vậy trong X chứa Al dư.
Vậy trong mỗi phần chứa Fe, Al2O3 và Al dư 0,06 mol.
Cho phần 2 tác dụng với 1,74 mol HNO3 thu được 0,18 mol NO. Cô cạn dung dịch Y thu được các muối, nung rắn tới khối lượng không đổi thu được rắn chứa Al2O3 và Fe2O3 có số mol bằng nhau.
Gọi số mol của Fe, Al2O3 trong mỗi phần lần lượt là a, b
![]()
Và a=2b+0,06
Giải hệ: a=0,3; b=0,12.
Gọi x là số mol NH4NO3 có thể tạo ra.
Bảo toàn N:
n N O 3 - t r o n g m u o i K l = 1 , 74 - 0 , 18 - 2 x = 1 , 56 - 2 x
Bảo toàn e: 1 , 56 - 2 x = 0 , 12 . 6 + 0 , 18 . 3 + 8 x
Vậy NO3– trong muối là 1,5 mol.
Muối trong Y gồm Al(NO3)3 0,3 mol, Fe(NO3)2 0,3 mol và NH4NO3 0,03 mol.
Cho Y tác dụng với Na2CO3 dư thu được kết tủa là Al(OH)3 0,3 mol và FeCO3 0,3 mol.
→ a = 58 , 2 g
Đúng 0
Bình luận (0)