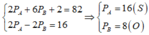Tổng số hạt mang điện trong ion AB4 3- là 50. Số hạt mang điện trong nguyên tử A nhiều hơn số hạt mang điện trong hạt nhân nguyên tử B là 22. Tìm số hiệu nguyên tử A, B

Những câu hỏi liên quan
tổng số hạt mang điện tích ion AB4-3 là 50. số hạt mang điện trong nguyên tử A nhiều hơn số hạt mang điện trong hạt nhân nguyên tử B là 22 . Số hiệu nguyên tử A,B là bao nhiêu?
Đề sai rùi bạn ơi ?/?/? AB4 2- chứ !
Xem lại đề hụ mình nhé
Đúng 0
Bình luận (1)
Tổng số hạt mang điện trong ion \(AB_3^{2-}\) ( phân tử \(AB_3+2e\rightarrow\) ion \(AB_3^{2-}\) ) bằng 82. Số hạt mang điện trong hạt nhân nguyên tử A nhiều hơn số hạt mang điện trong hạt nhân nguyên tử B là 8. Tìm số hiệu nguyên tử A và B.
Tổng hạt mang điện `AB_3^{2-}` là `82`
`->2p_A+3.2p_B+2=82(1)`
Số hạt mang điện trong hạt nhân `A` hơn `B` là `8`
`->p_A-p_B=8(2)`
`(1)(2)->p_A=16(S);p_B=8(O)`
`Z_A=16`
`Z_B=8`
Đúng 4
Bình luận (0)
Tổng số hạt mang điện trong ion AB32- bằng 82. Số hạt mang điện trong nhân nguyên tử A nhiều hơn số hạt mang điện trong nhân của nguyên tử B là 8. Số hiệu nguyên tử A và B (theo thứ tự) là
A. 6 và 8
B. 13 và 9
C. 16 và 8
D. 14 và 8
Tổng số hạt mang điện trong ion \(AB^{2-_3}\) bằng 82. Số hạt mang điện trong nhân nguyên tử A nhiều hơn trong nguyên tử B là 8. Số hiệu nguyên tử A và B là
Ta có: P = E (Do nguyên tử trung hòa về điện)
- Tổng số hạt mang điện trong AB32- là 82.
⇒ 2PA + 3.2PB = 82 - 2 (1)
- Số hạt mang điện trong nhân nguyên tử A nhiều hơn trong nguyên tử B là 8.
⇒ PA - 2PB = 8 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P_A=16=Z_A\\P_B=8=Z_B\end{matrix}\right.\)
Vậy: Số hiệu nguyên tử A và B lần lượt là 16 và 8.
Đúng 2
Bình luận (0)
Số hạt mang điện của nguyên tử A nhiều hơn so với nguyên tử B là 22. Số hạt không mang điên cuẩ nguyên tử A nhiều hơn số hạt không mang điện của nguyên tử B là 8. tổng số hạt của 2 nguyên tử này là 92. biết số hạt mang điện tích âm của nguyên tử A là 19. Tìm số hạt mỗi loại trong mỗi nguyên tử.
Ta có: pA +eA - pB + eB = 22 \(\Leftrightarrow\) 2eA - 2eB = 22
mà: eA = 19 = pA
\(\Rightarrow\) 38 - 2eB = 22 \(\Rightarrow\) 2eB = 16 \(\Rightarrow\) eB = 8 = pB
Theo đề bài :2eA + 2eB + nA + nB = 92
\(\Rightarrow\) 2.19 + 2.8 + nA +nB = 92
\(\Rightarrow\) nA + nB = 38 (1)
nA - nB = 8 \(\Rightarrow\) nA = 8 + nB (2)
Thay (2) vào (1), ta có: 8+nB + nB = 38
\(\Rightarrow\) 8 + 2nB = 38
\(\Rightarrow\) nB = 15
\(\Rightarrow\) nA = 8 + 15 = 23
Vây số hạt trong nguyên tử A: p = e = 19; n=23
B: p=e=8; n=15
Đúng 0
Bình luận (0)
các bạn có thể vào giải những câu hỏi mình vừa đăng hok...mình camon nhìu nhá....các bạn học giỏi quá :D :) ;)![]()
![]()
![]()
Đúng 0
Bình luận (0)
a) Tổng số hạt mang điện trong nguyên tử X là 18, nguyên tử X có tổng số hạt mang điện gấp đôi số hạt không mang điện. Hãy viết kí hiệu nguyên tử X b) Tổng số hạt P,E,N trong nguyên tử X là 156, số hạt mang điện nhiều hơn số hạt không mang điện là 32. Tìm số hạt P,E,N, số khối của X.
a) Ta có : \(\left\{{}\begin{matrix}2Z=18\\2Z=2N\end{matrix}\right.\)
=> Z=N=9
Vậy X là Flo (F)
b) Ta có : \(\left\{{}\begin{matrix}2Z+N=156\\2Z-N=32\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}Z=47=P=E\\N=62\end{matrix}\right.\)
A=Z+N=47+62=109
Đúng 2
Bình luận (2)
1 Tổng số hạt proton, nơtron, electron trong hai nguyên tử A và B là 142, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 42. Số hạt mang điện của nguyên tử B nhiều hơn số hạt mang điện của nguyên tử A là 12. Tìm hai nguyên tử A và B2Tổng số hạt proton, nơtron, electron trong hai nguyên tử A’ và B’ là 177, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 47. Số hạt mang điện của nguyên tử B nhiều hơn số hạt mang điện của nguyên tử A là 8. Tìm hai nguyên tử A’ và B’
Đọc tiếp
1 Tổng số hạt proton, nơtron, electron trong hai nguyên tử A và B là 142, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 42. Số hạt mang điện của nguyên tử B nhiều hơn số hạt mang điện của nguyên tử A là 12. Tìm hai nguyên tử A và B
2Tổng số hạt proton, nơtron, electron trong hai nguyên tử A’ và B’ là 177, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 47. Số hạt mang điện của nguyên tử B nhiều hơn số hạt mang điện của nguyên tử A là 8. Tìm hai nguyên tử A’ và B’
Tổng số hạt p,n,e trong hai nguyên tử A và B là 177 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 47, số hạt mang điện của nguyên tử B nhiều hơn số hạt mang điện của nguyên tử A là 8. Số proton của nguyên tử A là
26.
25.
24.
23.
Số hạt mang điện nhiều hơn số hạt không mang điện là 47 hạt nên ta có phương trình: \(\left(1\right)\left(2Z_A+2Z_B\right)-\left(N_A+N_B\right)=47\)
Số hạt mang điện của nguyên tử B nhiều hơn số hạt mang điện của nguyên tử A là 8. Nên ta có pt:
\(2Z_B-2Z_A=8\\ \Leftrightarrow Z_B-Z_A=4\left(2\right)\)
Tổng số hạt cơ bản của 2 nguyên tử A,B là 177. Nên ta có pt:
\(\left(3\right)2Z_A+N_A+2Z_B+N_B=147\)
Lấy (1) cộng (3), ta được:
\(4Z_A+4Z_B=224\\ \Leftrightarrow Z_A+Z_B=56\left(4\right)\)
Ta lấy (2) cộng (4) được: ZA=26; ZB=30
Vậy số proton nguyên tử A là 26
Đúng 2
Bình luận (1)
1:Tổng số hạt cơ bản của nguyên tử nguyên tố X là 36.Trong đó số hạt mang điện gấp đôi số hạt không mang điện.Xác định số hiệu nguyên tử và số khối của nguyên tử X?2:Tổng số hạt trong nguyên tử là Y là 54 hạt,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.a)Xác định các loại hạt trong Y b)Xác định đơn vị điện tích hạt nhân của Y c)Viết kí hiệu nguyên tử Y 3:Nguyên tử R có tổng số hạt là 115.Số hạt mang điện nhiều hơn số hạt không mang điện là 25.Xác định ngu...
Đọc tiếp
1:Tổng số hạt cơ bản của nguyên tử nguyên tố X là 36.Trong đó số hạt mang điện gấp đôi số hạt không mang điện.Xác định số hiệu nguyên tử và số khối của nguyên tử X?
2:Tổng số hạt trong nguyên tử là Y là 54 hạt,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.
a)Xác định các loại hạt trong Y b)Xác định đơn vị điện tích hạt nhân của Y c)Viết kí hiệu nguyên tử Y
3:Nguyên tử R có tổng số hạt là 115.Số hạt mang điện nhiều hơn số hạt không mang điện là 25.Xác định nguyên tử R từ đó suy ra STT của R?
-Mình cần rất gấp,các bạn giúp mình với!-
1. Ta có tổng số hạt cơ bản của nguyên tố X là 36 , suy ra
p + e + n = 36 => 2p + n = 36
Số hạt mang điện gấp đôi số hạt không mang điện : 2p = 2n => p = n
Vậy : 3p = 36 => p = 12 => số p = số e = số z = 12
Số khối : A = p + n = 12 + 12 = 24
Đúng 2
Bình luận (3)
2.
a, Ta có tổng số hạt cơ bản là 54 hạt.
=> p+e+n=54 => 2p+n=54(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 14
=> 2p-n=14(2)
Từ (1) và (2) ta có hệ pt:
2p-n=14
2p+n=54
<=> p=17
n=20
Vậy e=17, p=17, n=20
b, số hiệu nguyên tử Z=17
c, kí hiệu: Cl
Đúng 2
Bình luận (1)
3.
Ntử R có tổng số hạt cơ bản là 115
=> p+e+n=115
=>2p+n=115(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 25
=> 2p-n=25(2)
Từ (1)&(2) => ta có hệ phương trình
=>2p+n=115
2p-n=25
<=>p=35
n=45
=> e=35, p=35, n=45
=> R là Br
STT của Br là 35
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Một nguyên tử X có tổng số hạt nhân là 24. Trong đó số hạt điện mang điện nhiều hơn số hạt không mang điện là 8 a) Tìm P, n, e, A của nguyên tử X b) Viết kí hiệu của nguyên tử X
Tổng số hạt là :24
2p+n=24(1)
Số hạt mang điện nhiều hơn số hạt không mang điện là :8
2p−n=8(2)
(1),(2):p=e=8,n=8
=>A=8+8=16
=> đây là chất O oxi
Đúng 0
Bình luận (0)