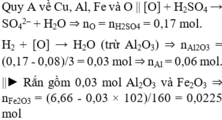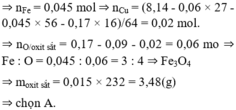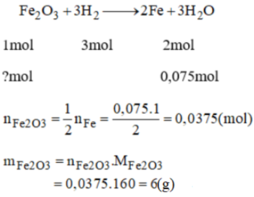Cho 23,2 g oxit sắt tác dụng vs dung dịch H2So4 loãng dư sau phản ứng thu được 55,2 gam muối sắt và 1 lượng nước . Tìm CT của oxit sắt trên

Những câu hỏi liên quan
Cho m gam Zn tác dụng với dung dịch H2SO4 loãng dư thu được V lít khí H2 đo ở đktc. Lượng khí H2 trên phản ứng vừa đủ với 16 gam sắt III oxit tạo ra kim loại và nước. Giá trị của m là:
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,1---->0,3
Zn + H2SO4 --> ZnSO4 + H2
0,3<--------------------0,3
=> m = 0,3.65 = 19,5 (g)
Đúng 3
Bình luận (0)
Bài 1: Cho kim loại sắt vào dung dịch axit H2SO4 loãng. Sau một thời gian, sắt tan hết thu được 6,72 lit khí hiđrô (đktc).
a) Tính khối lượng sắt ban đầu?
b) Để có lượng sắt tham gia phản ứng trên, phải cho bao nhiêu gam sắt(III) oxit tác dụng với khí hiđrô?
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3
a)\(m_{Fe}=0,3\cdot56=16,8g\)
b)\(Fe_2O_3+3H_2\rightarrow3Fe+3H_2O\)
0,1 0,3 0,3
\(m_{Fe_2O_3}=0,1\cdot160=16g\)
Đúng 4
Bình luận (0)
a)nH2 =6,72:22,4=0,3(mol)
PTHH Fe+H2SO4--->FeSO4+H2
theo pt , nFe = nH2 = 0,3 (mol)
=> mFe =n.M=0,3.56=16,8(g)
b) Ta có nH2=nFe=0,3(MOL)
Pthh: Fe2O3 + 3H2 ---> 2Fe + 3H2O
theo pt , nFe2O3=1/3 nH2=0,1(mol)
=> mFe2O3= n.M=0,1.(56.2+16.3)=16(g)
Vậy để có lượng sắt tham gia phản ứng trên phải có 16g Fe2O3 để tác dụng với H2
Đúng 1
Bình luận (0)
Hỗn hợp A có khối lượng 8,14 gam gồm: CuO,
Al
2
O
3
và một oxit sắt. Cho
H
2
dư qua A nung nóng, sau khi phản ứng xong thu được 1,44 gam
H
2
O
. Hòa tan hoàn toàn A cần 170 ml dung dịch...
Đọc tiếp
Hỗn hợp A có khối lượng 8,14 gam gồm: CuO, Al 2 O 3 và một oxit sắt. Cho H 2 dư qua A nung nóng, sau khi phản ứng xong thu được 1,44 gam H 2 O . Hòa tan hoàn toàn A cần 170 ml dung dịch H 2 SO 4 1M loãng được dung dịch B. Cho B tác dụng với NH 3 dư lọc lấy kết tủa đem nung trong không khí thu được 6,66 gam chất rắn. Công thức phân tử của oxit sắt và khối lượng của nó trong A là
A. Fe3O4; 3,48 gam.
B. Fe3O4; 2,32 gam.
C. FeO; 1,44 gam.
D. Fe2O3; 1,60 gam.
Hỗn hợp A có khối lượng 8,14 gam gồm: CuO, Al2O3 và một oxit sắt. Cho H2 dư qua A nung nóng, sau khi phản ứng xong thu được 1,44 gam H2O. Hòa tan hoàn toàn A cần 170 ml dung dịch H2SO4 1M loãng được dung dịch B. Cho B tác dụng với NH3 dư lọc lấy kết tủa đem nung trong không khí thu được 6,66 gam chất rắn. Công thức phân tử của oxit sắt và khối lượng của nó trong A là A. Fe3O4; 3,48 gam. B. Fe3O4; 2,32 gam. C. FeO; 1,44 gam. D. Fe2O3; 1,60 gam.
Đọc tiếp
Hỗn hợp A có khối lượng 8,14 gam gồm: CuO, Al2O3 và một oxit sắt. Cho H2 dư qua A nung nóng, sau khi phản ứng xong thu được 1,44 gam H2O. Hòa tan hoàn toàn A cần 170 ml dung dịch H2SO4 1M loãng được dung dịch B. Cho B tác dụng với NH3 dư lọc lấy kết tủa đem nung trong không khí thu được 6,66 gam chất rắn. Công thức phân tử của oxit sắt và khối lượng của nó trong A là
A. Fe3O4; 3,48 gam.
B. Fe3O4; 2,32 gam.
C. FeO; 1,44 gam.
D. Fe2O3; 1,60 gam.
Chọn đáp án A
Quy A về Cu, Al, Fe và O || [O] + H2SO4 → SO42– + H2O ⇒ nO = nH2SO4 = 0,17 mol.
H2 + [O] → H2O (trừ Al2O3) ⇒ nAl2O3 = (0,17 - 0,08)/3 = 0,03 mol ⇒ nAl = 0,06 mol.
||► Rắn gồm 0,03 mol Al2O3 và Fe2O3 ⇒ nFe2O3 = (6,66 - 0,03 × 102)/160 = 0,0225 mol
⇒ nFe = 0,045 mol ⇒ nCu = (8,14 - 0,06 × 27 - 0,045 × 56 - 0,17 × 16)/64 = 0,02 mol.
⇒ nO/oxit sắt = 0,17 - 0,09 - 0,02 = 0,06 mo ⇒ Fe : O = 0,045 : 0,06 = 3 : 4 ⇒ Fe3O4
⇒ moxit sắt = 0,015 × 232 = 3,48(g) ⇒ chọn A.
Đúng 0
Bình luận (0)
Cho mạt sắt vào một dung dịch chứa 0,2 mol H 2 S O 4 loãng. Sau một thời gian, bột sắt tan hoàn toàn và người ta thu được 1,68 lit khí hidro (đktc). Để có lượng sắt tham gia phản ứng trên, người ta phải dùng bao nhiêu gam sắt (III) oxit tác dụng với khí hidro.
Cho hỗn hợp A gồm Al và và một oxit sắt. Chia hỗn hợp A thành 2 phần bằng nhau. Phần 1: cho tác dụng với dung dịch H2SO4 loãng thu được 0,672 lít khí (đktc). Phần 2: Phản ứng nhiệt nhôm hoàn toàn, thu được hỗn hợp B, cho B tác dụng với dung dịch NaOH dư thu được 134,4 ml khí (đktc) sau đó cho tiếp dung dịch H2SO4 loãng, dư được 0,4032 lít H2(đktc). Oxit sắt là: A. Fe2O3 B. FeO C. Fe3O4 D. Không xác định
Đọc tiếp
Cho hỗn hợp A gồm Al và và một oxit sắt. Chia hỗn hợp A thành 2 phần bằng nhau.
Phần 1: cho tác dụng với dung dịch H2SO4 loãng thu được 0,672 lít khí (đktc).
Phần 2: Phản ứng nhiệt nhôm hoàn toàn, thu được hỗn hợp B, cho B tác dụng với dung dịch NaOH dư thu được 134,4 ml khí (đktc) sau đó cho tiếp dung dịch H2SO4 loãng, dư được 0,4032 lít H2(đktc). Oxit sắt là:
A. Fe2O3
B. FeO
C. Fe3O4
D. Không xác định
Đáp án C
Phần 1: Tác dụng vói dung dịch H2SO4 loãng gồm Al và FexOy nên n H 2 = 3 2 n Al ⇒ n Al = 0 , 02
Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn và hỗn hợp B tác dụng với dung dịch NaOH dư có H2 nên B có Fe, A12O3 và Al dư. Có n Al du = 2 3 n H 2 ( NaOH ) = 0 , 004 .
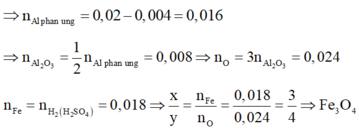
Đúng 0
Bình luận (0)
Cho 7,2 gam một oxit sắt tác dụng với dung dịch axit HCl có dư. Sau phản ứng thu được 12,7 gam một muối khan. Tim công thức oxit sắt đó.
Fe x O y + 2yHCl → x FeCl 2 y / x + y H 2 O
Theo phương trình : (56x + 16y) gam cho (56x + 71y) gam muối
Theo đề bài: 7,2 gam cho 12,7 gam
Giải ra, ta có : x/y = 1/1 . Công thức oxit săt là FeO.
Đúng 0
Bình luận (1)
Câu 3: Cho 23,2 gam oxit sắt từ tác dụng với 300 gam dung dịch axit clohiđric 3,65%. a/ Viết phương trình hóa học của phản ứng. b/ Chất nào còn dư sau phản ứng, khối lượng dư là bao nhiêu gam. c/ Tính khối lượng muỗi thu được sau phản ứng.
PTHH: \(Fe_3O_4+8HCl\rightarrow FeCl_2+2FeCl_3+4H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\\n_{HCl}=\dfrac{300\cdot3,65\%}{36,5}=0,3\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,3}{8}\) \(\Rightarrow\) Fe3O4 còn dư, HCl p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_3O_4\left(dư\right)}=0,0625\left(mol\right)\\n_{FeCl_2}=0,0375\left(mol\right)\\m_{FeCl_3}=0,075\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_3O_4\left(dư\right)}=0,0625\cdot232=14,5\left(g\right)\\m_{muối}=0,0375\cdot127+0,075\cdot162,5=16,95\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
nFe3O4= 23,2/232=0,1(mol); nHCl = (300.3,65%)/36,5= 0,3(mol)
a) PTHH: Fe3O4 + 8 HCl -> 2 FeCl3 + FeCl2 + 4 H2O
b) Ta có: 0,3/8 < 0,1/1
=> Fe3O4 dư, HCl hết, tính theo nHCl.
=> nFe3O4(p.ứ)= nFeCl2= nHCl/8=0,3/8= 0,0375(mol)
=> mFe3O4(dư)= (0,1- 0,0375).232=14,5(g)
c) nFeCl3= 2/8. 0,3= 0,075(mol)
=> mFeCl3= 0,075.162,5=12,1875(g)
mFeCl2= 0,0375. 127=4,7625(g)
=>m(muối)= 12,1875+ 4,7625= 16,95(g)
Đúng 2
Bình luận (0)
Dùng khí H 2 dư để khử hoàn toàn m gam một oxit sắt, sau phản ứng thu được 5,4
gam nước. Lấy toàn bộ lượng kim loại thu được ở trên hòa tan vào dung dịch HCl dư thì
thu được 25,4 gam muối. Tìm công thức oxit sắt và tính giá trị của m?
Moi người giải thích từng bước cho em nếu đc,
em cảm ơn ạ
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
Bảo toàn O: \(n_{O\left(oxit\right)}=n_{H_2O}=0,3\left(mol\right)\)
\(n_{FeCl_2}=\dfrac{25,4}{127}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,2 <-------------- 0,2
CTHH của oxit FexOy
=> x : y = 0,2 : 0,3 = 2 : 3
CTHH Fe2O3
Đúng 2
Bình luận (0)