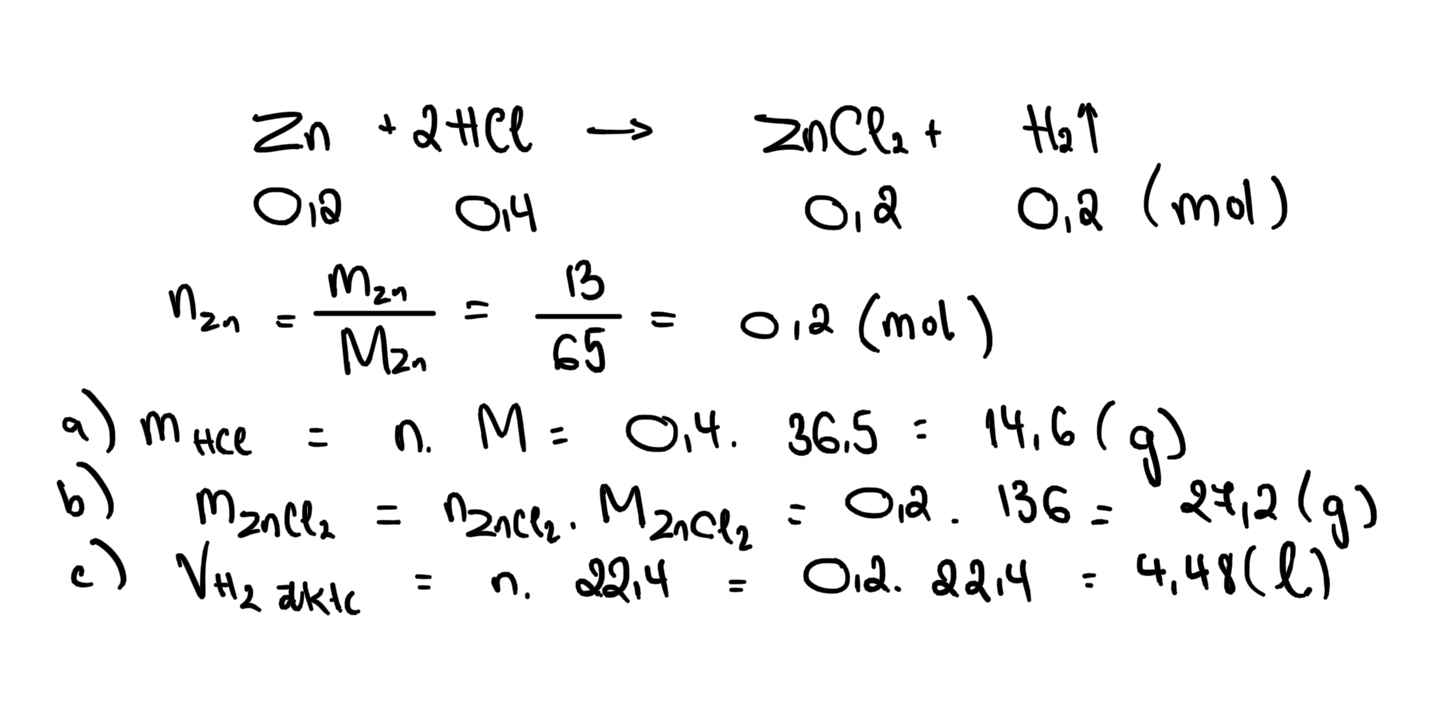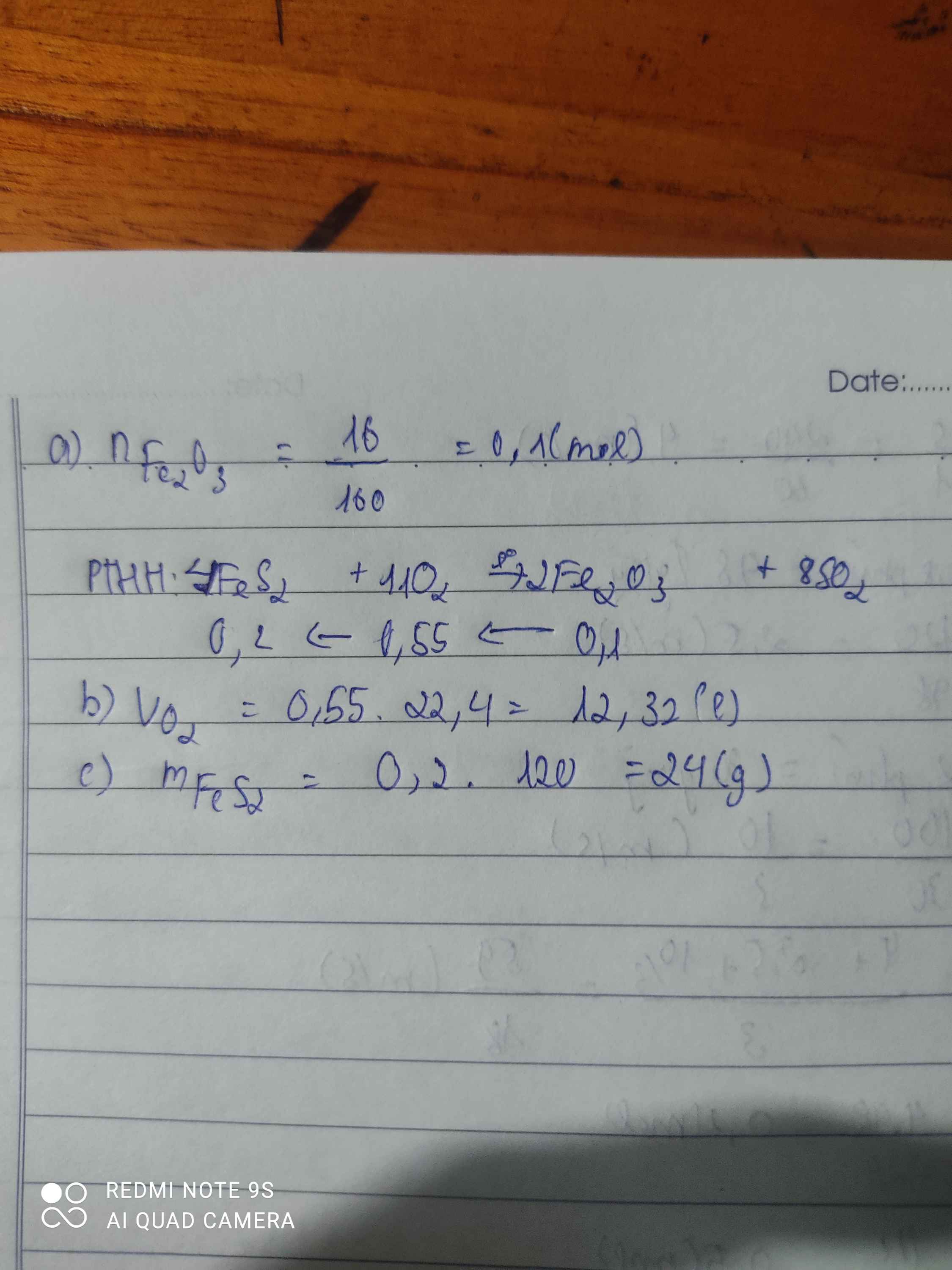Cho 13g Zn vào dung dịch HCl, thu được ZnCl và H\(_2\)
a) Viết PTHH
b) Tìm khối lượng HCl
c) Tìm khối lượng ZnCl\(_2\)
d) Tìm thể tích H\(_2\) (đktc)

Những câu hỏi liên quan
cho m kim loại kẽm tác dụng với 10,95g HCL tạo thành 13,6g ZnCl\(_2\)và khí H\(_2\)
a) tính khối lượng m
b) tính thể tích thu đc
a: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{HCL}=\dfrac{10.95}{36.5}=0.3\left(mol\right)\)
\(n_{ZnCl_2}=n_{Zn}=\dfrac{13.6}{136}=0.1\left(mol\right)\)
Vì \(\dfrac{n_{Zn}}{1}< \dfrac{n_{HCl}}{2}\)
nên HCl dư
=>Tính theo mol của Zn
\(m_{Zn}=0.1\cdot65=6.5\left(g\right)\)
b: \(n_{H_2}=0.1\left(mol\right)\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(lít\right)\)
Đúng 4
Bình luận (0)
a) \(n_{HCl}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\)
\(n_{ZnCl_2}=\dfrac{13,6}{136}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,1
Xét tỉ lệ \(\dfrac{0,3}{2}>\dfrac{0,1}{1}\) => HCl dư , ZnCl2 đủ
\(m_{Zn}=0,1.65=6,5\left(g\right)\)
b. \(V_{Zn}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
cho 32.5g Zn phản ứng vs HCL thu được ZnCl2 và H2
a) viết pthh
b) tính khối lượng HCL
c) Tích thể tích H2
d) Tính khối lượng ZnCl2
a) Zn + 2HCl → ZnCl2 + H2
b) mZn= 32,5g→ nZn=m/M= 32,5/65= 0,5 mol
Zn + 2HCl → ZnCl2 + H2
1mol 2mol 1mol 1mol
0,5mol→ 1mol→ 0,5mol→ 0,5mol
mHCl= n.M = 1.(1+35,5)=36,5 g
c) VH2= n.22,4= 0,5.(1.2)= 1 lít
d) mZnCl2= n.M= 0,5.( 65+ 35,5.2)= 68 g
Đúng 0
Bình luận (0)
Cho 9,75gam kim loại Zn tác dụng với dung dịch axit HCl dư, thủ được dùng dịch muối ZnCl² và khí H². Tính a. Thể tích khí H² thu được (đktc) b. Khối lượng dung dịch muối ZnCl² tạo thành
a, \(n_{Zn}=\dfrac{9,75}{65}=0,15\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,15\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)\)
b, \(m_{ZnCl_2}=0,15.136=20,4\left(g\right)\)
Đúng 1
Bình luận (0)
cho 32.5g Zn phản ứng vs HCL thu được ZnCl2 và H2
a) viết pthh
b) tính khối lượng HCL
c) Tích thể tích H2
d) Tính khối lượng ZnCl2
a) Zn + 2HCl -> ZnCl2 + H2
b) nZn = 32,5 : 65 = 0,5 mol
Zn + 2HCl -> ZnCl2 + H2
0,5 0,1 0,5 0,5 (mol)
=> mHCl = 0,1 . 36,5 = 3,65 g
c) V H2 = 0,5 . 22,4 = 11,2 l
d) mZnCl2 = 0,5 . 136 = 68 g
Đúng 0
Bình luận (0)
cho 13g kẽm tác dụng với dung dịch hcl, theo sơ đồ sau Zn+HCL->ZnCL+h2 a)khối lượng HCL cần dùng
b)khối lượng ZnCl2 thu dc
c) tính thể tích H2 ở (đktc)
Nhúng mottj thanh kẽm có khối lượng 13g và dung dịch HCl sau khi phản ứng một thời gian thì thu được 2,24l H2(đktc) và muối kemxclorua(ZnCl2)
a,Viết PTHH của phản ứng
b,Tính khối lượng ZnCl2 sinh ra
c,kim loại HCl cần dùng
d,khối lượng Zn có tan biến không
Câu 1: Cho 13g Zn phản ứng hoàn toàn với dung dịch axit clohidric (HCl)
a, Viết PTHH
b, Tính thể tích khí H\(_2\) sinh ra (đktc)
c, Nếu dùng toàn bộ lượng H\(_2\) bay ra ở trên đem khử 12g bột CuO ở nhiệt độ cao. Thì chất nào còn dư? Dư bao nhiêu gam?
Cho FeS_2 tác dụng với O_2 thì thu được Fe_2O_3 và SO_2 sau p.ưa, Viết PTHH của p.ư trên?b, Tìm thể tích oxi ở (đktc) cần sử dụng biết sau p.ư thu được 16g Fe_2O_3?c, Xác định khối lượng FeS_2 đã sử dụng
Đọc tiếp
Cho FeS\(_2\) tác dụng với O\(_2\) thì thu được Fe\(_2\)O\(_3\) và SO\(_2\) sau p.ư
a, Viết PTHH của p.ư trên?
b, Tìm thể tích oxi ở (đktc) cần sử dụng biết sau p.ư thu được 16g Fe\(_2\)O\(_3\)?
c, Xác định khối lượng FeS\(_2\) đã sử dụng
4FeS+7O2-to>2Fe2O3+4SO2
0,2----0,35------0,1 mol
n Fe2O3=\(\dfrac{16}{160}\)=0,1 mol
=>VO2=0,35.22,4=7,84l
=>m FeS2=0,2.120=24g
Đúng 1
Bình luận (1)
Cho 11,2 gam Fe tác dụng với dung dịch HCL . sau phản ứng thu được sắt ( II) clorua (FeCL_2) và khí Hidro (H_2)
a, Lập PTHH của phản ứng
b, Cho biết tỉ lệ số nguyện tử , số phân tử của từng cặp chất trong phản ứng
c, thể tích H_2 thu được ở đktc
d, Khối lượng HCL phản ứng
e, Khối lượng FeCL_2 tạo thành
Đọc tiếp
Cho 11,2 gam Fe tác dụng với dung dịch HCL . sau phản ứng thu được sắt ( II) clorua (FeCL\(_2\)) và khí Hidro (H\(_2\))
a, Lập PTHH của phản ứng
b, Cho biết tỉ lệ số nguyện tử , số phân tử của từng cặp chất trong phản ứng
c, thể tích H\(_2\) thu được ở đktc
d, Khối lượng HCL phản ứng
e, Khối lượng FeCL\(_2\) tạo thành
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
a) PT: Fe + 2HCl → FeCl2 + H2
mol 0,2 → 0,4 0,2 0,2
b) Số nguyên tử Fe : Số phân tử HCl : Số phân tử FeCl2 : Số phân tử H2
= 1 : 2 : 1 : 1
c) \(V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)
d) mHCl = 0,4.36,5 = 14,6 (g)
e) \(m_{FeCl_2}=0,2.127=25,4\left(g\right)\)
Đúng 0
Bình luận (0)
a)Fe+2HCl--->FeCl2+H2
b) tỉ lệ: 1:2:1:1
nFe=11,2:56=0,2mol
c)theo PTHH 1 mol Fe tạo thành 1 mol H2
0,2 mol Fe tạo thành 0,2 mol H2
VH2=0,2.22,4=4,48(l)
d) theo PTHH 1 mol Fe cần 2 mol HCl
0,2 mol Fe cần 0,4 mol HCl
mHCl= 0,4.36,5=14,6g
e) theo PTHH 1mol Fe cần 1 mol FeCl2
0,2 mol Fe cần 0,2 mol FeCl2
mFeCl2 = 0,2.127=25,4g
Đúng 0
Bình luận (0)
a) \(Fe\) + \(2HCl\) \(\rightarrow\) \(FeCl_2\) + \(H_2\)
b) Fe : HCl=1:2
Fe : FeCl\(_2\)=1:1
Fe : H\(_2\) =1:1
(còn HCl bạn làm tiếp nhé)
c) \(n_{Fe}\)=\(\dfrac{11,2}{56}\)=0,2(mol)
Theo PT ta có: \(n_{H_2}\)=\(n_{Fe}\)=0,2(mol)\(\Rightarrow\)\(V_{H_2}\)=0,2\(\times\)22,4=4,48(l)
d) Theo PT ta có: \(n_{HCl}\)=\(2n_{Fe}\)=2\(\times\)0,2=0,2\(\Rightarrow\)\(m_{HCl}\)=0,4\(\times\)36,5=14,6(g)
e)Theo PT ta có:\(n_{FeCl_2}\)=\(n_{Fe}\)=0,2\(\Rightarrow\)\(m_{FeCl_2}\)=0,2\(\times\)127=25,4(g)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời