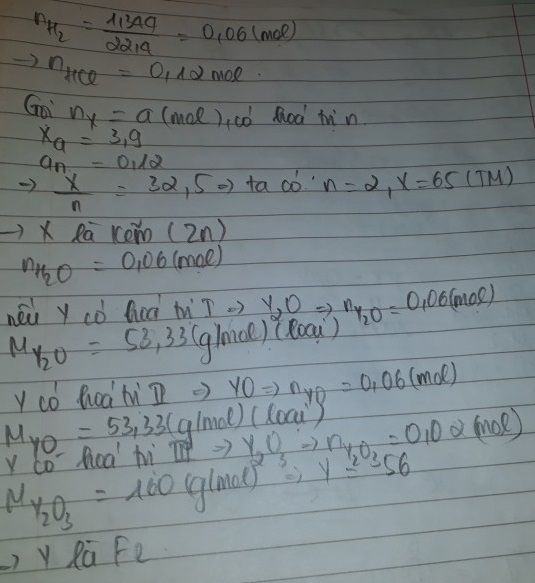Để hòa tan 3,9g kim loại X cần dùng thể tích (ml) dd HCl và có 1,344l Hiđro bay ra(dktc). Mặt khác để hòa tan 3,2g oxit kim loại Y nặng a gam. Nung Y cũng cần dùng thể tích (ml) dd HCl ở trên. Hoi X,Y là kim loại gì?

Những câu hỏi liên quan
Xác định kim loại X,Y
Để hoàn tan 3,9g kim loại X cần dùng V ml dung dịch HCl và có 1,344l H2 bay ra (đktc).Mặt khác để hoàn tan 3,2g oxit kim loại Y cũng cần V ml dung dịch HCl ở trên. X,Y là kim loại gì
2X +2a HCl \(\rightarrow\)2XCla + aH2 (1)
nH2=\(\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Theo PTHH 1 ta có:
nX=\(\dfrac{a}{2}\)nH2=0,03a(mol)
=>MX=\(\dfrac{3,9}{0,03a}=\dfrac{130}{a}\)
Vì X là kim loại nên a=1;2;3
Ta có bảng:
| a=1 | X=130(loại) | |
| a=2 | X=65(chọn) | |
| b=3 | X=43.3(loại) |
Vậy X là kẽm,KHHH là Zn
nHCl đã PƯ=2nH2=0,12(mol)
2Y +2a HCl \(\rightarrow\)2YCla + aH2 (2)
Theo PTHH 2 ta cso:
nY=\(\dfrac{1}{a}\)nHCl=\(\dfrac{0,12}{a}\)
MY=\(\dfrac{3,2}{\dfrac{0,12}{a}}\)
Đúng 0
Bình luận (0)
Để hòa tan 3,9 g kim loại X cần dùng V ml dung dịch HCl và thu được 1,344 lít khí H2 (đktc). Mặt khác để hòa tan 3,2 g oxit của kim loại Y cũng cần dùng V ml dung dịch HCl trên. Hỏi X,Y là kim loại gì?
- Thí nghiệm 1: Gọi hóa trị của X là n
CÓ n H2 = 0,06 ( mol ) => n HCL = 0,12 ( mol )
PTHH: 2X +2n HCL ===> 2XCLn + nH2
theo pthh: n X = 0,12/n ( mol )
=> X = 32,5n
Xét: n = 2 => X = 65 ( Zn )
- Thí nghiệm 2
Gọi CT của oxit : YaOb
PTHH
\(YaOb+2bHCL\rightarrow aYCl_{\dfrac{2b}{a}}+bH2O\)
theo pthh: n YaOb = 0,06/b ( mol )
=> aY + 16b = 160/3 . b
=> Y = 56 . 2b/a
Xét: 2b/a = 3 => Y = 56 ( Fe )
Đúng 1
Bình luận (0)
Để hoà tan 1,95 gam kim loại X cần dùng V ml dung dịch HCl và thu được 0,672 lít khí H 2 (ở đktc). Mặt khác nếu hoà tan 1,6 gam oxit của kim loại Y cũng cần dùng V ml dung dịch HCl ở trên. Xác định hai kim loại X và Y.
Thể tích dung dịch HCl dùng cho cả 2 phản ứng bằng nhau, nên có cùng số mol. Kí hiệu X, Y là khối lượng mol nguyên tử của 2 kim loại.
Phương trình hoá học của phản ứng :
2X + 2nHCl → 2X Cl n + n H 2 ↑
n H 2 = 0,672 /22,4 = 0,03 mol
Theo đề bài: 0,06/n x X = 1,95 → X = 32,5n
Kẻ bảng
| n | 1 | 2 | 3 |
| X | 32,5 | 65 | 97,5 |
Vậy X là Zn
Y 2 O m + mHCl → Y Cl m + m H 2 O
Theo đề bài, ta có:
(2Y + 16m) = 1,6 → Y = 56/3.m
Kẻ bảng
| m | 1 | 2 | 3 |
| Y | 56,3 | 112/3 | 56 |
Vậy Y là Fe.
Đúng 0
Bình luận (0)
để hòa tan 3,2g một oxit kim loại cần dùng v ml dung dịch HCl. mặt khác đẻ hòa tan 3,9g một kim loại khác cũng cần dùng v ml dung dịch HCl và thấy có 1344cm2 hidro bay ra ở đktc. hãy xác định kim loại và oxit kim loại trên
Để hòa tan hoàn toàn 7,8 gam kim loại A càn dùng V ml dung dịch HCl và có 2,688 lít H2 bay ra (ĐKTC). Mặt khác để hòa tan 6,4 gam oxit của kim loại B cũng cần dùng V ml dung dịch HCL trên. Xác định kim loại A và B
Đúng 0
Bình luận (0)
Để hòa tan hoàn toàn 7,8 gam kim loại A cần dùng V ml dung dịch Hcl và 2,688l H2 ( đktc ). Mặt khác, để hoà tan 6,4 ô-xit của kim loại B cũng cần V ml dung dịch Hcl trên. Xác định A,B
\(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
PTHH: 2A + 2nHCl --> 2ACln + nH2
\(\dfrac{0,24}{n}\)<-0,24------------0,12
=> \(M_A=\dfrac{7,8}{\dfrac{0,24}{n}}=32,5n\left(g/mol\right)\)
Xét n = 1 => Loại
Xét n = 2 => MA = 65 (g/mol) => A là Zn
Xét n = 3 => Loại
PTHH: B2Om + 2mHCl --> 2BClm + mH2O
\(\dfrac{0,12}{m}\)<--0,24
=> \(M_{B_2O_m}=2.M_B+16m=\dfrac{6,4}{\dfrac{0,12}{m}}=\dfrac{160}{3}m\left(g/mol\right)\)
=> \(M_B=\dfrac{56}{3}m\left(g/mol\right)\)
Xét m = 1 => Loại
Xét m = 2 => Loại
Xét m = 3 => MB = 56 (g/mol)
=> B là Fe
Đúng 2
Bình luận (0)
Khử hoàn toàn 24 gam Fe3O4 bằng khí H2(nung nóng),thu được sắt kim loại và nước. a. Viết PTHH xảy ra b. Tính thể tích khí H2(ở đktc) thu được c. Tính thể tích dd HCl 1.5M cần dùng để hòa tan hết lượng sắt tạo thành từ phản ứng trên.
\(n_{Fe_3O_4}=\dfrac{24}{232}=\dfrac{3}{29}\left(mol\right)\)
PTHH :
\(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
3/29 9/29
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
9/29 18/29
\(c,V_{HCl}=\dfrac{\dfrac{18}{29}}{1,5}=\dfrac{12}{29}\left(l\right)\)
Đúng 3
Bình luận (0)
Khử hoàn toàn 24 gam Fe2O3 bằng khí H2(nung nóng),thu được sắt kim loại và nước. a. Viết PTHH xảy ra b. Tính thể tích khí H2(ở đktc) thu được c. Tính thể tích dd HCl 1.5M cần dùng để hòa tan hết lượng sắt tạo thành từ phản ứng trên.
a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe_2O_3}=\dfrac{24}{160}=0,15\left(mol\right)\)
Theo PT: \(n_{H_2}=3n_{Fe_2O_3}=0,45\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,45.22,4=10,08\left(l\right)\)
c, n\(n_{Fe}=2n_{Fe_2O_3}=0,3\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{HCl}=2n_{Fe}=0,6\left(mol\right)\Rightarrow V_{HCl}=\dfrac{0,6}{1,5}=0,4\left(M\right)\)
Đúng 2
Bình luận (0)
a. Phương trình hoá học của phản ứng khử Fe2O3 bằng H2 là: Fe2O3 + 3H2 -> 2Fe + 3H2O
b. Theo phương trình trên, ta thấy 1 mol Fe2O3 cần 3 mol H2 để khử hoàn toàn. Do đó, số mol H2 cần dùng để khử hoàn toàn 24 gam Fe2O3 là:
n(H2) = 24/(2*55.85) * 3 = 2.56 (mol)
Theo định luật Avogadro, 1 mol khí ở đktc có thể chiếm thể tích là 22.4 lít. Vậy, thể tích khí H2 ở đktc thu được là:
V(H2)= n(H2) * 22.4 = 2.56 * 22.4 = 57.2 (lít)
Vậy thể tích khí H2 thu được là 57.2 lít.
c. Theo phương trình trên, ta thấy 1 mol Fe tạo thành cần 6 mol HCI để hòa tan hoàn toàn. Do đó, số mol HCI cần dùng để hòa tan hết lượng sắt tạo thành là: n(HCI) = 2 * n(H2) * 6 = 30.72 (mol)
Thể tích HCI 1.5M cần dùng là: V(HCI)= n(HCI) C(HCI)= 30.72/1.5 = 20.48 (lít)
Vậy thể tích dd HCI 1.5M cần dùng để hòa tan hết lượng sắt tạo thành là 20.48 lít.
Đúng 0
Bình luận (0)
Câu 2: Hòa tan hoàn toàn kim loại nhôm vào 300 ml dd HCl 2M a/ Viết phương trình phản ứng và tính thể tích khí Hydrogen H2 thoát ra (đktc) b/ Tính khối lượng kim loại cần dùng
Đọc tiếp
Câu 2: Hòa tan hoàn toàn kim loại nhôm vào 300 ml dd HCl 2M
a/ Viết phương trình phản ứng và tính thể tích khí Hydrogen H2 thoát ra (đktc)
b/ Tính khối lượng kim loại cần dùng
\(a/n_{HCl}=0,3.2=0,6mol\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,6 0.2 0,3
\(V_{H_2}=0,2.22,4=4,48l\\ b/m_{Al}=0,2.27=5,4g\)
Đúng 1
Bình luận (0)
Bài 1 Hòa tan 10 gam hỗn hợp gồm hai kim loại đồng và kẽm cần dùng hết V ml dung dịch axit HCl 0,2 mol thấy thoát ra 2,24 l khí ( đo ở dktc )a. Tính phần trăm theo khối lượng của mỗi kim loại có trong hỗn hợp đầu.b. Tính V của dd axit HCl cần dùng. Bài 2 Cho 20g hỗn hợp muối Na2CO3 và Na2SO4 tác dụng vừa đủ với dd HCl 20% thu được 2,24 dm^3 khí ở dktca. Tính phần trăm theo khối lượng của các chất có trong hỗn hợp b. Tính khối lượng Hcl đã dùng
Đọc tiếp
Bài 1
Hòa tan 10 gam hỗn hợp gồm hai kim loại đồng và kẽm cần dùng hết V ml dung dịch axit HCl 0,2 mol thấy thoát ra 2,24 l khí ( đo ở dktc )
a. Tính phần trăm theo khối lượng của mỗi kim loại có trong hỗn hợp đầu.
b. Tính V của dd axit HCl cần dùng.
Bài 2 Cho 20g hỗn hợp muối Na2CO3 và Na2SO4 tác dụng vừa đủ với dd HCl 20% thu được 2,24 dm^3 khí ở dktc
a. Tính phần trăm theo khối lượng của các chất có trong hỗn hợp
b. Tính khối lượng Hcl đã dùng