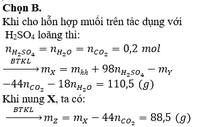Nung 15,15g chất rắn A thu được chất rắn B và 1,68 lít khí O2 (đktc).Trong B có 37,65% O ;15,47% N còn lại là Kali . Xác định CTHH A; B

Những câu hỏi liên quan
nung hoàn toàn 15,15g chất rắn A thu được chất rắn B và 1,68l O2 (đktc) . Trong B có % theo khối lượng các nguyên tố là 37,65% O2 , 16,75%N còn lại là K . Xác định CTHH của A-B
\(Đặt:CTTQ.B:K_aN_bO_c\left(a,b,c:nguyên,dương\right)\\ \Rightarrow a:b:c=\dfrac{45,6\%}{39}:\dfrac{16,75\%}{14}:\dfrac{37,65\%}{16}=0,01:0,01:0,02\\ Vậy:a:b:c=1:1:2\\ \Rightarrow B:KNO_2\\ \Rightarrow A:KNO_3\\ PTHH:2KNO_3\rightarrow\left(t^o\right)2KNO_2+O_2\)
Đúng 4
Bình luận (0)
Nung hoàn toàn 15,15 gam chất rắn A thu được chất rắn B và 1,68 lít khí oxi (ở đktc). Trong hợp chất B có thành phần % khối lượng các nguyên tố: 37,65% Oxi, 16,47% Nitơ còn lại là Kali. Xác định công thức hóa học của B và A. Biết rằng công thức đơn giản nhất chính là công thức hóa học của A, B.
Đọc tiếp
Nung hoàn toàn 15,15 gam chất rắn A thu được chất rắn B và 1,68 lít khí oxi (ở đktc). Trong hợp chất B có thành phần % khối lượng các nguyên tố: 37,65% Oxi, 16,47% Nitơ còn lại là Kali. Xác định công thức hóa học của B và A. Biết rằng công thức đơn giản nhất chính là công thức hóa học của A, B.
a. Nung hoàn toàn 15,15 gam chất rắn A thu được chất rắn B và 1,68 lít khí oxi (ở đktc). Trong hợp chất B có thành phần % khối lượng các nguyên tố: 37,65% Oxi, 16,75% Nitơ còn lại là Kali. Xác định công thức hóa học của B và A. Biết rằng công thức đơn giản nhất chính là công thức hóa học của A, Bb. Một hợp chất khí X có thành phần gồm 2 nguyên tố C và O. Biết tỉ lệ về khối lượng của C đối với O là mC : mO 3 : 8. Xác định công thức phân tử của hợp chất khí X (Biết rằng công thức đơn giản nhất ch...
Đọc tiếp
a. Nung hoàn toàn 15,15 gam chất rắn A thu được chất rắn B và 1,68 lít khí oxi (ở đktc). Trong hợp chất B có thành phần % khối lượng các nguyên tố: 37,65% Oxi, 16,75% Nitơ còn lại là Kali. Xác định công thức hóa học của B và A. Biết rằng công thức đơn giản nhất chính là công thức hóa học của A, B
b. Một hợp chất khí X có thành phần gồm 2 nguyên tố C và O. Biết tỉ lệ về khối lượng của C đối với O là mC : mO = 3 : 8. Xác định công thức phân tử của hợp chất khí X (Biết rằng công thức đơn giản nhất chính là công thức phân tử của X)
a. Nung hoàn toàn 15,15 gam chất rắn A thu được chất rắn B và 1,68 lít khí oxi (ở đktc). Trong hợp chất B có thành phần % khối lượng các nguyên tố: 37,65% Oxi, 16,75% Nitơ còn lại là Kali. Xác định công thức hóa học của B và A. Biết rằng công thức đơn giản nhất chính là công thức hóa học của A, B
a) \(n_{O_2}=0,075\left(mol\right)\)=>\(m_{O_2}=2,4\left(g\right)\)
Bảo toàn khối lượng : \(m_A=m_B+m_{O_2}\Rightarrow m_B=15,15-2,4=12,75\left(g\right)\)
Trong B có : \(m_O=37,65\%.12,75=4,8\left(g\right)\Rightarrow n_O=0,3\left(mol\right)\)
\(m_N=16,75\%.12,75=2,1\left(g\right)\Rightarrow n_N=0,15\left(mol\right)\)
\(m_K=12,75-\left(4,8+2,1\right)=5,85\left(g\right)\Rightarrow n_K=0,15\left(mol\right)\)
Gọi CTHH của B là KxNyOz
Ta có : x:y:z=0,15:0,15:0,3=1:1:2
=> CTHH B là KNO2
Gọi CTHH của A là KaNbOc
Bảo toàn nguyên tố O => \(n_{O\left(trongA\right)}=0,075.2+0,3=0,45\left(mol\right)\)
Bảo toàn nguyên tố N : \(n_{N\left(trongA\right)}=n_{N\left(trongB\right)}=0,15\left(mol\right)\)
Bảo toàn nguyên tố N : \(n_{N\left(trongA\right)}=n_{N\left(trongB\right)}=0,15\left(mol\right)\)
Ta có a:b:c=0,15 : 0,15 : 0,45 = 1:1:3
=> CTHH của A là KNO3
Đúng 3
Bình luận (0)
b. Một hợp chất khí X có thành phần gồm 2 nguyên tố C và O. Biết tỉ lệ về khối lượng của C đối với O là mC : mO = 3 : 8. Xác định công thức phân tử của hợp chất khí X (Biết rằng công thức đơn giản nhất chính là công thức phân tử của X)
Gọi CTHH của khí cần tìm là CxOy
Ta có : \(\dfrac{m_C}{m_O}=\dfrac{12x}{16y}=\dfrac{3}{8}\Rightarrow\dfrac{x}{y}=\dfrac{1}{2}\)
Vi công thức đơn giản nhất chính là công thức phân tử của X
Vậy CTHH của X là CO2
Đúng 0
Bình luận (0)
a) nO2=0,075(mol)nO2=0,075(mol)=>mO2=2,4(g)mO2=2,4(g)
Bảo toàn khối lượng : mA=mB+mO2⇒mB=15,15−2,4=12,75(g)mA=mB+mO2⇒mB=15,15−2,4=12,75(g)
Trong B có : mO=37,65%.12,75=4,8(g)⇒nO=0,3(mol)mO=37,65%.12,75=4,8(g)⇒nO=0,3(mol)
mN=16,75%.12,75=2,1(g)⇒nN=0,15(mol)mN=16,75%.12,75=2,1(g)⇒nN=0,15(mol)
mK=12,75−(4,8+2,1)=5,85(g)⇒nK=0,15(mol)mK=12,75−(4,8+2,1)=5,85(g)⇒nK=0,15(mol)
Gọi CTHH của B là KxNyOz
Ta có : x:y:z=0,15:0,15:0,3=1:1:2
=> CTHH B là KNO2
Gọi CTHH của A là KaNbOc
Bảo toàn nguyên tố O => nO(trongA)=0,075.2+0,3=0,45(mol)nO(trongA)=0,075.2+0,3=0,45(mol)
Bảo toàn nguyên tố N : nN(trongA)=nN(trongB)=0,15(mol)nN(trongA)=nN(trongB)=0,15(mol)
Bảo toàn nguyên tố N : nN(trongA)=nN(trongB)=0,15(mol)nN(trongA)=nN(trongB)=0,15(mol)
Ta có a:b:c=0,15 : 0,15 : 0,45 = 1:
Đúng 0
Bình luận (0)
nung hoàn toàn 15,15 gam chất rắn A thu được chất rắn B và 1,68 lít khí oxi trong hợp chất B có thành phần % khối lượng các nguyên tố 37,65% oxi, 116,47% nito còn lại là kali.vác định công thức HH của A,B(biết công thức HH là công thức đơn giản nhất)
Gọi công thức tổng quát của A là KxNyOz
\(n_O=2n_{O_2}=2.\frac{1,68}{22,4}=0,15\)
\(\Rightarrow m_O=0,15.16=2,4\)
Cứ 15,15 g A thì có 2,4g O
Vậy để có 16g O thì \(A=\frac{16.15,15}{2,4}=101\)
Tới đây hết giải được %N mà hơn 100% thì làm gì có. Đề sai rồi
Đúng 0
Bình luận (2)
chép đè sai rồi kìa bạn, sao lại 116,47% được?
Đúng 0
Bình luận (0)
Nung hoàn toàn 15,15g chất rắn A thu được chất rắn B và 1,68 l khí O2 (đktc). Trong hợp chất B có thành phần phần trăm khối lượng các nguyên tố 37,65%O, 16,47%N, còn lại là K. Xác định CTHH của A và B ( Biết CT đơn giản nhất chính là CTHH của A, B)
* hợp chất B
%K=100-(37,65+16,47)=45,88%
Đặt Cthh là \(K_xN_yO_z\)
\(x:y:z=\dfrac{45,88}{39}:\dfrac{16,47}{14}:\dfrac{37,65}{16}=1:1:2\)
Cthh là KNO2
Trong A gồm các nguyên tố K,N và O
nO2=1,68/22,4=0,075 mol=> mO2=0,075.32=2,4 gam
\(A-t^o->KNO_2+O_2\)
Áp dụng định luật bảo toàn khối lượng
=> mKNO2=12,75 mol => mKNO2=0,15 mol
=> Trong A có chứa 0,15 mol K,0,15 mol N và còn lại là O
mO trong A: 15,15-39.0,15-14.0,15=7,2 gam => nO=0,45 mol
Đặt Cthh của A là KaNbOc
\(a:b:c=0,15:0,15:0,45=1:1:3\)
=> CTHH của A là KNO3
Đúng 0
Bình luận (13)
PTHH: A --to--> B + O2
- Gọi CTHH của B có dạng : \(K_xN_yO_z\) (K, N, O \(\ne\)0)
=> %K = 100% - %O - %N = 100% - 37,65% - 16,47% = 45,88%
=> \(x:y:z=\dfrac{45,88\%}{39}:\dfrac{16,47\%}{14}:\dfrac{37,65\%}{16}=1:1:2\)
=> CTHH của B là: KNO2
n\(O_2\)= \(\dfrac{1,68}{22,4}\)= 0,075 (mol)
=> m\(O_2\)= 0,075.32 = 2,4 (gam)
=> mB = mA - m\(O_2\)= 15,15 - 2,4 = 12,75 (g)
=> mB = m\(KNO_2\)=12,75 (g)
=> n\(KNO_2\) = \(\dfrac{12,75}{85}=0,15\left(mol\right)\)
Từ trên suy ra trong hợp chất A chứa K, N, O
- Gọi CTHH của A là KaNbOt (a, b, t \(\ne\) 0)
Theo bài ra: n\(K\left(trongA\right)\)= n\(K\left(hcKNO_2\right)\)= 0,15 (mol)
=> n\(N\left(A\right)\)= n\(N\left(hcKNO_2\right)\) = 0,15 (mol)
=> \(n_{O\left(A\right)}=n_{O\left(hcKNO_2\right)}+n_{O\left(O_2\right)}\) = 2. 0,15 + 2. 0,075 = 0,45 (mol)
=> a : b: t = \(n_K:n_N:n_O\) = 0,15 :0,15: 0,45 = 1:1:3
=> CTHH của A là KNO3
Đúng 1
Bình luận (0)
\(n_{O_2}=0,075mol\)
\(\rightarrow m_{O_2}0,075.32=2,4g\)
Áp dụng định luật bảo toàn khối lượng ta có :
\(m_B=15,15-2,4=12,75g\)
Ta có \(\%0=37,65\%;\%N=16,47\%\rightarrow\%K=45,88\%\)
\(\Rightarrow m_O=\dfrac{37,65}{100}.12.75=4,8g\)
\(m_K=\dfrac{45,88}{100}.12,75\approx5,85g\)
\(m_N=\dfrac{16,47}{100}.12,75\approx2,1g\)
\(\Rightarrow m_O=\dfrac{37,65}{100}.12.75=4,8g\)
Khi đó : \(n_K:n_N:n_O=\dfrac{4,8}{16}:\dfrac{2,1}{14}:\dfrac{5,85}{39}=1:1:2\)
Vì công thức đơn giản nhất chính là CTHH nên ta có CTHH của B là\(KNO_2\)
Áp dụng định luật bảo toàn nguyên tố m:
\(m_{O_2}=4,8+2,4=7,2g\)
\(\rightarrow n_O=\dfrac{7,2}{16}=0,45mol\)
\(\Rightarrow n_{O_2}=0,225mol\)
\(n_N=n_K=0,15mol\)
Khi đó : \(n_K:n_N:n_O=0,15:0,15:0,45=1:1:3\)
Vì công thức đơn giản nhất chính là CTHH nên ta có CTHH của A là\(KNO_3\)
TỐI RỒI NÊN GẢI THÍCH NGẮN GỌN .
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 17,92 lít khí H2 đktc trong 15,68 lít O2 đktc. Ngưng tụ sản phẩm thu được chất lỏng A và khí B. Cho toàn bộ khí B pư hết với 16,2g Al, thu được hỗn hợp chất rắn C. Hoà tan hoàn toàn chất rắn C trong dung dịch có chứa 73g HCl thu được dung dịch D và khí E. Xác định các chất trong A,B,C,D và E. Tính khối lượng các chất trong A, C và số mol các chất trong dd DBiết: Al2O3 + 6HCl -- 2AlCl3 + 3H2O
Đọc tiếp
Đốt cháy hoàn toàn 17,92 lít khí H2 đktc trong 15,68 lít O2 đktc. Ngưng tụ sản phẩm thu được chất lỏng A và khí B. Cho toàn bộ khí B pư hết với 16,2g Al, thu được hỗn hợp chất rắn C. Hoà tan hoàn toàn chất rắn C trong dung dịch có chứa 73g HCl thu được dung dịch D và khí E.
Xác định các chất trong A,B,C,D và E. Tính khối lượng các chất trong A, C và số mol các chất trong dd D
Biết: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
Nung x mol Fe và 0,2 mol Cu trong không khí một thời gian thu được 26,8 gam hỗn hợp chất rắn. Hoà tan hoàn toàn hỗn hợp chất rắn trên bằng
H
2
SO
4
đặc, nóng, dư thu được dung dịch Y và 1,68 lít khí
SO
2
(đktc). Giá trị của x mol là A. 0,1 mol B. 0,15mol C. 0,2 mol D. 0,25 mol
Đọc tiếp
Nung x mol Fe và 0,2 mol Cu trong không khí một thời gian thu được 26,8 gam hỗn hợp chất rắn. Hoà tan hoàn toàn hỗn hợp chất rắn trên bằng H 2 SO 4 đặc, nóng, dư thu được dung dịch Y và 1,68 lít khí SO 2 (đktc). Giá trị của x mol là
A. 0,1 mol
B. 0,15mol
C. 0,2 mol
D. 0,25 mol
một hỗn hợp x gồm KClO3 và KMnO4 được chia thành 2 phần bằng nhau. Phần 1 nung nóng một thời gian thu được 2,24 lít khí O2 ở đktc và chất rắn Y, trong Y có %O = 34,5%. Phần 2 đem nhiệt phân hoàn toàn thì thu được 29,1 gam chất rắn. Tính % khối lượng các chất trong X
Gọi số mol KClO3, KMnO4 trong mỗi phần là a, b (mol)
Phần 1:
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
mY = 122,5a + 158b - 0,1.32 = 122,5a + 158b - 3,2 (g)
Bảo toàn O: \(n_{O\left(Y\right)}=3a+4b-0,2\left(mol\right)\)
\(\%O=\dfrac{16\left(3a+4b-0,2\right)}{122,5a+158b-3,2}.100\%=34,5\%\)
=> 5,7375a + 9,49b = 2,096 (1)
Phần 2:
PTHH: 2KClO3 --to--> 2KCl + 3O2
a----------->a
2KMnO4 --to--> K2MnO4 + MnO2 + O2
b------------>0,5b------>0,5b
=> 74,5a + 142b = 29,1 (2)
(1)(2) => a = 0,2 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{0,2.122,5}{0,2.122,5+0,1.158}.100\%=60,8\%\\\%m_{KMnO_4}=\dfrac{0,1.158}{0,2.122,5+0,1.158}.100\%=39,2\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Hòa tan 115,3 gam hổn hợp X gồm MgCO3 và RCO3 bằng dung dịch H2SO4 loảng thu được dung dịch A, chất rắn B và 4,48 lít khí (ở đktc). Cô cạn dung dịch A thu được 12 gam muối khan. Mặt khác đem nung chất rắn B tới khối lượng không đổi thu được 11,2 lít khí CO2 (ở đktc) và chất rắn B1. Khối lượng của B1 là A. 110,3 gam B. 88,5 gam C. 83,8 gam D. 101,3 gam
Đọc tiếp
Hòa tan 115,3 gam hổn hợp X gồm MgCO3 và RCO3 bằng dung dịch H2SO4 loảng thu được dung dịch A, chất rắn B và 4,48 lít khí (ở đktc). Cô cạn dung dịch A thu được 12 gam muối khan. Mặt khác đem nung chất rắn B tới khối lượng không đổi thu được 11,2 lít khí CO2 (ở đktc) và chất rắn B1. Khối lượng của B1 là
A. 110,3 gam
B. 88,5 gam
C. 83,8 gam
D. 101,3 gam