Cho các kim loại na, mg, al lần lượt tác dụng với HCl
a) nếu ác kim loại có số mol như nhau thì kim loại nào cho nhiều khí H2
b) nếu thu dc cùng 1 lượng H2 thì khối lượng kim loại nào ít
1) Nếu lấy cùng một khối lượng kim loại Na, Al, Fe rồi cho tác dụng lần lượt với dung dịch HCl dư thì kim loại nào cho nhiều thể tích khí H2 (đktc) nhất.
\(n_{Al}=\dfrac{a}{27}\left(mol\right)\\
n_{Fe}=\dfrac{a}{56}\left(mol\right)\\
n_{Na}=\dfrac{a}{23}\left(mol\right)\\
pthh:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(\dfrac{a}{56}\) \(\dfrac{a}{56}\)
\(pthh:2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\) (2)
\(\dfrac{a}{27}\) \(\dfrac{a}{18}\)
\(pthh:Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\uparrow\) (3)
\(\dfrac{a}{23}\) \(\dfrac{a}{46}\)
nhận xét : pt (2) cho nhiều H2 nhất
gọi số mol của 3 chất = nhau là a (mol) (a>0)
\(pthh:Fe+2HCl\rightarrow FeCl_2+H_2\) (1)
a a
\(pthh:2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
a \(\dfrac{3}{2}a\)
\(pthh:Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\) (3)
a \(\dfrac{1}{2}a\)
nhận xét : phản ứng (2) cho nhiều VH2 nhiều nhất
Nếu lấy cùng một khối lượng kim loại Na, Al, Fe rồi cho tác dụng lần lượt với dung dịch HCl dư thì kim loại nào cho nhiều thể tích khí H2 (đktc) nhất
2Na + 2HCl => 2NaCl + H2
x/23________________x/46
2Al + 6HCl => 2AlCl3 + 3H2
x/27_________________x/18
Fe + 2HCl => FeCl2 + H2
x/56_______________x/56
x/18 > x/46 > x/56
=> Al cho nhiều H2 nhất
Gọi KL là x. (g) (x>0)
PTHH: Na + HCl -> NaCl + 1/2 H2
x/23___________________x/46(mol)
PTHH: 2 Al + 6 HCl -> 2 AlCl3 + 3 H2
x/27_______________________x/18(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
x/56_____________________x/56(mol)
Vì số mol tỉ lệ thuận thể tích : x/18 > x/46> x/56
=>Kim loại Al cho thể tích H2 lớn nhất.
cho các kim loại Mg,Al,Zn lần lượt tác dụng với dung dịch axit HCl.Nếu thu được cùng lượng khí H2 thì khối lượng kim loại nào cần ít nhất
Gọi x là số mol \(H_2\) thu được
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
x <----------------------------- x
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\dfrac{2}{3}x\) <---------------------------- x
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
x <----------------------------- x
có:
\(m_{Mg}=24x\) (g)
\(m_{Al}=27.\dfrac{2}{3}x=18x\) (g)
\(m_{Zn}=65x\left(g\right)\)
Vì 18x < 24x< 65x
=> Al là kim loại cần số gam ít nhất.
☕T.Lam
Cho kim loại : Zn,Alo,Fe,Mg lần lượt tác dụng với dung dịch H2SO4 loãng. Nếu cho cùng một khối lượng kim loại trên tác dụng hết với axit ,thì kim loại nào cho nhiều khí h2 nhất
Nếu cho cùng lượng 3,24g kim loại Mg hoặc Al tác dụng với axit HCl thì kim loại nào thu được nhiều khí H2 hơn, biết ngoài ra sản phẩm thu được có muối MgCl2 và AlCl3?
\(n_{Mg}=\dfrac{3,24}{24}=0,135\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
____0,135----------------->0,135
\(n_{Al}=\dfrac{3,24}{27}=0,12\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
____0,12---------------------->0,18
=> Cho Al thu được nhiều khí H2 hơn
\(n_{Mg}=\dfrac{3,24}{24}=0,135;n_{Al}=\dfrac{3,24}{27}=0,12\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\\Rightarrow n_{H_2}=n_{Mg}=0,135\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ \Rightarrow n_{H_2}=1,5n_{Al}=0,18\left(mol\right)\\ Vì:n_{H_2\left(Al\right)}>n_{H_2\left(Mg\right)}\\ \Rightarrow V_{H_2\left(Al\right)}>V_{H_2\left(Mg\right)}\)
Bài 1:
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
b, Giả sử: mZn = mAl = a (g)
\(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=\dfrac{a}{65}\left(mol\right)\\n_{Al}=\dfrac{a}{27}\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2\left(1\right)}=n_{Zn}=\dfrac{a}{65}\left(mol\right)\\n_{H_2\left(2\right)}=n_{Al}=\dfrac{a}{27}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2\left(1\right)}< n_{H_2\left(2\right)}\)
Vậy: Al cho nhiều khí H2 hơn.
c, Giả sử: nH2 (1) = nH2 (2) = b (mol)
Theo PT: \(\left\{{}\begin{matrix}n_{Zn}=n_{H_2\left(1\right)}=b\left(mol\right)\\n_{Al}=n_{H_2\left(2\right)}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=65b\left(g\right)\\m_{Al}=27b\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{Zn}>m_{Al}\)
Vậy: Khối lượng Al đã pư nhỏ hơn.
Bài 2:
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
a, Ta có: \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,1}{1}\), ta được Fe dư.
Theo PT: \(n_{Fe\left(pư\right)}=n_{H_2SO_4}=0,1\left(mol\right)\)
\(\Rightarrow n_{Fe\left(dư\right)}=0,1\left(mol\right)\Rightarrow m_{Fe\left(dư\right)}=0,1.56=5,6\left(g\right)\)
b, Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Bạn tham khảo nhé!
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
a) Phương trình phản ứng:
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4loãng → FeSO4 + H2
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2
b) Giả sử cho cùng một khối lượng là a g kim loại kẽm sắt và nhôm
Zn + H2SO4 → ZnSO4 + H2 (1)
Fe + H2SO4loãng → FeSO4 + H2 (2)
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2 (3)
Ta có 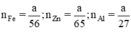
Theo pt nH2 (1) = nZn = 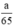 mol
mol
nH2 (2) = nFe = 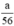 mol
mol
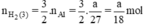
Như vậy ta nhận thấy 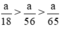 ⇒ nH2 (3) > nH2 (2) > nH2 (1)
⇒ nH2 (3) > nH2 (2) > nH2 (1)
Như vậy cho cùng một lượng kim loại tác dụng với axit H2SO4 loãng dư thì nhôm cho nhiều khí hidro hơn, sau đó đến sắt và ít nhất là kẽm
c) Nếu thu được cùng một lượng khí hidro thì khối lượng kim loại ít nhất là nhôm, sau đó đến sắt, cuối cùng là kẽm.
Cho các kim loại : kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a, Viết các phương trình phản ứng
b, Cho cùng một khối lượng các kim loại trên tác dụng hết với axit thì kim loại nào cho nhiều khí hidro nhất ?
c, Nếu thu được cùng một thể tích khí hidro thì khối lượng kim loại nào dùng cho phản ứng là nhỏ nhất ?
giúp mình nhé các bạn ?
Bài 3/ Người ta điều chế khí H2 bằng phản ứng sau:
1/ Al + HCl → AlCl3 + H2
2/ Zn + HCl → ZnCl2 + H2
a. Mỗi phản ứng trên đều thu được 13,44 lít khí H2 (ở đktc) thì khối
lượng kim loại nào cần phản ứng ít hơn?
b. Nếu lấy cùng một khối lượng kim loại Al hoặc Zn cho phản ứng, thì
phản ứng nào cho số mol H2 nhiều hơn?