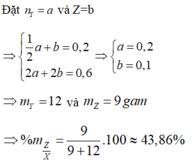Hỗn hợp A(gồm 2 KL X và Y có hóa trị lần lượt là II,III) chia làm 2 phaand bằng nhau :
Phần 1 : hòa tan hết trong dd axit sunfuric thì thấy tạo ra 4.48 lit khí H2 đo ĐKTC
Phần 2 : Đốt cháy hoàn toàn trong khí Oxi thì thu được 7.1 gam hh 2 oxit
a) tính KL hh A
b) Cho biết X có NTK bé hơn Y lad 3Đvc và số mol X bằng 1/2 số mol Y .Tìm X và Y

Những câu hỏi liên quan
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một t/d hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối lượng của Z trong hh X lần lượt là A. HOOC-CH2-COOH và 70,87% B. HOOC-CH2-COOH và 54,88%. C. HOOC-COOH và 60,00% D. HOOC-COOH và 42,86%.
Đọc tiếp
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một t/d hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối lượng của Z trong hh X lần lượt là
A. HOOC-CH2-COOH và 70,87%
B. HOOC-CH2-COOH và 54,88%.
C. HOOC-COOH và 60,00%
D. HOOC-COOH và 42,86%.
Đáp án D
Vì 2 Axit có chung số C nên gọi số C là số Cacbon trong mỗi Axit.
(C ≥ 2 vì Z là Axit 2 chức)
+Phần 1:
nH2 = 0,2 ⇒ nCOOH/X = 0,2 . 2 = 0,4
⇒ nY + 2nZ = nCOOH/X = 0,4 (1)
+Phần 2:
nCO2 = C.( nY + nZ ) = 26,4 : 44 = 0,6 (2)
Với C = 2 ⇒ nY = 0,2 ; nZ = 0,1.
Y là CH3COOH và Z là (COOH)2
⇒ %mZ = 0,1 . 90 : (0,1.90 + 0,2.46) = 42,86%
Với C = 3 ⇒ nY = 0 ; nZ = 0,2 ( vô lí)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trắm về khối lượng của Z trong hỗn hợp X lần lượt là A. HOOCCOOH và 42,86% B. HOOCCOOH và 60,00% C. HOOCCH2COOH và 70,87% D. HOOCCH2COOH và 54,88%
Đọc tiếp
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trắm về khối lượng của Z trong hỗn hợp X lần lượt là
A. HOOCCOOH và 42,86%
B. HOOCCOOH và 60,00%
C. HOOCCH2COOH và 70,87%
D. HOOCCH2COOH và 54,88%
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối lượng của Z trong hỗn hợp X lần lượt là A. HOOC-CH2-COOH và 70,87%. B. HOOC-COOH và 60,00%. C. HOOC-CH2-COOH và 54,88%. D. HOOC-COOH và 42,86%.
Đọc tiếp
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối lượng của Z trong hỗn hợp X lần lượt là
A. HOOC-CH2-COOH và 70,87%.
B. HOOC-COOH và 60,00%.
C. HOOC-CH2-COOH và 54,88%.
D. HOOC-COOH và 42,86%.
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối lượng của Z trong hỗn hợp X lần lượt là A. HOOCCOOH và 42,86%. B. HOOCCOOH và 60,00%. C. HOOCCH2COOH và 70,87%. D. HOOCCH2COOH và 54,88%.
Đọc tiếp
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối lượng của Z trong hỗn hợp X lần lượt là
A. HOOCCOOH và 42,86%.
B. HOOCCOOH và 60,00%.
C. HOOCCH2COOH và 70,87%.
D. HOOCCH2COOH và 54,88%.
Đáp án : A
Giả sử Y, Z có n nguyên tử C; nY = y ; nZ = z mol
Theo đề bài => nY + 2nZ = 2nH2
<=> y + 2z = 0,4
n.(nY + nZ) = nCO2 = 0,6
<=> n(y + z) = 0,6
=> z = 0,4 - 0 , 6 n .
Mà 0 < z < 0,2
=> 1,5 < n < 3 => n = 2
Do đó, z = 0,1 ; y = 0,2.
Hai axit là CH3COOH và HOOC-COOH
% HOOC-COOH = 0 , 1 . 90 0 , 2 . 60 + 0 , 1 . 90 = 42,86%
Đúng 0
Bình luận (0)
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối lượng của Z trong hỗn hợp X lần lượt là: A. HOOC - CH2 - COOH và 70,87% B. HOOC - CH2 - COOH và 54,88% C. HOOC - COOH và 60% D. HOOC - COOH và 42,86%
Đọc tiếp
Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc). Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối lượng của Z trong hỗn hợp X lần lượt là:
A. HOOC - CH2 - COOH và 70,87%
B. HOOC - CH2 - COOH và 54,88%
C. HOOC - COOH và 60%
D. HOOC - COOH và 42,86%
Lời giải
n H 2 = 0 , 2 ( m o l ) ⇒ n C O O H = 2 n H 2 = 0 , 04 ( m o l ) ⇒ 0 , 2 < n a x i t < 0 , 4 n C O 2 = 0 , 6 ( m o l ) ⇒ 1 , 5 < M ¯ a x i t < 3 ⇒ c ả 2 a x i t đ ề u c ó 2 n g u y ê n t ử C t r o n g p h â n t ử
=> Y là CH3COOH; Z là (HCOOH)2
Xét trong mỗi phần lại có:
n a x i t = n C O 2 2 0 , 3 ( m o l )
Gọi số mol Y, Z trong mỗi phần là y, z(mol) .
⇒ y + z = 0 , 3 y + 2 z = 0 , 4 ⇔ y = 0 , 2 z = 0 , 1
Vậy %mZ = 42,86%
Đáp án D.
Đúng 0
Bình luận (0)
Chia 10 gam hỗn hợp gồm 2 kim loại A và B có hóa trị không đổi thành 2 phần bằng nhau. Phần 1 đốt cháy hoàn toàn V lít khí O2 và thu được 5,32 gam hỗn hợp gồm 2 ôxít. Phần còn lại hòa tan trong dung dịch HCl dư thu được V' lít khí H2 thoát ra và m gam muối clorua. Tính V, V' và m. Biết các khí đo ở điều kiện tiêu chuẩn.
Hỗn hợp X gồm Zn, Al, Mg có khối lượng 22,1g được chia thành hai phần đều nhau. Đốt cháy hoàn toàn phần 1 trong khí oxi, sau phản ứng thu được 18,25g hỗn hợp chất rắn. Phần 2 đem hòa tan hết trong dung dịch axit sunfuric loãng, dư thoát ra V lít khí (đktc) và thu được dung dịch Y. Đun cạn dung dịch Y cho nước bay hét còn lại m gam chất rắn . tính V và m
Ta có: m1 = m2 = 11,05 (g)
Phần 1:
PT: \(2Zn+O_2\underrightarrow{t^o}2ZnO\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
Theo ĐLBT KL, có: mKL + mO2 = m oxit
⇒ mO2 = 18,25 - 11,05 = 7,2 (g)
\(\Rightarrow n_{O_2}=\dfrac{7,2}{32}=0,225\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Zn}+\dfrac{3}{4}n_{Al}+\dfrac{1}{2}n_{Mg}=0,225\left(mol\right)\)
\(\Rightarrow n_{Zn}+\dfrac{3}{2}n_{Al}+n_{Mg}=0,45\left(1\right)\)
Phần 2:
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}+n_{Mg}\left(2\right)\)
Từ (1) và (2) \(\Rightarrow n_{H_2}=0,45\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,45.22,4=10,08\left(l\right)\)
Theo PT: \(n_{H_2SO_4}=n_{H_2}=0,45\left(mol\right)\)
Theo ĐLBT KL, có: mKL + mH2SO4 = m muối + mH2
⇒ m chất rắn khan = m muối = 11,05 + 0,45.98 - 0,45.2 = 54,25 (g)
Bạn tham khảo nhé!
Đúng 0
Bình luận (0)
Hỗn hợp X gồm ancol và một axit hữu cơ. Chia X thành 3 phần bằng nhau: - Cho phần 1 tác dụng hết với Na thu được 3,36 lít khí không màu (đktc) - Đốt cháy hoàn toàn phần 2 thu được 39,6 gam CO2 - Thực hiện phản ứng este hóa phần 3 thu được este Y. Đốt cháy hoàn toàn 15,3 gam Y thấy tạo thành 16,8 lít CO2 (đktc) và 13,5 gam H2O. Số CTCT có thể có của Y là: A. 4. B. 6. C. 8. D. 9.
Đọc tiếp
Hỗn hợp X gồm ancol và một axit hữu cơ. Chia X thành 3 phần bằng nhau:
- Cho phần 1 tác dụng hết với Na thu được 3,36 lít khí không màu (đktc)
- Đốt cháy hoàn toàn phần 2 thu được 39,6 gam CO2
- Thực hiện phản ứng este hóa phần 3 thu được este Y. Đốt cháy hoàn toàn 15,3 gam Y thấy tạo thành 16,8 lít CO2 (đktc) và 13,5 gam H2O.
Số CTCT có thể có của Y là:
A. 4.
B. 6.
C. 8.
D. 9.
Đáp án B
Khi đốt cháy 15,3 gam Y ta có:
n C O 2 = 0 , 75 ( m o l ) ; n H 2 O = 0 , 75 ( m o l )
=> este no, đơn chức, mạch hở
=> ancol và axit cũng no, đơn chức, mạch hở
Bảo toàn khối lượng ta có:
m e s t e = m C + m H + m O = 12 n C O 2 + 2 n H 2 O + 16 n ( O t r o n g e s t e ) ⇒ n ( O t r o n g e s t e ) = 0 , 3 ( m o l ) ⇒ n e s t e = 0 , 15 ( m o l )
=> este có CTPT là C5H10O2
Xét phần 1 có: n H 2 = 0 , 15 ( m o l ) .
Vì axit và ancol đơn chức ⇒ n a x i t + n a n c o l = 0 , 3 ( m o l )
Xét phần 2: n C O 2 = 0 , 9 ( m o l ) ⇒ C ¯ X = 3
=>trong X một chất có 4 nguyên tử C, một chất có 1 nguyên tử C trong phân tử.
=>Các CTCT phù hợp của Y là:
H C O O C H 2 ( C H 2 ) 2 C H 3 ; H C O O C H 2 ( C H 3 ) C H 2 C H 3 ; H C O O C H 2 ( C H 3 ) ( C H 3 ) - C H 3 ; H C O O C H 2 - C H ( C H 3 ) - C H 3 ; C H 3 ( C H 2 ) 2 C O O C C H 3 ; C H 3 - C H ( C H 3 ) - C O O C C H 3
Chú ý: Bài toán chỉ cho rằng phần 3 thực hiện este hóa thu được este Y chứ không nói rằng khối lượng este trong phần 3 là 15,3 gam. Nếu bạn nào ngộ nhận khối lượng este là 15,3 gam sẽ thấy các số liệu bên trên của phần 1 và phần 2 không thỏa mãn.
Đúng 0
Bình luận (0)
Hỗn hợp X gồm axit Y đơn chức và axit Z đa chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần 1 tác dung với Na, sinh ra 4,48 lít khí H2 (đktc). Đốt cháy hoàn toàn phần 2, sinh ra 26,4g CO2. Công thức cấu tạo thu gọn và phần trăm khối lượng của Z trong hỗn hợp X là: A. HOOC–CH2–COOH; 70,87% B. HOOC–CH2–COOH; 54,88% C. HOOC–COOH; 60% D. HOOC–COOH; 42,86%
Đọc tiếp
Hỗn hợp X gồm axit Y đơn chức và axit Z đa chức (Y, Z có cùng số nguyên tử cacbon). Chia X thành hai phần bằng nhau. Cho phần 1 tác dung với Na, sinh ra 4,48 lít khí H2 (đktc). Đốt cháy hoàn toàn phần 2, sinh ra 26,4g CO2. Công thức cấu tạo thu gọn và phần trăm khối lượng của Z trong hỗn hợp X là:
A. HOOC–CH2–COOH; 70,87%
B. HOOC–CH2–COOH; 54,88%
C. HOOC–COOH; 60%
D. HOOC–COOH; 42,86%