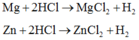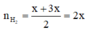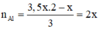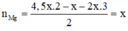Hỗn hợp X gồm Na, Al, Mg. Tiến hành 3 thí nghiệm sau: Thí nghiệm 1: Cho m gam X vào nước dư thu được V lít khí. Thí nghiệm 2: Cho 2m gam X vào dung dịch NaOH dư thu được 3,5V lít khí. Thí nghiệm 3: Hòa tan 4m gam X vào dung dịch HCl dư thu được 9V lít khí. Các thể tích đều đo ở đktc và coi như Mg không tác dụng với nước và kiềm. Phát biểu nào sau đây là đúng ? A. Số mol Al gấp 1,5 lần số mol Mg B. Trong X có 2 kim loại có số mol bằng nhau. C. Ở thí nghiệm 1, Al bị hòa tan hoàn toàn D. Phần t...
Đọc tiếp
Hỗn hợp X gồm Na, Al, Mg. Tiến hành 3 thí nghiệm sau:
Thí nghiệm 1: Cho m gam X vào nước dư thu được V lít khí.
Thí nghiệm 2: Cho 2m gam X vào dung dịch NaOH dư thu được 3,5V lít khí.
Thí nghiệm 3: Hòa tan 4m gam X vào dung dịch HCl dư thu được 9V lít khí.
Các thể tích đều đo ở đktc và coi như Mg không tác dụng với nước và kiềm. Phát biểu nào sau đây là đúng ?
A. Số mol Al gấp 1,5 lần số mol Mg
B. Trong X có 2 kim loại có số mol bằng nhau.
C. Ở thí nghiệm 1, Al bị hòa tan hoàn toàn
D. Phần trăm khối lượng của Na là 23,76%.