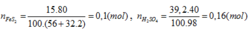Qúa trình sản xuất axit H2SO4 từ quặng pirit diễn ra 3 giai đoạn theo sơ đồ sau:
FeS2 \(\rightarrow\) SO2 \(\rightarrow\) SO3 \(\rightarrow\) H2SO4
Hiệu suất mỗi giai đoạn lần lượt là 70%, 80%, 90%. Hỏi từ 250 tấn quặng pirit chứa 60% FeS2 có chế được bao nhiêu tấn dung dịch H2SO4 98%