Cho 13,5 gam AL tác dụng với 250gam dung dịch H2SO4 31,36% thu được V lít khí và dung dịch A .
a) Tính V ( đktc)
b) Tính nồng độ phần trăm của các chất trong A
Cho 16,2 g Al tác dụng vừa đủ với dung dịch hỗn hợp H2SO4 6,694% và HCl x%. Sau phản ứng thu được V lít khí H2 (đktc) và dung dịch A trong đó nồng độ phần trăm của muối Al2(SO4)3 bằng 7,6%. a. Tìm V, x. b. Tính nồng độ phần trăm AlCl3 dung dịch A.
a) 2Al + 6HCl -> 2AlCl3 + 3H2
Al2O3 + 6HCl -> 2AlCl3 + 3H2O
nH2 = 0,15mol => nAl=0,1mol => mAl=2,7g; mAl2O3 = 10,2g => nAl2O3 = 0,1mol
=>%mAl=20,93% =>%mAl2O3 = 79,07%
b) nHCl = 0,1.3+0,1.6=0,9 mol=>mHCl(dd)=100g
mddY=12,9+100-0,15.2=112,6g
mAlCl3=22,5g=>C%=19,98%
Cho 5,1 gam hỗn hợp Al và Mg tác dụng với lượng vừa đủ dung dịch H2SO4 9,8%, sau phản ứng thu được 5,6 lít khí H2 (ở đktc)
(a) Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu.
(b) Tính nồng độ phần trăm của dung dịch X
a)\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: x 1,5x
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}27x+24y=5,1\\1,5x+y=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{0,1.27.100\%}{5,1}=52,94\%;\%m_{Mg}=100-52,94=47,06\%\)
b)
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: 0,1 0,15 0,05
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: 0,1 0,1 0,1
\(m_{ddH_2SO_4}=\dfrac{\left(0,1+0,15\right).98.100}{9,8}=250\left(g\right)\)
mdd sau pứ = 5,1+250-0,15.2 = 254,8(g)
\(C\%_{ddAl_2\left(SO_4\right)_3}=\dfrac{0,05.342.100\%}{254,8}=6,71\%\)
\(C\%_{ddMgSO_4}=\dfrac{0,1.120.100\%}{254,8}=4,71\%\)
Câu 5: Cho 5,1 gam hỗn hợp Al và Mg tác dụng với lượng vừa đủ dung dịch H2SO4 9,8%, sau phản ứng thu được 5,6 lít khí H2 (ở đktc) a. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu. b. Tính nồng độ phần trăm của dung dịch X. Giúp mình với các b ơi
\(a.n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ Đặt:\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ \rightarrow\left\{{}\begin{matrix}27a+24b=5,1\\1,5a+b=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \left\{{}\begin{matrix}\%m_{Al}=\dfrac{27.0,1}{5,1}.100\approx52,941\%\\\%m_{Mg}\approx47,059\%\end{matrix}\right.\)
\(b.m_{ddH_2SO_4}=\dfrac{0,25.98.100}{9,8}=250\left(g\right)\\ m_{ddsau}=m_{Al,Mg}+m_{ddH_2SO_4}-m_{H_2}=5,1+250-0,25.2=254,6\left(g\right)\\ C\%_{ddAl_2\left(SO_4\right)_3}=\dfrac{0,05.342}{254,6}.100\approx6,716\%\\ C\%_{ddMgSO_4}=\dfrac{0,1.120}{254,6}.100\approx4,713\%\)
Bài 2: Hòa tan hoàn toàn 8,64 gam Al trong 365 gam dung dịch HCl 10% thu được dung dịch Y và V lít khí H2 (đktc).
a. Tính V
b. Xác định chất tan trong dung dịch Y. Cô cạn dung dịch Y thu được m gam chất rắn. Tính m.
c. Tính nồng độ phần trăm các chất tan trong dung dịch Y.
a) \(n_{Al}=\dfrac{8,64}{27}=0,32\left(mol\right)\)
\(n_{HCl}=\dfrac{365.10\%}{36,5}=1\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
Xét tỉ lệ \(\dfrac{0,32}{2}< \dfrac{1}{6}\) => Al hết, HCl dư
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,32-->0,96---->0,32--->0,48
=> \(V_{H_2}=0,48.22,4=10,752\left(l\right)\)
b) Trong Y chứa AlCl3 và HCl dư
\(m_{AlCl_3}=0,32.133,5=42,72\left(g\right)\)
c) mdd sau pư = 8,64 + 365 - 0,48.2 = 372,68 (g)
\(\left\{{}\begin{matrix}C\%\left(AlCl_3\right)=\dfrac{42,72}{372,68}.100\%=11,463\%\\C\%\left(HCldư\right)=\dfrac{\left(1-0,96\right).36,5}{372,68}.100\%=0,392\%\end{matrix}\right.\)
Cho 12 gam hỗn hợp hai kim loại Fe, Cu tác dụng vừa đủ với dung dịch HNO3 63%. Sau phản ứng thu được dung dịch A và 11,2 lít khí NO2 duy nhất (đktc). Tính nồng độ phần trăm của các chất có trong dung dịch A.
A. 36,66% và 28,48%.
B. 27,19% và 21,12%.
C. 27,19% và 72,81%.
D. 78,88% và 21,12%.
Ta có thể viết 2 phản ứng:
Fe+6HNO3 ⇒ Fe(NO3)3 +3NO2 +3H2O
Cu+4HNO3 ⇒ Cu(NO3)2 +2NO2 +2H2O
Có
![]()
Quan sát các phản ứng nhận thấy:
![]()
![]()
Dung dịch A thu được chứa Fe(NO3)3 và Cu(NO3)2.
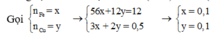
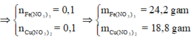
Áp dụng định luật bảo toàn khối lượng ta có:
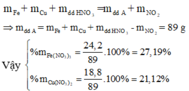
Đáp án B.
Hoà tan 4,6 gam Na vào 100 ml nước thu được dung dich A và V lít khí H2 (đktc).
a) Tính giá trị của V?
b) Tính nồng độ mol của dung dịch A?
c) Tính nồng độ phần trăm của chất tan trong dung dịch A?
a) nNa = 4,6/23 = 0,2 (mol)
PTHH: 2Na + 2H2O -> 2NaOH + H2
Mol: 0,2 ---> 0,2 ---> 0,2 ---> 0,1
VH2 = 0,1 . 22,4 = 2,24 (l)
b) CMNaOH = 0,2/0,1 = 2M
c) mH2O = 100 . 1 = 100 (g)
mNaOH = 0,2 . 40 = 8 (g)
mH2 = 0,1 . 2 = 0,2 (g)
mdd = 100 + 8 - 0,2 = 107,8 (g)
C%NaOH = 8/107,8 = 7,42%
Hoà tan 4,6 gam Na vào 100 ml nước thu được dung dich A và V lít khí H2 (đktc).
a) Tính giá trị của V?
b) Tính nồng độ mol của dung dịch A?
c) Tính nồng độ phần trăm của chất tan trong dung dịch A?
cho 5,6 gam sắt phản ứng vừa đủ với 200 gam dung dịch axit h2so4 loãng b% sau phản ứng thu được dung dịch b và v lít (đktc) a/ viết phương trình phản ứng
b/ tính V
c/ tính B
d/ tính nồng độ phần trăm của chất tan trong dung dịch B
a, \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b, \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c, \(n_{H_2SO_4}=n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{0,1.98}{200}.100\%=4,9\%=b\)
d, \(n_{FeSO_4}=n_{Fe}=0,1\left(mol\right)\)
Ta có: m dd sau pư = 5,6 + 200 - 0,1.2 = 205,4 (g)
\(\Rightarrow C\%_{FeSO_4}=\dfrac{0,1.152}{205,4}.100\%\approx7,4\%\)
a/ Viết phương trình phản ứng:
Fe + H2SO4 -> FeSO4 + H2
b/ Tỉnh V:
Vì số mol của sắt bằng số mol axit H2SO4, ta có:
5,6 g Fe = một số mol H2SO4 x khối lượng mol Fe 200 g dung dịch H2SO4 = một số mol H2SO4 x khối lượng mol H2SO4
Từ đó, suy ra số mol axit H2SO4 trong dung dịch ban đầu:
n(H2SO4) = 5,6 / (55,85 g/mol) = 0,1 mol
Theo phương trình phản ứng, mỗi mol axit H2SO4 tác dụng với một mol sắt, sinh ra một mol khí H2. Vậy, số mol khí H2 sinh ra trong phản ứng cũng bằng 0,1 mol.
Theo định luật Avogadro, một mol khí ở điều kiện tiêu chuẩn chiếm thể tích là 22,4 lít. Vậy, số lít khí H2 sinh ra trong phản ứng là:
V = 0,1 mol x 22,4 l/mol = 2,241
Vậy, V = 2,24 lít.
c/ Tính B:
• Theo định luật bảo toàn khối lượng, khối lượng của sản phẩm thu được bằng khối lượng của chất đầu vào. Do đó, khối lượng dung dịch sau phản ứng cũng bằng 200 g. o Ta đã tính được số mol H2SO4
trong dung dịch ban đầu là 0,1 mol.
Sau phản ứng, số mol H2SO4 còn
lại trong dung dịch là: n(H2SO4) = n(H2SO4 ban đầu) -
n(H2 sinh ra) = 0,1 - 0,1 = 0 mol
• Vì vậy, dung dịch sau phản ứng chỉ còn chứa FeSO4 và H2O. Khối lượng của FeSO4