khử hoàn toàn á (g) Fe2O3 bằng khí H2 dư thu được b(g) kim loại Fe đốt cháy hết lượng Fe này trong khí O2 dư thu dc 23,2g Fe3O4 . hãy viết pthh và tính a,b

Những câu hỏi liên quan
khử hoàn toàn 16 gam fe2O3 bằng khí H2 dư thu được b (g) kim loại Fe . Đốt cháy hết lượng Fe này trong khí O2 thì thu đươc 23.2 g oxit sắt từ. Hãy viết các PTHH và tìm a và b
1,
n: 0,1 0,2
vậy m = 0,2. 162,5 = 32,5 (g)
Đúng 0
Bình luận (0)
Khử hoàn toàn a(g) Fe2O3 bằng khí H2 dư thu được b(g) kim loại Fe. Đốt cháy hết lượng Fe này trong khí O2 dư thu được 23,2 g oxit sắt từ. Hãy viết các PTHH. Tính a và b
\(Fe_2O_3\left(0,15\right)+3H_2\rightarrow2Fe\left(0,3\right)+3H_2O\)
\(3Fe\left(0,3\right)+2O_2\rightarrow Fe_3O_4\left(0,1\right)\)
\(n_{Fe_3O_4}=\frac{23,2}{232}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,15.160=24\left(g\right)\)
\(\Rightarrow m_{Fe}=0,3.56=16,8\left(g\right)\)
Đúng 0
Bình luận (0)
Ta có: \(n_{Fe_3O_4}=\frac{23,2}{232}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 -to-> 2Fe + 3H2O (1)
3Fe + 2O2 -to-> Fe3O4 (2)
Theo các PTHH và đề bài, ta có:
\(n_{Fe\left(2\right)}=3.n_{Fe_3O_4\left(2\right)}=3.0,1=0,3\left(mol\right)\)
\(n_{Fe\left(1\right)}=n_{Fe\left(2\right)}=0,3\left(mol\right)\)
\(n_{Fe_2O_3\left(1\right)}=\frac{n_{Fe\left(1\right)}}{2}=\frac{0,3}{2}=0,15\left(mol\right)\)
Ta có: \(a=m_{Fe_2O_3\left(1\right)}=0,15.160=24\left(g\right)\)
\(b=m_{Fe\left(1\right)}=0,3.56=16,8\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 16,8g Fe trong bình chứa O2 dư thu được sắt từ oxit (Fe3O4)
A.Hãy viết phương trình phản ứng xảy ra
B.Tính khối lượng FeO4 thu được?
C.Khử hoàn toàn lượng sắt từ oxit trên bằng 44,8 lít khí H2 ở đktc thành sắt kim loại ở nhiệt độ cao,sau phản ứng chất nào dư và dư bao nhiêu gam?
nFe = 16,8 : 56 = 0,3 (mol)
pthh :3 Fe + 2O2 -t--> Fe3O4
0,3--------------> 0,1 (mol)
=> mFe3O4 =0,1 . 232 = 23,2(G)
nH2 = 44,8 : 22,4 = 2 (g)
pthh : Fe3O4 + H2 -t--> Fe + H2O
LTL : 0,1 / 1 < 2 /1
=> H2 du
nH2 (pu) = nFe3O4 = 0,1 (mol)
=> nH2 (d) = 2-0,1 = 1,9 (mol)
mH2 (d) = 1,9 . 2 = 3,8 (g)
Đúng 3
Bình luận (2)
Đốt cháy 2,8g Fe trong bình chứa 22,4 khí O2 ở điều kiện tiêu chuẩn , thu được Fe3O4 a/ viết pthh b / cho biết chất nào dư sau phản ứng bao nhiêu g? c/ tính mFe3O4 thu được (Fe=56,O=16)
Xem chi tiết
nFe = 2.8/56 = 0.05 (mol)
nO2 = 22.4 / 22.4 = 1 (mol)
3Fe + 2O2 -to-> Fe3O4
0.05__1/30______1/60
mO2 (dư) = ( 1 - 1/30) * 32 = 30.93 (g)
mFe3O4 = 1/60 * 232 = 3.867 (g)
Đúng 3
Bình luận (0)
a/ \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b/ Ta có: \(n_{Fe}=\dfrac{2.8}{56}=0.05\left(mol\right)\)
\(n_{O_2}=\dfrac{22.4}{22.4}=1\left(mol\right)\)
Ta có: \(\dfrac{n_{Fe\left(bra\right)}}{n_{Fe\left(pt\right)}}=\dfrac{0.05}{3}=0.016< \dfrac{n_{O_2\left(bra\right)}}{n_{O_2\left(pt\right)}}=\dfrac{1}{2}=0.5\)
=> Oxi phản ứng dư
mO2 dư = (1 - 1/30) . 32 = 30.93 (g)
mFe3O4 = 1/60 . 232 = 3.867 (g)
Đúng 1
Bình luận (0)
a) 3Fe + 2O2 t o Fe3O4
b) nFe = \(\dfrac{2,8}{56}\)= 0,05 (mol)
nO2= \(\dfrac{22,4}{22,4}\)= 1 (mol)
3Fe +2 O2 toFe3O4
\(\dfrac{3Fe}{2O_2}=\dfrac{0,05}{1}\Leftrightarrow\dfrac{Fe}{O_2}=\dfrac{0,1}{3}\)Vậy O2 dư
3Fe +2 O2 toFe3O4
(mol) 0,05-> \(\dfrac{1}{30}\)-------> \(\dfrac{1}{60}\)
mO2dư= (1-\(\dfrac{1}{30}\)). 32 = 30,93 (g)
c) mFe3O4=\(\dfrac{1}{60}\) . 232 = 3,87 (g)
Đúng 2
Bình luận (0)
Khử hoàn toàn m gam hỗn hợp các oxit FeO, Fe2O3 và Fe3O4 thu được khí CO2 và Fe. Hấp thụ khí CO2 bằng nước vôi trong dư thu được a gam kết tủa. Hòa tan hoàn toàn Fe trong dung dịch HCl dư thu được V lít H2 (đktc). Mối liên hệ giữa m, V và a là A. m 5V + 1,6a B. m 1,25V + 0,16a C. m 2,5V + 0,16a D. m 2,5V + 1,6a
Đọc tiếp
Khử hoàn toàn m gam hỗn hợp các oxit FeO, Fe2O3 và Fe3O4 thu được khí CO2 và Fe. Hấp thụ khí CO2 bằng nước vôi trong dư thu được a gam kết tủa. Hòa tan hoàn toàn Fe trong dung dịch HCl dư thu được V lít H2 (đktc). Mối liên hệ giữa m, V và a là
A. m = 5V + 1,6a
B. m = 1,25V + 0,16a
C. m = 2,5V + 0,16a
D. m = 2,5V + 1,6a
Khử hoàn toàn m gam hỗn hợp các oxit FeO, Fe2O3 và Fe3O4 thu được khí CO2 và Fe. Hấp thụ khí CO2 bằng nước vôi trong dư thu được a gam kết tủa. Hòa tan hoàn toàn Fe trong dung dịch HCl dư thu được V lít H2 (đktc). Mối liên hệ giữa m, V và a là: A. m 5V + 1,6a B. m 1,25V + 0,16a C. m 2,5V + 0,16a D. m 2,5V + 1,6a
Đọc tiếp
Khử hoàn toàn m gam hỗn hợp các oxit FeO, Fe2O3 và Fe3O4 thu được khí CO2 và Fe. Hấp thụ khí CO2 bằng nước vôi trong dư thu được a gam kết tủa. Hòa tan hoàn toàn Fe trong dung dịch HCl dư thu được V lít H2 (đktc). Mối liên hệ giữa m, V và a là:
A. m = 5V + 1,6a
B. m = 1,25V + 0,16a
C. m = 2,5V + 0,16a
D. m = 2,5V + 1,6a
Đáp án C
(FeO, Fe2O3, Fe3O4) + CO → Fe + CO2
CO2 + Ca(OH)2 dư → a gam ↓ CaCO3
Fe + HCl dư → V lít H2↑
• nFe = nH2 = V/22,4 mol; nCO = nCO2 = a/100 mol.
Theo bảo toàn khối lượng mhỗn hợp oxit = mFe + mCO2 - mCO
→ m = V/22,4 × 56 + a/100 × 44 - a/100 × 28 = 2,5V - 0,16a
Đúng 0
Bình luận (0)
13/ Cần 6,72 g H2(đktc) để khử hết 16 g oxit của kim loại hóa trị III.XĐ CTHH của oxit
14/ Người ta dùng H2(dư) để khử m g Fe2O3 và thu được n g Fe. Cho lượng Fe này tác dụng với dd H2SO4 (dư ) thu đuợc FeSO4 và 2,8 (l) H2. (đktc) a/ tính m b/ tính n
Câu 13:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ PTHH:R_2O_3+3H_2\underrightarrow{t^o}2R+3H_2O\\ Theo.pt:n_{R_2O_3}=\dfrac{1}{3}n_{H_2}=\dfrac{1}{3}.0,3=0,1\left(mol\right)\\ M_{R_2O_3}=\dfrac{16}{0,1}=160\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow2R+16.3=160\\ \Leftrightarrow R=56\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow R.là.Fe\\ CTHH:Fe_2O_3\)
Bài 14:
\(n_{H_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ PTHH:Fe+H_2SO_{4\left(loãng\right)}\rightarrow FeSO_4+H_2\uparrow\left(1\right)\\ Theo.pt\left(1\right):n_{Fe}=n_{H_2}=0,125\left(mol\right)\\ PTHH:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\left(2\right)\\ Theo.pt\left(2\right):n_{Fe_2O_3}=\dfrac{1}{3}n_{Fe}=\dfrac{1}{3}.0,125=\dfrac{1}{24}\left(mol\right)\\ m=m_{Fe_2O_3}=\dfrac{1}{24}.160=\dfrac{20}{3}\left(g\right)\\ n=n_{Fe}=0,125.56=7\left(g\right)\)
Đúng 1
Bình luận (0)
C1: Viết các PTHH để thực hiện sơ đồ chuyển hóa sau:
Fe(OH)3 - Fe2O3 - Fe - FeSO4 - FeCl2 - Fe(OH)2
C2: Hòa tan hoàn toàn 11,1 gam hỗn hợp X gồm Al và Fe bằng 1 lượng dư dd HCl, thu được 6,72 lít khí H2 (đktc)
a. Viết PTHH của các pư xảy ra và tính phần trăm khối lượng của từng chất trong X
b) Khi cho 11,1 gam X pư hết với khí Cl2(dư) thì có q mol Cl2 tham gia pư. Tính giá trị của q
c) Bằng phương pháp hóa học hãy trình bày sơ đồ tách riêng kim loại ra khỏi hỗn hợp X.
Đọc tiếp
C1: Viết các PTHH để thực hiện sơ đồ chuyển hóa sau:
Fe(OH)3 -> Fe2O3 -> Fe -> FeSO4 -> FeCl2 -> Fe(OH)2
C2: Hòa tan hoàn toàn 11,1 gam hỗn hợp X gồm Al và Fe bằng 1 lượng dư dd HCl, thu được 6,72 lít khí H2 (đktc)
a. Viết PTHH của các pư xảy ra và tính phần trăm khối lượng của từng chất trong X
b) Khi cho 11,1 gam X pư hết với khí Cl2(dư) thì có q mol Cl2 tham gia pư. Tính giá trị của q
c) Bằng phương pháp hóa học hãy trình bày sơ đồ tách riêng kim loại ra khỏi hỗn hợp X.
gvvvvvvvvvvvvvvvvvvvvvvvvvvft
Đốt cháy 5,6g bột Fe trong bình đựng O2 thu được 7,36g hỗn hợp A gồm Fe2O3, Fe3O4 và Fe. Hòa tan hoàn toàn lượng hỗn hợp A bằng dung dịch HNO3-, thu được V lít hỗn hợp khí B gồm NO và NO2. Tỉ khối của B so với H2 là 19. Thể tích V ở đktc là bao nhiêu?
MX= 19.2=38
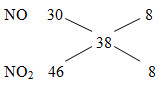
=> nN2=nNO2=x
mFe + mO = moxit
=> mO = moxit- mFe = 7,36-5,6=1,76 gam
=> nO = 0,11 mol
Fe0 →Fe3+ + 3e
0,1 0,3
O0 +2e →O2- N+5 + 3e → N+2 N+5 +1e → N+4
0,11 0,22 3x x x x
Bảo toàn e: 0,3 = 0,22+3x+x =0,22+4x =>x= 0,02
=> nkhí = 2x=0,04 mol
=> Vkhí = 0,04.22,4=0,896 lít=896 ml
Đúng 2
Bình luận (0)




























