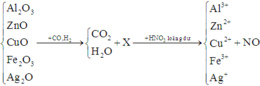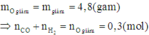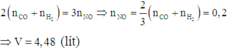Cho một luồng khí hidro đi qua bột đồng(2)oxit màu đen thu được hỗn hợp chất rắn trong đó có 6.4gam chất rắn màu đỏ. Tiếp tục cho 4.48 lít khí hidro(đktc) đi qua thì thu được một chất rắn duy nhất có màu đỏ.
a. Viết phương trình phản ứng xảy ra
b. Tính khối lượng đồng (2) oxit ban đầu.
c. Cho toàn bộ lượng chất rắn màu đỏ thu được sau 2 lần phản ứng ở trên tác dụng với 5.6 lít khí oxi, nung nóng đến khi phản ứng xảy ra hoàn toàn. Tính khối lượng các chất thu được sau phản ứng.