hoa tan hoan toan 4.59g Al bằng dd HNO3 thu duoc hh khí Z gom NO, N2O ,Z có tỉ khối so voi H2 bằng 16.75 . vay the tich cua NO va N2O trong Z lan luot la bn?

Những câu hỏi liên quan
Hòa tan 4,59 gam Al bằng dung dịch HNO3 thu được hỗn hợp khí NO và N2O có tỉ khối so với H2 bằng 16,75. Thể tích NO và N2O thu được ở đktc là: A. 2,24 lít và 6,72 lít B. 2,016 lít và 0,672 lít C. 0,672 lít và 2,016 lít D. 1,972 lít và 0,448 lít
Đọc tiếp
Hòa tan 4,59 gam Al bằng dung dịch HNO3 thu được hỗn hợp khí NO và N2O có tỉ khối so với H2 bằng 16,75. Thể tích NO và N2O thu được ở đktc là:
A. 2,24 lít và 6,72 lít
B. 2,016 lít và 0,672 lít
C. 0,672 lít và 2,016 lít
D. 1,972 lít và 0,448 lít
Hòa tan 4,59 gam Al bằng dung dịch HNO3 thu được hỗn hợp khí NO và N2O có tỉ khối so với H2 bằng 16,75. Thể tích NO và N2O thu được ở đktc là: A. 2,24 lít và 6,72 lít B. 2,016 lít và 0,672 lít C. 0,672 lít và 2,016 lít D. 1,972 lít và 0,448 lít
Đọc tiếp
Hòa tan 4,59 gam Al bằng dung dịch HNO3 thu được hỗn hợp khí NO và N2O có tỉ khối so với H2 bằng 16,75. Thể tích NO và N2O thu được ở đktc là:
A. 2,24 lít và 6,72 lít
B. 2,016 lít và 0,672 lít
C. 0,672 lít và 2,016 lít
D. 1,972 lít và 0,448 lít
Đáp án B
n A l = 0 , 17 g ọ i n N O = a n N 2 O = b c ó M ¯ = 30 a + 44 b a + b = 16 , 75 . 2 < = > a = 3 b ( 1 ) q u á t r ì n h n h ư ờ n g e :
A l o → A l + 3 + 3 e
Quá trình nhận e:

Từ (1) và (2)
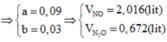
Đúng 0
Bình luận (0)
1, cho 1.84 g hon hop Fe va Cu tan het trong HNO3 du thu duoc 1.12 lit khi gom NO va NO2 co ti khoi hoi so voi hidro la 21.4 tim phan tram ve khoi luong cua Fe va Cu trong hon hop
2, cho 7.2 g Mg tac dung H2SO4dac nong thu doc dung ditch X va san pham khi A co S co the rich la 6.72 lit tim A
3, hoa tan hoan toan 0.2 mol ho hop kim Lois gom Mg,Zn ,Cu bang HNO3 du thu duoc hon hop 2 khi NO va NO2 co ti khoi hoi so voi hidro la 19 tim the tich moi khi
Câu 1) Hòa tan 4.59 gan Al bằng dd HNO3 thu đc hh khí A gồm No và N2O có tỉ khối hơi đối với H2 bằng 16.75
a) Tính V khí hh khí A
b) Trộn thêm V lít khí NO đktc vào A đc hh khí B.Tính V,biết dB/H2=16.4
Ta có :
\(M_A=\frac{m_{NO}+m_{N_2O}}{n_{NO}+n_{N_2O}}=16,75.2=33,5\)
<=> \(33,5=\frac{30n_{NO}+44n_{N_2O}}{n_{NO}+n_{N_2O}}\)
<=> \(3,5n_{NO}=10,5n_{N_2O}\)
=> \(n_{NO}=3n_{N_2O}\)
Lại có
Al0+ ----> -3e Al3+ N5+----> +3e N2+
0,17_____0,51__0,17 3a______9a____3a
2N5+----> +8e 2N1+
a_______8a____a
=> \(n_{Al}=\frac{4,59}{27}=0,17\left(mol\right)\)
Gọi a là số mol của \(N_2O\)
=> 3a___________NO
=> 9a+8a=0,51
=>a=0,03(mol)
a)=> Σnh2=0,03+0,03.3=0,12(mol)
=> Vh2=0,12.22,4=2,688(l)
b)\(M_B=16,4.2=32,8\left(\frac{gam}{mol}\right)\)
<=> \(\frac{44n_{N_2O}+30n_{NO}}{n_{N_2O}+n_{NO}}=32,8\)
<=>11,2\(n_{N_2O}\)=2,8\(n_{NO}\)
=> \(n_{NO}=4n_{N_2O}\)
mà trước khi trộn : \(n_{NO}=3n_{N_2O}\)
=> trộn thêm số mol khí \(n_{NO}=n_{N_2O}=0,03\left(mol\right)\)
=> \(V_{NO}=0,03.22,4=0,672\left(mol\right)\)
Đúng 0
Bình luận (0)
cho hon hop X gom FeO, Fe2O3, Fe3O4 voi so mol bang nhau.Lay a gam X cho phan ung voi CO ung nong sau phan ung binh con lai 16,8lit hh ran Y. Hoa tan hoan toan Y trong dung dich H2SO4 dac nong thu duoc 3,36lit SO2 duy nhat (dktc) Gia tri cua a va so mol H2SO4 da phan ung lan luot la bao nhieu?
FeO, Fe2O3 , Fe3O4 với số mol bằng nhau
coi hh ban đầu là Fe3O4 với số mol x
Y gồm Fe3O4 và Fe với số mol là x-y và 3y
Có 232(x-y)+3y*56=16.8
x-y +3y*3=0.15*2
=>x=0.08,y=0.0275
=> a=0.08*232=18.56g
H2SO4 làm 2 nhiệm vụ : tạo khí vào tạo muối
nSO2=0.15
nSO42- = 3x*3/2=0.36
=>nH2SO4=0.51
Đúng 0
Bình luận (1)
Hỗn hợp M gồm
A
l
,
A
l
2
O
3
,
F
e
3
O
4
,
C
u
O
,
F
e
v
à
C
u
trong đó oxi chiếm 20,4255% khối lượng hỗn hợp. Cho 6,72 lít khí CO (đktc) đi qua 35,25 nung...
Đọc tiếp
Hỗn hợp M gồm A l , A l 2 O 3 , F e 3 O 4 , C u O , F e v à C u trong đó oxi chiếm 20,4255%
khối lượng hỗn hợp. Cho 6,72 lít khí CO (đktc) đi qua 35,25 nung nóng, sau một thời gian thu được hỗn hợp rắn N và hỗn hợp khí X có tỉ khối so với H 2 bằng 18. Hòa tan toàn bộ N trong lượng dư dung dịch H N O 3 loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa m gam muối (không có N H 4 N O 3 ) và 4,48 lít (đktc) hỗn hợp khí Z gồm N O v à N 2 O . Tỉ khối của Z so với H 2 là 16,75Giá trị của m là
A. 96,25
B. 117,95
C. 80,75
D. 139,50
Đáp án B
Trong, đặt ![]()
![]()
![]()
=> giải hệ có x = y = 0,15 mol
![]()
![]()
![]()
![]()
![]()
![]()
![]() giải hệ có: a = 0,15 mol; b = 0,05 mol
giải hệ có: a = 0,15 mol; b = 0,05 mol
![]()
![]()
= 0,45 mol
![]()
Đúng 0
Bình luận (0)
Hoà tan 10,8g bột Al vào HNO3 dư thu được 4,76 lit hỗn hợp 2 khí N2O, NO có tỉ khối so với H2 bằng a. Tính a?
Mọi người ơi ai giúp mình với :3
$n_{Al} = \dfrac{10,8}{27} = 0,4(mol)$
Gọi $n_{N_2O} = a(mol) ; n_{NO} = b(mol)$
$n_{hh} = a + b = \dfrac{4,76}{22,4} = 0,2125(mol)$
Bảo toàn e : $8a + 3b = 0,4.3 = 1,2$
Suy ra $a = 0,1125 ; b = 0,1$
$M_{hh} = \dfrac{0,1125.44 + 0,1.30}{0,2125} = 37,41$
$d_{hh/H_2} =a = \dfrac{37,41}{2} = 18,705$
Đúng 2
Bình luận (0)
: Hòa tan hết 9 gam hh Al và Mg trong dd HNO3 thu được 2,24 lít hh N2 và N2O (đktc) có tỉ khối so với H2 = 20,4. Cô cạn dd được 65,4 gam muối. Tính % khối lượng của Al trong hh
\(\overline{M}=\dfrac{28.nN_2+44.nN_2O}{nN_2+nN_2O}=20,4.2\left(1\right)\)
\(nN_2+nN_2O=\dfrac{2,24}{22,4}=0,1\left(2\right)\)
Từ (1), (2) suy ra\(\left\{{}\begin{matrix}nN_2=0,02\\nN_2O=0,08\end{matrix}\right.\)
gọi x, y lần lượt là nAl và nMg
\(\left\{{}\begin{matrix}mhh=27x+24y=9\\3x+2y=10.0,02+8.0,08\left(BTne\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=0,12\\y=0,24\end{matrix}\right.\)
\(\%mAl=\dfrac{mAl.100\%}{mhh}=\dfrac{0,12.27.100\%}{9}=36\%\)
Đúng 0
Bình luận (0)
Cho 0,9 mol Al tan hết trong dung dịch HNO3 dư thu được V lít (đktc) hỗn hợp khí X gồm NO và N2O có tỉ khối hơi so với H2 là 20,25 (sản phẩm khử của N+5 chỉ có NO và N2O). Giá trị của V là A. 13,44. B. 8,96. C. 11,2. D. 6,72.
Đọc tiếp
Cho 0,9 mol Al tan hết trong dung dịch HNO3 dư thu được V lít (đktc) hỗn hợp khí X gồm NO và N2O có tỉ khối hơi so với H2 là 20,25 (sản phẩm khử của N+5 chỉ có NO và N2O). Giá trị của V là
A. 13,44.
B. 8,96.
C. 11,2.
D. 6,72.
Đáp án B
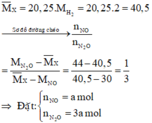
Sơ đồ phản ứng:
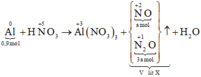
Các quá trình nhường, nhận electron:
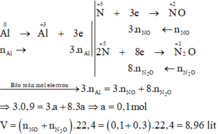
Đúng 0
Bình luận (0)



















