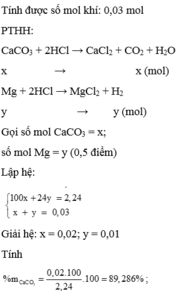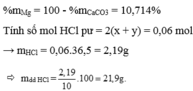Cho 5,4 gam hỗn hợp CaSO3, CaCO3, và KHSO4 phản ứng với dd HCl dư thu đươc 11,2 lít hỗn hợp khí A (đktc).Tính % về khối lượng CaCO3 trong hỗn hợp ban đầu và % về thể tích SO2 trong hỗn hợp khí A.

Những câu hỏi liên quan
Cho 21,2g hỗn hợp CaO và CaCO3 tác dụng hết với dd HCL dư thì thu được 2,24 lít khí (đktc) a Tính khối lượng mỗi chất trong hỗn hợp ban đầu b Dẫn toàn bộ lít khí thu được vào nước vôi trong dư tính khối lượng kết tủa thu được
Đọc tiếp
Cho 21,2g hỗn hợp CaO và CaCO3 tác dụng hết với dd HCL dư thì thu được 2,24 lít khí (đktc) a Tính khối lượng mỗi chất trong hỗn hợp ban đầu b Dẫn toàn bộ lít khí thu được vào nước vôi trong dư tính khối lượng kết tủa thu được
a)
$CaCO_3+ 2HCl \to CaCl_2 + CO_2 + H_2O$
$n_{CaCO_3} = n_{CO_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$m_{CaCO_3} = 0,1.100 = 10(gam)$
$m_{CaO} = 21,2 - 10 = 11,2(gam)$
b)
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,1(mol)$
$m_{kết\ tủa} = 0,1.100 = 10(gam)$
Đúng 2
Bình luận (1)
hòa tan hoàn toàn 20, 6 gam hỗn hợp 2 chất rắn là CaCO3 và CaO vào dd HCl 10%.Sau phản ứng thu được 3,36l khí ở đktc. Tính thành phần % theo khối lượng của mỗi chất rắn trong hỗn hợp ban đầu và tính khối lượng dd HCl cần dùng cho phản ứng
PTHH:
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
0,15 0,15
\(CaO+2HCl\rightarrow CaCl_2+H_2O\)
Ta có: \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,15\cdot100=15\left(g\right)\)
\(\Rightarrow m_{CaO}=20,6-15=5,6\left(g\right)\)
\(\Rightarrow\%m_{CaCO_3}=\dfrac{15\cdot100}{20,6}\approx73\%\)
\(\Rightarrow\%m_{CaO}=100\%-73\%=27\%\)
Đúng 2
Bình luận (0)
cho 1,66 gam hỗn hợp gồm 2 kim loại Fe và Al tác dụng với dd HCL dư, sau phản ứng thu được 11,2 lít khí (dktc)
a, viết PTHH
b,tính khối lượng của kim loại trong hỗn hợp ban đầu
a) Fe +2 HCl -> FeCl2 + H2
x____2x______x____x(mol)
2 Al + 6 HCl -> 2 AlCl3 + 3 H2
y____3y______y________1,5y(mol)
b) nH2= 0,05(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}56x+27y=1,66\\x+1,5y=0,05\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
=> mFe=0,02.56= 1,12(g)
mAl=0,02.27=0,54(g)
Đúng 2
Bình luận (0)
cho 35,2 gam hỗn hợp (a) gồm hai muối na2so3 và caco3 và 200 gam dung dịch hcl , phản ứng vừa đủ thu được 6,72 lít hỗn hợp khí x (đktc) và dung dịch b . tính a) thành phần % về khối lượng mỗi muối trong hỗn hợp a
b) nồng độ % của mỗi muối trong dung dịch B
Cho 30,7 gam hỗn hợp gồm kẽm và sắt tác dụng hoàn toàn với dung dịch HCl 2M, sau phản ứng thu được 11,2 lít khí ở đktc. a) Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu b) Tính thể tích dung dịch HCl đã phản ứng
a,\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: x x
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}65x+56y=30,7\\x+y=0,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Zn}=\dfrac{0,3.65.100\%}{30,7}=63,52\%;\%m_{Fe}=100\%-63,52\%=36,48\%\)
b,
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,3 0,6
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,2 0,4
nHCl = 0,6+0,4 = 1 (mol)
\(V_{ddHCl}=\dfrac{1}{2}=0,5\left(l\right)=500\left(ml\right)\)
Đúng 2
Bình luận (0)
cho 11,2 lít (đktc) hỗn hợp bao gồm CH4 và C2H4 tác dụng với dd brom dư, lượng brom đã tham gia phản ứng là 32 gam
a, viết pt phản ứng
b. tính % về thể tích mỗi khí có trong hỗn hợp ban đầu
giúp mình với ạ mình cần gấp ạ
a) \(n_{Br_2}=\dfrac{56}{160}=0,35\left(mol\right)\)
Chỉ có \(C_2H_4\) phản ứng với \(brom\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b) \(V_{C_2H_4}=0,35.2,24=7,84\left(l\right)\Rightarrow\%C_2H_4=70\%\)
\(\%CH_4=100\%-70\%=30\%\)
Đúng 2
Bình luận (1)
Cho 2,24 gam hỗn hợp G gồm: CaCO3 và Mg vào một lượng vừa đủ m gam dd HCl 10%. Sau phản ứng thu được dd A và 0,672 lít hỗn hợp khí B ở đktc. Xác định % khối lượng của các chất trong G và khối lượng dung dịch HCl đã dùng.
Nung hỗn hợp A gồm CaCO3 và CaSO3 tới phản ứng hoàn toàn thu được một chất rắn và
hỗn hợp khí B gồm SO2 và CO2.Khối lượng của hỗn hợp khí B bằng 49,6% khối lượng của hỗn
hợp A.Tính thành phần % về khối lượng của mỗi chất trong A.
Cho 18,4g hỗn hợp MgCO3 và CaCO3 phản ứng với 150g dung dịch HCl 14,6 thu được 4,48 lít khí ở đktc.
a. Tính % khối lượng mỗi chất trong hỗn hợp đầu.
b. Tính C % dung dịch sau phản ứng
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(\Rightarrow\left\{{}\begin{matrix}84\cdot n_{MgCO_3}+100\cdot n_{CaCO_3}=18,4\\n_{MgCO_3}+n_{CaCO_3}=n_{CO_2}=0,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{MgCO_3}=0,1mol\\n_{CaCO_3}=0,1mol\end{matrix}\right.\)
\(\%m_{CaCO_3}=\dfrac{0,1\cdot100}{18,4}\cdot100\%=54,35\%\)
\(\%m_{MgCO_3}=100\%-54,35\%=45,65\%\)
Đúng 1
Bình luận (0)