Hỗn hợp X gồm 2 kim loại Mg và R. Tìm kim loại R:
- Nếu cho 8 gam X vào dung dịch HCl dư thu được 4,48 lít khí (đktc)
-Nếu cho 16 gam X tác dụng vừa đủ với 11,2 lít Cl2 (đktc)
Cho 8 gam hỗn hợp A gồm Mg và kim loại R tác dụng với dung dịch HCl dư thu được 4,48 lít khí (đktc). Nếu cho 9,6 gam hỗn hợp A phản ứng với khí clo dư thì thu được 30,9 gam hỗn hợp muối. a. Xác định tên kim loại R. Biết các phản ứng hóa học đều xảy ra hoàn toàn.
Đặt a,b là số mol Mg, R trong 8 gam A. Đặt x,y là hoá trị thấp cao của R
mA = 24a + bR = 8 (1)
Với HCl -> 2a + bx = 0,2 .2 (2)
Trong 9,6 gam A ( gấp 1,2 lần 8 gam A ) chứa 1,2a và 1,2b mol Mg, R
Với Cl2 -> 2 . 1,2a + 1,2by = 2 ( 30,9 - 9,6 ) / 71 (3)
Với 1 ≤ x ≤ y ≤ 3 -> Chọn x = 2; y = 3
(2)(3) -> a = b = 0,1
(1) -> R= 56 -> = Fe
hỗn hợp x gồm 2 kim loại Mg và R
-thí nghiệm 1: cho 8 gam hỗn hợp x vào dd hcl dư thu được 4,48 lít khí ở đktc -thí nghiệm 2: cho 16 gam hỗn hợp X tác dụng với dd h2so4 đặc, nóng, dư thu được một khí z sản phẩm khử duy nhất không màu mùi hắc. khí z này được hấp thụ hoàn toàn vào 450 ml dd 2M thu được 75,2 gam muối kali.
1 viết các pthh xảy ra và tính số mol khí z. các pu xảy ra hoàn toàn
2. xác định R
Cho 13,8 gam hỗn hợp X gồm kim loại kiềm R và Ca tác dụng hết với nước thu được 5,6 lít H2 (đktc) và dung dịch Y. Mặt khác, cho 8,58 gam kim loại R phản ứng hết với lượng dư dung dịch HCl thì thể tích khí H2 thoát ra lớn hơn 2,24 lít (đktc).
1. Tìm kim loại R?
2. Cho 15 lít hỗn hợp khí Z gồm N2 và CO2 (đktc) vào dung dịch Y. Sau khi phản ứng kết thúc thu được 8,5 gam kết tủa. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp Z?
1.
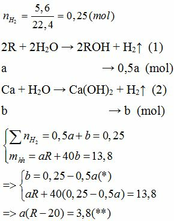
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
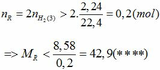
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
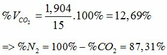
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
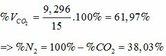
Cho 13,6 gam hỗn hợp X gồm kim loại R và oxit của R (R thuộc nhóm IIA) tác dụng vừa đủ với 150 gam dung dịch HCl 14,6%, sau phản ứng xảy ra hoàn toàn thu được dung dịch Y và 4,48 lít khí H2 (đktc).
a. Tìm R
b. Tính % các chất trong X
b. Tính C% chất tan trong dung dịch Y
Hỗn hợp X gồm Fe và kim loại M có hóa trị không đổi. Cho 15,2 gam X tác dụng với dung dịch HC1 dư, thấy thoát ra 2,24 lít khí H2 (đktc). Nếu cho lượng X như trên tác dụng với dung dịch HNO3 dư, thu được 4,48 lít khí NO (đktc). Kim loại M là
A. Ag.
B. Cu.
C. Al.
D. Mg.
Đáp án B
n H 2 = 0 , 1 ; n NO = 0 , 4 . Gọi n là hóa trị của M.
Căn cứ vào 4 đáp án ta có 2 trường hợp:
+) M là kim loại đứng trước H trong dãy hoạt động hóa học. Khi đó cả M và Fe có phản ứng với dung dịch HCl. Vì hóa trị của M không đổi nên sự chênh lệch về số electron trao đổi trong hai lần thí nghiệm là do sắt có hai mức hóa trị là II và III.
Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có: 2 n Fe + n . n M = 2 n H 2
- Khi hòa tan hỗn hợp vào dung dịch HNO3, ta có: 3 n Fe + n . n M = 3 n NO
Trừ hai vế của hai phương trình cho nhau, ta được:
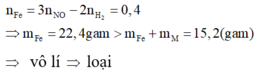
+) M là kim loại đứng sau H và trước Pt trong dãy hoạt động hóa học. Khi đó M không phản ứng được với dung dịch HCl và phản ứng được với dung dịch HNO3. Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có:

Cho 4,32 gam hỗn hợp X gồm Mg và Fe tác dụng với V lít (đktc) hỗn hợp khí Y gồm Cl2 và O2 (có tỉ khối so với H2 bằng 32,25), thu được hỗn hợp rắn Z. Cho Z vào dung dịch HCl, thu được 1,12 gam một kim loại không tan, dung dịch T và 0,224 lít H2 (đktc). Cho T vào dung dịch AgNO3 dư thu được 27,28 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
A. Al.
B. Na
C. Ca.
D. K.
Cho 8,6 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng hết với lượng dư dung dịch HCl loãng, thu được 4,48 lít khí (đktc). Kim loại X, Y là
A. Rb và Ba
B. Liti và beri
C. Natri và Canxi
D. Ba và Cs
Lấy 16 gam hỗn hợp Mg và M (có cùng số mol) tác dụng hoàn toàn với dung dịch HNO3 dư, thu được dung dịch X chứa 84 gam muối và 4,48 lít (đktc) hỗn hợp khí X gồm NO và NO2 (tỉ lệ 1:1 về số mol). Nếu lấy 22,4 gam kim loại M tác dụng hoàn toàn với 300 ml dung dịch H2SO4 1M thì thu được V lít khí (đktc). Giá trị của lớn nhất của V là?
A. 8,96.
B. 6,72.
C. 12,544.
D. 17,92.