Khi cho Mg tác dụng với axit clo hidric thì khối lượng của MgCl2 nhỏ hơn tổng khối lượng của Mg và axit clo hidric tham gia phản ứng điều này có phù hợp với định luật bảo toàn khối lượng không vì sao

Những câu hỏi liên quan
Câu 3: Cho kim loại Nhôm (Al) tác dụng với dung dịch axit Clo hidric (HCl) sau phản ứng thu được muối Nhôm Clorua (AlCl3) và 6,72 lít khí Hidro (H2) ở đktc.a. Tính khối lượng axit Clo hidric (HCl) tham gia.b. Tính khối lượng Nhôm tham gia phản ứng.
Đọc tiếp
Câu 3: Cho kim loại Nhôm (Al) tác dụng với dung dịch axit Clo hidric (HCl) sau phản ứng thu được muối Nhôm Clorua (AlCl3) và 6,72 lít khí Hidro (H2) ở đktc.
a. Tính khối lượng axit Clo hidric (HCl) tham gia.
b. Tính khối lượng Nhôm tham gia phản ứng.
a, PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,6.36,5=21,9\left(g\right)\)
b, Theo PT: \(n_{Al}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Al}=0,2.27=5,4\left(g\right)\)
Đúng 2
Bình luận (0)
nH2=6.72/22,4=0,3(mol)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
bài ra: 0,2 <-- 0,6 <-- 0,2 <-- 0,3 /mol
a) mHCl = 0,6.36,5=21,9(g)
b) mAl = 0.2.24 = 4,8(g)
Đúng 0
Bình luận (1)
Câu 3: Cho kim loại Nhôm (Al) tác dụng với dung dịch axit Clo hidric (HCl) sau phản ứng thu được muối Nhôm Clorua (AlCl3) và 6,72 lít khí Hidro (H2) ở đktc.a. Tính khối lượng axit Clo hidric (HCl) tham gia.b. Tính khối lượng Nhôm tham gia phản ứng.
Đọc tiếp
Câu 3: Cho kim loại Nhôm (Al) tác dụng với dung dịch axit Clo hidric (HCl) sau phản ứng thu được muối Nhôm Clorua (AlCl3) và 6,72 lít khí Hidro (H2) ở đktc.
a. Tính khối lượng axit Clo hidric (HCl) tham gia.
b. Tính khối lượng Nhôm tham gia phản ứng.
\(PTHH:2Al+6HCl->2AlCl_3+3H_2\)
0,2<--0,6<----------0,2<------0,3 (mol)
\(n_{H_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(m_{HCl}=n\cdot M=0,6\cdot\left(1+35,5\right)=21,9\left(g\right)\)
\(m_{AlCl_3}=n\cdot M=0,2\cdot\left(27+35,5\cdot3\right)=26,7\left(g\right)\)
Đúng 0
Bình luận (0)
a, PT: 2Al+6HCl→2AlCl3+3H2
Ta có: nAl=23nH2=0,2(mol)
⇒mAl=0,2.27=5,4(g)
Đúng 0
Bình luận (0)
a, PT: 2Al+6HCl→2AlCl3+3H2
Ta có: nAl=23nH2=0,2(mol)
⇒mAl=0,2.27=5,4(g)
Đúng 0
Bình luận (0)
1. Hãy xác định c9ng thức hóa học của hợp chất có thành phần các nguyên tố theo khối lượng lần lượt là : 56,52% Kali, 8,7% Cacbon và 34,78%Oxi. Biết khối lượng mol của hợp chất này là 138 g/mol2. Hoà tan hoan toan 13g kẽm Zn bằng dung dịch axit clo hidric HCM, phản ứng kết thúc thu được muối kẽm clorua (ZnCl2)và khi hiđrô A. Viết phương trình hóa học của phản ứng B. Tính khối lượng axit clo hidric (HCl)đã tham gia phản ứng
Đọc tiếp
1. Hãy xác định c9ng thức hóa học của hợp chất có thành phần các nguyên tố theo khối lượng lần lượt là : 56,52% Kali, 8,7% Cacbon và 34,78%Oxi. Biết khối lượng mol của hợp chất này là 138 g/mol
2. Hoà tan hoan toan 13g kẽm Zn bằng dung dịch axit clo hidric HCM, phản ứng kết thúc thu được muối kẽm clorua (ZnCl2)và khi hiđrô
A. Viết phương trình hóa học của phản ứng
B. Tính khối lượng axit clo hidric (HCl)
đã tham gia phản ứng
xem bài mình làm nhé


Bài 2 :
a) PTHH : Zn + 2HCL ------> ZnCl2 + H2
b) Theo ĐLBTKL, ta có:
mZn + mHCl = mZnCl + mH2
=> 13 + mHCl = .................
tự tính ra ... cái này bạn viết thiếu đề bài :)
Nguyễn Vy
KO có thiếu đề bài đâu
Khi cho Kẽm tác dụng với axit clohiđric thì khối lượng của kẽm clorua nhỏ hơn tổng khối lượng của kẽm và axit clohiđric tham gia phản ứng. Điều này có phù hợp với định luật bảo toàn khối lượng không ? Giải thích tại sao ?
Khi cho Kẽm tác dụng với axit clohiđric thì khối lượng của kẽm clorua nhỏ hơn tổng khối lượng của kẽm và axit clohiđric tham gia phản ứng. Điều này vẫn phù hợp với định luật bảo toàn khối lượng vì có một lượng khí hidro thoát ra ngoài
\(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Đúng 0
Bình luận (0)
Zn + 2HCl → ZnCl2 + H2↑
Theo bài: \(m_{ZnCl_2}< m_{Zn}+m_{HCl}\)
Theo định luật bảo toàn khối lượng:
\(m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\)
Tuy nhiên do H2 bay hơi ra ngoài nên:
\(m_{ZnCl_2}< m_{Zn}+m_{HCl}\)
Vậy theo bài khôi lượng kẽm clorua nhỏ hơn tổng khối lượng kẽm và axit clohiđric tham gia phản ứng vẫn phù hợp với định luật bảo toàn khối lượng
Đúng 0
Bình luận (0)
Khi cho Kẽm tác dụng với axit clohiđric thì khối lượng của kẽm clorua nhỏ hơn tổng khối lượng của kẽm và axit clohiđric tham gia phản ứng. Điều này vẫn phù hợp với định luật bảo toàn khối lượng
Vì SPU còn có 1 lượng khí H2 sinh ra
Đúng 0
Bình luận (0)
cho 4,8 gam Mg tác dunjng với dung dịch có chứa 7.3g axit clo hidric. Sau khi phản ứng kết thúc chát nào dư và dư bao nhiêu gam(Mg=24,H=1,Cl=35,5)?
\(n_{Mg}=\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
1--------2-------------1---------1
Ta có: \(\dfrac{n_{Mg}}{1}=\dfrac{0,2}{1}=0,2;\dfrac{n_{HCl}}{2}=\dfrac{0,4}{2}=0,2\)
\(\Rightarrow\dfrac{n_{Mg}}{1}=\dfrac{n_{HCl}}{2}\)
Vậy 2 chất phản ứng hết không dư
Đúng 2
Bình luận (1)
Mn giúp em câu này với ạ🙏 Cho một lượng axit axetic tác dụng với 4,8 g Mg thấy thoát ra V lít khí Hidro. B) Tính V C) Tính m của axit axetic đã tham gia phản ứng? D) Nếu đem toàn bộ khối lượng axit axetic ở trên tác dụng với rượu Etylic. Tính khối lượng este Thu được? Biết hiệu suất phản ứng đạt 60%
Thể tích khí clo cần phản ứng với kim loại M bằng 1,5 lần lượng khí sinh ra khi cho cùng lượng kim loại đó tác dụng hoàn toàn với dung dịch axit HCl dư trong cùng điều kiện. Khối lượng muối clorua sinh ra trong phản ứng với clo gấp 1,2886 lần lượng sinh ra trong phản ứng với axit HCl. Xác định kim loại M
Phương trình hóa học của phản ứng:
M + n/2HCl → M Cl n
M + mHCl → M Cl m + m/2 H 2
Theo đề bài, ta có:
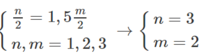
và M + 106,5 = 1,2886 (M+71)
Giải ra, ta có M = 52 (Cr)
Đúng 0
Bình luận (0)
câu 1: cho 2,4 magie tác dụng với dung dịch axit clohdric HCL , sau phản ứng thu được 9,5g magie clorua MgCl2 và 0,2g khí hidroa) Viết phương trình phản ứng trên b) Áp dụng định luật bảo toàn khối lượng, hãy tính khối lượng axit clohidric HCL đã phản ứng câu 2 : cho 13g kẽm tác dụng hoàn toàn với 14,6g axit clohidric (HCL) sau phản ứng thu được muối kẽm clorua (ZnCl2) và 0,4 khí hidro a. Viết phương trình hóa họcb. tính khối lượng muối kẽm clorua (ZnCl2) thu đượcMọi người giải giúp mình với
Đọc tiếp
câu 1: cho 2,4 magie tác dụng với dung dịch axit clohdric HCL , sau phản ứng thu được 9,5g magie clorua MgCl2 và 0,2g khí hidro
a) Viết phương trình phản ứng trên
b) Áp dụng định luật bảo toàn khối lượng, hãy tính khối lượng axit clohidric HCL đã phản ứng
câu 2 : cho 13g kẽm tác dụng hoàn toàn với 14,6g axit clohidric (HCL) sau phản ứng thu được muối kẽm clorua (ZnCl2) và 0,4 khí hidro
a. Viết phương trình hóa học
b. tính khối lượng muối kẽm clorua (ZnCl2) thu được
Mọi người giải giúp mình với
Câu 1:
\(a,PTHH:Mg+2HCl\to MgCl_2+H_2\\ b,m_{Mg}+m_{HCl}=m_{MgCl_2}+m_{H_2}\\ \Rightarrow m_{HCl}=9,5+0,2-2,4=7,3(g)\)
Câu 2:
\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\\ \Rightarrow m_{ZnCl_2}=13+14,6-0,4=27,2(g)\)
Đúng 2
Bình luận (1)
Hòa tan hoàn toàn kim loại Mg trong dung dịch axit HCl. Sau phản ứng thu được MgCl2 và 4.48 lít khí ở đktc. Tính khôí lượng Mg tham gia? Tính khối lượng HCl tham gia? Tính khối lượng MgCl2 tạo thành?
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=n_{H_2}=n_{MgCl_2}=0,2mol\\n_{HCl}=0,4mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{HCl}=0,4\cdot36,5=14,6\left(g\right)\\m_{Mg}=0,2\cdot24=4,8\left(g\right)\\m_{MgCl_2}=0,2\cdot95=19\left(g\right)\end{matrix}\right.\)
Đúng 4
Bình luận (1)
Ta có PTHH: Mg + 2HCl -----> MgCl2 + H2.
nH2=4,48/22,4=0,2(mol)
Theo PT, ta có: nMg= nH2 = 0,2(mol)
=> mMg=0,2.24=4,8(g)
Ta có: nHCl=2 . 0,2=0,4(mol)
=> mHCl=0,4.37,5=15(g)
Ta có: nMgCl2=nH2=0,2(mol)
=> mMgCl2=0,2 . 95=19(g)
Đúng 0
Bình luận (0)

































